1 . 氮氧化物的污染治理是环境科学家研究的热点之一。回答下列问题:
Ⅰ. 还原法:
还原法:
已知有关化学键的键能如下表:
(1)写出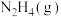 和
和 反应生成
反应生成 和
和 的热化学方程式
的热化学方程式_______ 。
Ⅱ. 还原法:
还原法:
已知反应 ;在一容积不变的密闭容器中充入
;在一容积不变的密闭容器中充入 和
和 ,
, 的平衡转化率随温度的变化如下图:
的平衡转化率随温度的变化如下图: 平衡转化率的措施是_______。
平衡转化率的措施是_______。
(3)若不使用催化剂,判断在400℃时,NO的平衡转化率是否能从M点降至P点,并说明理由_______ 。
(4)已知M点时容器的压强为3.5kPa,计算400℃时,该反应的平衡常数
_______  。
。
Ⅲ. 还原法:
还原法:
已知反应
 ,相同时间内测得选用不同催化剂时的相关实验数据如下图:
,相同时间内测得选用不同催化剂时的相关实验数据如下图:_______ 。
(6)反应合适的催化剂和温度分别是_______ 。
(7)分析两图中100~250℃时NO转化率随温度升高而增大的原因为_______ 。
Ⅰ.
 还原法:
还原法:已知有关化学键的键能如下表:
化学键 |
|
|
|
|
|
键能( | 247 | 392 | 632 | 946 | 463 |
(1)写出
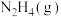 和
和 反应生成
反应生成 和
和 的热化学方程式
的热化学方程式Ⅱ.
 还原法:
还原法:已知反应
 ;在一容积不变的密闭容器中充入
;在一容积不变的密闭容器中充入 和
和 ,
, 的平衡转化率随温度的变化如下图:
的平衡转化率随温度的变化如下图: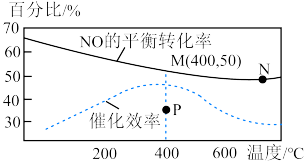
 平衡转化率的措施是_______。
平衡转化率的措施是_______。A.平衡后再充入一定量的 | B.平衡后再充入一定量的 |
| C.升高反应温度 | D.起始时充入 和 和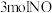 |
(3)若不使用催化剂,判断在400℃时,NO的平衡转化率是否能从M点降至P点,并说明理由
(4)已知M点时容器的压强为3.5kPa,计算400℃时,该反应的平衡常数

 。
。Ⅲ.
 还原法:
还原法:已知反应

 ,相同时间内测得选用不同催化剂时的相关实验数据如下图:
,相同时间内测得选用不同催化剂时的相关实验数据如下图:
(6)反应合适的催化剂和温度分别是
(7)分析两图中100~250℃时NO转化率随温度升高而增大的原因为
您最近一年使用:0次
2 . 常温下,用KOH溶液分别滴定 、
、 溶液、
溶液、 溶液,
溶液, [
[ 表示负对数,
表示负对数, 表示
表示 、
、 、
、 ]随pH变化的关系图,已知
]随pH变化的关系图,已知 ,下列说法正确的是
,下列说法正确的是
 、
、 溶液、
溶液、 溶液,
溶液, [
[ 表示负对数,
表示负对数, 表示
表示 、
、 、
、 ]随pH变化的关系图,已知
]随pH变化的关系图,已知 ,下列说法正确的是
,下列说法正确的是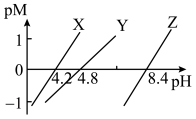
A. 的电离平衡常数 的电离平衡常数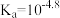 |
B.直线X代表滴定 溶液的变化关系 溶液的变化关系 |
C.将物质的量均为0.1mol的 、 、 溶于 溶于 水中快速搅拌均匀,该分散系中 水中快速搅拌均匀,该分散系中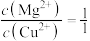 |
D. 易溶于 易溶于 |
您最近一年使用:0次
3 . 常温下,已知亚磷酸(H3PO3二元弱酸)溶液中含磷物种浓度之和为0.1mol·L-1,溶液中各含磷物种的pc与pOH关系如图所示(纵坐标数值上小下大,横坐标数值左小右大)。图中pc表示各含磷物种浓度的负对数(pc=-lgc),pOH对数[pOH=-lgc(OH-)]。x、y、z三点的坐标分别为x(7.3,1.3),y(10.0,3.6),z(12.6,1.3)。下列说法错误的是

A.H3PO3的结构简式为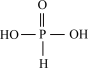 |
B.曲线①表示pc( )随pOH的变化 )随pOH的变化 |
C.H3PO3+HPO  2H2PO 2H2PO 的平衡常数K=1.0×106.3 的平衡常数K=1.0×106.3 |
D.pH=4的溶液中,c(H2PO )=0.1mol·L-1-2c(HPO )=0.1mol·L-1-2c(HPO ) ) |
您最近一年使用:0次
4 . 室温下,向Mg(NO3)2溶液、HF溶液、CH3CH2COOH溶液中分别滴加NaOH溶液,测得溶液中pH与pX[pX=-lgX,X代表 、
、 、
、 ]的关系如图所示。
]的关系如图所示。
 ,HF的酸性比CH3CH2COOH强。下列叙述正确的是
,HF的酸性比CH3CH2COOH强。下列叙述正确的是
已知:
 、
、 、
、 ]的关系如图所示。
]的关系如图所示。
 ,HF的酸性比CH3CH2COOH强。下列叙述正确的是
,HF的酸性比CH3CH2COOH强。下列叙述正确的是已知:

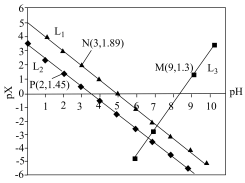
A. 代表的是pH与 代表的是pH与 的关系 的关系 |
B. 的 的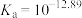 |
C.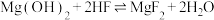 的 的 |
| D.含相同浓度NaF、HF的混合溶液的pH>7 |
您最近一年使用:0次
2024-04-01更新
|
580次组卷
|
6卷引用:2024届山西省太原市第五中学高三下学期一模理综试题-高中化学
5 . 羟基自由基(·OH)是自然界中氧化性仅次于氟的氧化剂,在直流电源的作用下,利用如图所示装置处理含苯酚废水和含甲醛废水(已知: 在膜a、b间解离为
在膜a、b间解离为 和
和 )。下列说法错误的是
)。下列说法错误的是
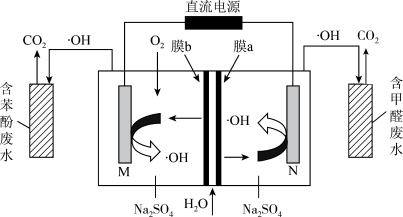
 在膜a、b间解离为
在膜a、b间解离为 和
和 )。下列说法错误的是
)。下列说法错误的是
| A.直流电源的电极电势:右端高于左端 |
B.阳极的电极反应式为: |
C.电解质 的作用是可以增强溶液的导电能力 的作用是可以增强溶液的导电能力 |
D.每处理9.4g苯酚,理论上有2.8mol 透过膜b 透过膜b |
您最近一年使用:0次
解题方法
6 . 1,3-丙二胺[H2N(CH2)3NH2]是一种二元弱碱[可简写为M(OH)2],25℃时,向一定浓度的MCl2溶液中逐滴加入NaOH溶液,以X表示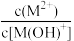 或
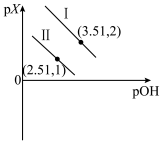
或 已知pX=-lgX,混合溶液中pX与pOH的关系如图所示。下列说法正确的是
已知pX=-lgX,混合溶液中pX与pOH的关系如图所示。下列说法正确的是
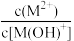 或
或 已知pX=-lgX,混合溶液中pX与pOH的关系如图所示。下列说法正确的是
已知pX=-lgX,混合溶液中pX与pOH的关系如图所示。下列说法正确的是
A.曲线Ⅱ表示p{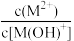 }与pOH的关系 }与pOH的关系 |
| B.M(OH)2第一步电离的电离常数为1×10-1.51 |
| C.pOH=4.01时,c(M2+)=c[M(OH)2]>c[M(OH)+] |
| D.pOH=3.51时,3c[M(OH)2]+c(OH-)=c(H+)+c(Na+) |
您最近一年使用:0次
名校
解题方法
7 . 高纯四氧化三锰是电子工业生产锰锌氧软磁材料重要原料之一、以菱锰矿(主要成分为 ,含
,含 和少量Fe、Cu、Ni、Ca、Mg等元素)为原料制备四氧化三锰工艺流程如下图所示。
和少量Fe、Cu、Ni、Ca、Mg等元素)为原料制备四氧化三锰工艺流程如下图所示。
(1)酸浸时 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(2)“滤渣1”的主要成分为 、
、 ,还含有
,还含有___________ (填化学式)。
(3)福美钠的化学式为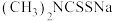 。生成福美镍沉淀的结构为
。生成福美镍沉淀的结构为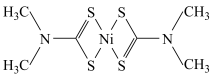 ,其中硫与镍之间的结合方式为下列中的
,其中硫与镍之间的结合方式为下列中的___________ (填标号);
A.离子键 B.金属键 C.氢键 D.配位键
25℃,电离常数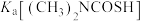
___________  (填“大于”“小于”或“等于”),其判断理由是
(填“大于”“小于”或“等于”),其判断理由是___________ 。
(4)除钙镁时, 、
、 沉淀后溶液中
沉淀后溶液中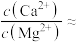
___________ [已知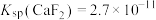 、
、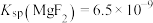 ]
]
(5)除硅时,絮凝剂为阳离子型聚丙烯酰胺,可通过“吸附—电中和—架桥”使硅酸胶体絮凝沉淀,硅酸胶体粒子带___________ 电荷(填“正”或“负”)。
(6) 在空气中被氧化生成
在空气中被氧化生成 反应的化学方程式为
反应的化学方程式为___________ 。
(7) 可表示为
可表示为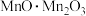 ,温度高于1170℃时属于立方晶体,其中
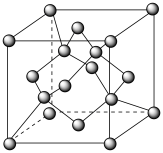
,温度高于1170℃时属于立方晶体,其中 和Mn3+占据晶胞的顶点、面心及内部交错的4个小立方体的体心,与金刚石晶胞中碳原子占据的位置相似(金刚石晶胞如图所示)。若
和Mn3+占据晶胞的顶点、面心及内部交错的4个小立方体的体心,与金刚石晶胞中碳原子占据的位置相似(金刚石晶胞如图所示)。若 晶体的密度为
晶体的密度为 ,则晶胞参数
,则晶胞参数
___________ pm(列出计算式,阿伏加德罗常数的值为 )。
)。
 ,含
,含 和少量Fe、Cu、Ni、Ca、Mg等元素)为原料制备四氧化三锰工艺流程如下图所示。
和少量Fe、Cu、Ni、Ca、Mg等元素)为原料制备四氧化三锰工艺流程如下图所示。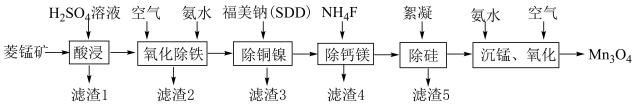
(1)酸浸时
 发生反应的离子方程式为
发生反应的离子方程式为(2)“滤渣1”的主要成分为
 、
、 ,还含有
,还含有(3)福美钠的化学式为
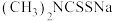 。生成福美镍沉淀的结构为
。生成福美镍沉淀的结构为 ,其中硫与镍之间的结合方式为下列中的
,其中硫与镍之间的结合方式为下列中的A.离子键 B.金属键 C.氢键 D.配位键
25℃,电离常数
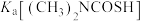
 (填“大于”“小于”或“等于”),其判断理由是
(填“大于”“小于”或“等于”),其判断理由是(4)除钙镁时,
 、
、 沉淀后溶液中
沉淀后溶液中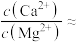
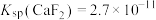 、
、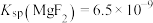 ]
](5)除硅时,絮凝剂为阳离子型聚丙烯酰胺,可通过“吸附—电中和—架桥”使硅酸胶体絮凝沉淀,硅酸胶体粒子带
(6)
 在空气中被氧化生成
在空气中被氧化生成 反应的化学方程式为
反应的化学方程式为(7)
 可表示为
可表示为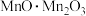 ,温度高于1170℃时属于立方晶体,其中
,温度高于1170℃时属于立方晶体,其中 和Mn3+占据晶胞的顶点、面心及内部交错的4个小立方体的体心,与金刚石晶胞中碳原子占据的位置相似(金刚石晶胞如图所示)。若
和Mn3+占据晶胞的顶点、面心及内部交错的4个小立方体的体心,与金刚石晶胞中碳原子占据的位置相似(金刚石晶胞如图所示)。若 晶体的密度为
晶体的密度为 ,则晶胞参数
,则晶胞参数
 )。
)。
您最近一年使用:0次
2024-01-06更新
|
646次组卷
|
3卷引用:2024届山西省介休市定阳高级中学高三下学期模拟考试(九)理综试题-高中化学
解题方法
8 . 1-丁烯是仅次于乙烯和丙烯的重要石油化工基本原料,可以利用正丁烷催化脱氢制备,催化脱氢又分为无氧催化脱氢和有氧催化脱氢。实际化工生产中需对反应条件(催化剂、温度等)进行探究,以获取最佳效益。
已知:I.温度过高会引发正丁烷裂解生成低碳烃类的副反应。
II.产物收率=生成某产物的原料量/投入的原料量×100%。
(1)利用正丁烷无氧催化脱氢制备1-丁烯反应原理如下:
CH3CH2CH2CH3 H2C=CHCH2CH3+H2 ΔH
H2C=CHCH2CH3+H2 ΔH
已知CH3 CH2CH2CH3、CH2 =CHCH2CH3、H2的燃烧热分别为2 878 kJ/mol、2 720 kJ/mol、286 kJ/mol,计算ΔH=___________ 。
(2)无氧催化脱氢用Pt系催化剂时,正丁烷单位时间转化率和1-丁烯选择性如表所示。
①仅从1-丁烯选择性的角度考虑,应选择的催化剂为___________ (填催化剂序号,下同)。
②工业上,从1-丁烯单位时间收率的角度考虑,应选择的最佳催化剂为___________ 。
(3)其他条件相同,30 min时测得正丁烷转化率、1-丁烯收率随温度的变化关系如图所示。
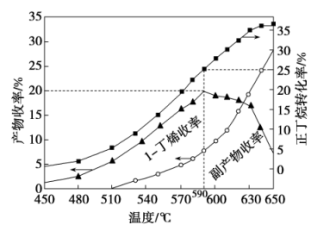
温度高于590 ℃时1-丁烯收率降低的原因是_________________ 。
(4)有氧催化脱氢通常选择O2或CO2为氧化剂,VOx-MgO为催化剂,反应原理如下:
2CH3CH2CH2CH3+O2 2CH2 =CHCH2CH3 +2H2O i
2CH2 =CHCH2CH3 +2H2O i
CH3 CH2CH2CH3+CO2 H2C=CHCH2CH3+H2O+CO ii
H2C=CHCH2CH3+H2O+CO ii
一定温度下,在体积为10 L的恒容密闭容器中,加入10 mol CH3CH2CH2CH3、7 mol O2、3 mol CO2进行反应i和ii.测得初始压强为20kPa,经过10h,反应达到平衡,此时压强变成25kPa,其中O2的体积分数为16%。回答下列问题:
①v(O2)=___________ kPa/h (用O2分压表示速率)。
②该温度下,反应ii的平衡常数Kp=___________ kPa。
③O2为氧化剂时,1-丁烯的选择性明显低于CO2为氧化剂时的选择性,分析可能原因:______________ 。
已知:I.温度过高会引发正丁烷裂解生成低碳烃类的副反应。
II.产物收率=生成某产物的原料量/投入的原料量×100%。
(1)利用正丁烷无氧催化脱氢制备1-丁烯反应原理如下:
CH3CH2CH2CH3
 H2C=CHCH2CH3+H2 ΔH
H2C=CHCH2CH3+H2 ΔH已知CH3 CH2CH2CH3、CH2 =CHCH2CH3、H2的燃烧热分别为2 878 kJ/mol、2 720 kJ/mol、286 kJ/mol,计算ΔH=
(2)无氧催化脱氢用Pt系催化剂时,正丁烷单位时间转化率和1-丁烯选择性如表所示。
| 催化剂 | 单位时间转化率/% | 1-丁烯选择性/% |
| 催化剂1:PtSn/γ-Al2O3 | 23.0 | 92.0 |
| 催化剂2:PtSnSr0.2/γ-Al2O3 | 38.5 | 88.1 |
| 催化剂3:PtSn(0.3%)/MgAl2O4 | 27.0 | 98.9 |
②工业上,从1-丁烯单位时间收率的角度考虑,应选择的最佳催化剂为
(3)其他条件相同,30 min时测得正丁烷转化率、1-丁烯收率随温度的变化关系如图所示。

温度高于590 ℃时1-丁烯收率降低的原因是
(4)有氧催化脱氢通常选择O2或CO2为氧化剂,VOx-MgO为催化剂,反应原理如下:
2CH3CH2CH2CH3+O2
 2CH2 =CHCH2CH3 +2H2O i
2CH2 =CHCH2CH3 +2H2O iCH3 CH2CH2CH3+CO2
 H2C=CHCH2CH3+H2O+CO ii
H2C=CHCH2CH3+H2O+CO ii一定温度下,在体积为10 L的恒容密闭容器中,加入10 mol CH3CH2CH2CH3、7 mol O2、3 mol CO2进行反应i和ii.测得初始压强为20kPa,经过10h,反应达到平衡,此时压强变成25kPa,其中O2的体积分数为16%。回答下列问题:
①v(O2)=
②该温度下,反应ii的平衡常数Kp=
③O2为氧化剂时,1-丁烯的选择性明显低于CO2为氧化剂时的选择性,分析可能原因:
您最近一年使用:0次
解题方法
9 . 苯基硫醇(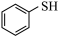 )又叫苯硫酚,是一种医药中间体,工业制备原理如下:
)又叫苯硫酚,是一种医药中间体,工业制备原理如下:
主反应: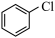 (g)+H2S(g)
(g)+H2S(g)
 (g)+HCl(g) ΔH=-16.8kJ ·mol-1
(g)+HCl(g) ΔH=-16.8kJ ·mol-1
副反应: (g)+H2S(g)
(g)+H2S(g)
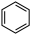 (g)+HCl(g)+
(g)+HCl(g)+ S8(g) ΔH =-45.8 kJ ·mol-1
S8(g) ΔH =-45.8 kJ ·mol-1
回答下列问题:
(1)一定温度下,相同时间内,苯基硫醇浓度增大的程度明显高于苯,其原因可能是主反应的活化能较___________ (填“大”或“小”)。
(2)T℃时,在容积为5L的恒容密闭容器中,充入物质的量均为2mol的氯苯和硫化氢,发生上述主反应和副反应,达到平衡时苯基硫醇的物质的量分数为25%,平衡时总压是初始总压的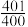 倍。
倍。
①平衡时苯的浓度为___________ mol·L-1。
②主反应Kp=___________ (列出算式)。
(3)恒容密闭容器中,在投料比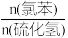 =1的条件下,测得苯基硫醇和苯的收率(
=1的条件下,测得苯基硫醇和苯的收率( )在相同时间内随温度的变化如下图所示:
)在相同时间内随温度的变化如下图所示:
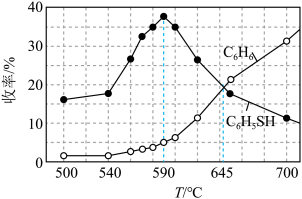
①温度小于590℃,苯基硫醇的收率随温度升高而增大的可能原因是___________ 。
②590℃时,副反应未达到平衡,理由是___________ 。
③645℃时,H2S中硫原子的物质的量是S8中硫原子的物质的量___________ 倍。
(4)反应 (g)
(g) 
 (g) +
(g) + S8(g)的ΔH =
S8(g)的ΔH =___________ kJ ·mol-1,恒温恒容条件下,该分解反应达到平衡时,增大反应物苯基硫醇的浓度,再次达到平衡后,苯基硫醇的转化率___________ (填“增大”“减小”或“不变”)。
 )又叫苯硫酚,是一种医药中间体,工业制备原理如下:
)又叫苯硫酚,是一种医药中间体,工业制备原理如下:主反应:
 (g)+H2S(g)
(g)+H2S(g)
 (g)+HCl(g) ΔH=-16.8kJ ·mol-1
(g)+HCl(g) ΔH=-16.8kJ ·mol-1副反应:
 (g)+H2S(g)
(g)+H2S(g)
 (g)+HCl(g)+
(g)+HCl(g)+ S8(g) ΔH =-45.8 kJ ·mol-1
S8(g) ΔH =-45.8 kJ ·mol-1回答下列问题:
(1)一定温度下,相同时间内,苯基硫醇浓度增大的程度明显高于苯,其原因可能是主反应的活化能较
(2)T℃时,在容积为5L的恒容密闭容器中,充入物质的量均为2mol的氯苯和硫化氢,发生上述主反应和副反应,达到平衡时苯基硫醇的物质的量分数为25%,平衡时总压是初始总压的
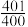 倍。
倍。①平衡时苯的浓度为
②主反应Kp=
(3)恒容密闭容器中,在投料比
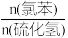 =1的条件下,测得苯基硫醇和苯的收率(
=1的条件下,测得苯基硫醇和苯的收率( )在相同时间内随温度的变化如下图所示:
)在相同时间内随温度的变化如下图所示: 
①温度小于590℃,苯基硫醇的收率随温度升高而增大的可能原因是
②590℃时,副反应未达到平衡,理由是
③645℃时,H2S中硫原子的物质的量是S8中硫原子的物质的量
(4)反应
 (g)
(g) 
 (g) +
(g) + S8(g)的ΔH =
S8(g)的ΔH =
您最近一年使用:0次
名校
解题方法
10 . 一定条件下向某密闭容器中加入 、
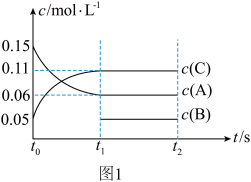
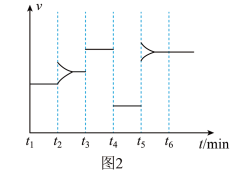
、 和一定量的B三种气体,图1表示各物质浓度随时间的变化关系,图2表示速率随时间的变化关系,
和一定量的B三种气体,图1表示各物质浓度随时间的变化关系,图2表示速率随时间的变化关系, 时刻各改变一种条件,且改变的条件均不同。若
时刻各改变一种条件,且改变的条件均不同。若 时刻改变的条件是压强,则下列说法错误的是
时刻改变的条件是压强,则下列说法错误的是
 、
、 和一定量的B三种气体,图1表示各物质浓度随时间的变化关系,图2表示速率随时间的变化关系,
和一定量的B三种气体,图1表示各物质浓度随时间的变化关系,图2表示速率随时间的变化关系, 时刻各改变一种条件,且改变的条件均不同。若
时刻各改变一种条件,且改变的条件均不同。若 时刻改变的条件是压强,则下列说法错误的是
时刻改变的条件是压强,则下列说法错误的是

A.若 ,则前 ,则前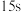 的平均反应速率 的平均反应速率 |
B.该反应的化学方程式为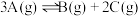 |
C.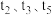 时刻改变的条件分别是升高温度、加入催化剂、增大反应物浓度 时刻改变的条件分别是升高温度、加入催化剂、增大反应物浓度 |
D.B的起始物质的量为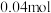 |
您最近一年使用:0次
2023-01-17更新
|
851次组卷
|
21卷引用:山西省实验中学2018届高三上学期学业质量监测化学试题
山西省实验中学2018届高三上学期学业质量监测化学试题山西省运城市景胜中学2020-2021学年高二10月月考化学试题黑龙江省大庆市铁人中学2018-2019学年高一下学期期末化学试题江西省吉安市遂川中学2019—2020学年高二上学期第一次月考化学试题(A)黑龙江省大庆实验中学2019-2020学年高二上学期第一次月考化学试题甘肃省天水市天水一中2019-2020学年高二(普通班)上学期第一次月考化学(理)试题天津市六校(静海一中,杨村中学,宝坻一中,大港一中等)2019-2020学年高二上学期期中联考化学试题天津市七校2019-2020学年高二上学期期中联考化学试题广东省揭阳市惠来县第一中学2019-2020学年高二上学期期中考试化学试题2020届高三化学二轮冲刺新题专练——化学反应速率的图像分析(提升练)黑龙江省鹤岗市第一中学2019-2020学年高一下学期期末考试化学试题(已下线)第17讲 化学平衡计算与图像-2021年高考化学一轮复习名师精讲练鲁科版(2019)选择性必修1第2章 化学反应的方向、限度与速率 第2节 化学反应的限度 课时2 反应条件对化学平衡的影响高中必刷题高二选择性必修1第二章 化学反应速率与化学平衡 第二节 化学平衡 课时3 影响化学平衡的因素(已下线)第二章 化学反应速率与化学平衡(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)河南省许昌市第三中学2020-2021学年高二3月月考化学试题选择性必修1 专题2 第三单元 课时1 影响化学平衡的因素(已下线)6.2.2 化学平衡(第2课时 化学平衡移动)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)河南省商丘市回民中学2022-2023学年高三上学期期末考试(线上)化学试题黑龙江省牡丹江市第三高级中学2023-2024学年高二上学期期中考试化学试题四川省广安市华蓥中学2023-2024学年高二上学期12月月考化学试题






 )
)

