1 . 常温下,分别在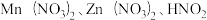 溶液中滴加NaOH溶液,溶液中
溶液中滴加NaOH溶液,溶液中 ,X代表
,X代表 、
、 、
、 、
、 与pH关系如图所示。已知:
与pH关系如图所示。已知: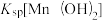 >
>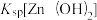 。下列叙述正确的是
。下列叙述正确的是
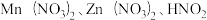 溶液中滴加NaOH溶液,溶液中
溶液中滴加NaOH溶液,溶液中 ,X代表
,X代表 、
、 、
、 、
、 与pH关系如图所示。已知:
与pH关系如图所示。已知: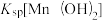 >
>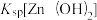 。下列叙述正确的是
。下列叙述正确的是
A.图中 代表: 代表: 与pH的关系, 与pH的关系,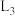 代表 代表 与pH的关系 与pH的关系 |
B.同时产生两种沉淀时, |
C.再向体系中加入硫化钠溶液, 减少, 减少,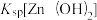 将变小 将变小 |
D. 的平衡常数 的平衡常数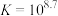 |
您最近一年使用:0次
2 . 工业上利用锌焙砂(主要成分为  ,含有少量
,含有少量 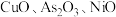 等)生产高纯
等)生产高纯  的流程示意图如下。
的流程示意图如下。
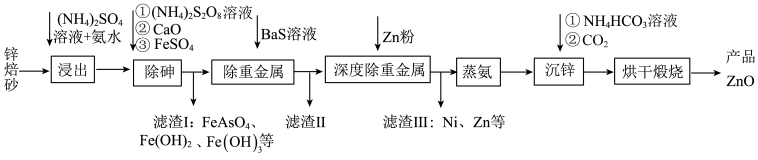
(1)用足量 溶液和氨水 “浸出” 锌焙砂。
溶液和氨水 “浸出” 锌焙砂。
①“浸出”前,锌焙砂预先粉碎的目的是___________ 。
②通过“浸出”步骤,锌焙砂中的 转化为
转化为  ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(2)“浸出”时 转化为
转化为  。“除砷”步骤①中用
。“除砷”步骤①中用  作氧化剂,步骤①反应中的氧化剂与还原剂物质 的量之比为
作氧化剂,步骤①反应中的氧化剂与还原剂物质 的量之比为___________
(3)“除重金属”时,加入 溶液。滤渣II中含有的主要物质是
溶液。滤渣II中含有的主要物质是___________ 和  。
。
(4)“蒸氨”时会出现白色固体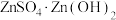 ,运用平衡移动原理解释原因:
,运用平衡移动原理解释原因:___________ 。
(5)“沉锌”步骤①中加入足量 溶液将白色固体转化为
溶液将白色固体转化为  的离子方程式为
的离子方程式为___________ 。
(6)煅烧”步骤中,在一定温度下,煅烧 一定时间后固体失重质量分数为
一定时间后固体失重质量分数为  ,则
,则  的分解率 为
的分解率 为___________  (保留到小数点后一位)。已知: 固体失重质量分数
(保留到小数点后一位)。已知: 固体失重质量分数  。
。
(7)该流程中可循环利用的物质有___________ (答出任意 2 种即可)
 ,含有少量
,含有少量 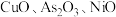 等)生产高纯
等)生产高纯  的流程示意图如下。
的流程示意图如下。
(1)用足量
 溶液和氨水 “浸出” 锌焙砂。
溶液和氨水 “浸出” 锌焙砂。①“浸出”前,锌焙砂预先粉碎的目的是
②通过“浸出”步骤,锌焙砂中的
 转化为
转化为  ,该反应的离子方程式为
,该反应的离子方程式为(2)“浸出”时
 转化为
转化为  。“除砷”步骤①中用
。“除砷”步骤①中用  作氧化剂,步骤①反应中的氧化剂与还原剂物质 的量之比为
作氧化剂,步骤①反应中的氧化剂与还原剂物质 的量之比为(3)“除重金属”时,加入
 溶液。滤渣II中含有的主要物质是
溶液。滤渣II中含有的主要物质是 。
。(4)“蒸氨”时会出现白色固体
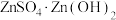 ,运用平衡移动原理解释原因:
,运用平衡移动原理解释原因:(5)“沉锌”步骤①中加入足量
 溶液将白色固体转化为
溶液将白色固体转化为  的离子方程式为
的离子方程式为(6)煅烧”步骤中,在一定温度下,煅烧
 一定时间后固体失重质量分数为
一定时间后固体失重质量分数为  ,则
,则  的分解率 为
的分解率 为 (保留到小数点后一位)。已知: 固体失重质量分数
(保留到小数点后一位)。已知: 固体失重质量分数  。
。(7)该流程中可循环利用的物质有
您最近一年使用:0次
名校
解题方法
3 . 氧钒(Ⅳ)碱式碳酸铵晶体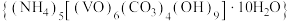 是制备多种含钒产品的前驱体。已知:氧钒(Ⅳ)碱式碳酸铵晶体呈紫红色,难溶于水和乙醇。实验室制备该晶体的流程如图所示。
是制备多种含钒产品的前驱体。已知:氧钒(Ⅳ)碱式碳酸铵晶体呈紫红色,难溶于水和乙醇。实验室制备该晶体的流程如图所示。
 溶液
溶液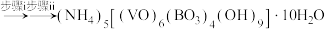
步骤i:用 排除装置中的氧气,将
排除装置中的氧气,将 溶液缓慢加入足量
溶液缓慢加入足量 溶液中,有气泡产生,析出紫红色晶体。
溶液中,有气泡产生,析出紫红色晶体。
步骤ii:待反应结束后,在 保护气的环境中,将混合液静置一段时间,抽滤,所得晶体用饱和
保护气的环境中,将混合液静置一段时间,抽滤,所得晶体用饱和 溶液洗涤3次,再用无水乙醇洗涤2次,得到粗产品。
溶液洗涤3次,再用无水乙醇洗涤2次,得到粗产品。
(1)仪器E的名称为________ ;上述装置连接的顺序为________ 。
(2)装置B中发生反应的化学方程式是________ 。
(3)①预测 保护气排除氧气的目的是
保护气排除氧气的目的是________ ;判断装置中的 基本上排尽的方法是
基本上排尽的方法是________ (填实验现象)。
②晶体用无水乙醇代替水洗涤的目的是________ 。
(4)称bg粗品,用 溶液氧化,再除去多余的
溶液氧化,再除去多余的 (方法略),滴入2滴
(方法略),滴入2滴 溶液,最后用
溶液,最后用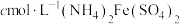 标准溶液滴定,滴定终点消耗标准溶液的体积如下图(已知钒的相对原子质量为M,滴定反应为
标准溶液滴定,滴定终点消耗标准溶液的体积如下图(已知钒的相对原子质量为M,滴定反应为 )。
)。
I.配制 标准溶液:称量→溶解→冷却→操作①→洗涤→注入→混匀→定容→操作②→装瓶贴标签,下列图示中,操作①②分别为
标准溶液:称量→溶解→冷却→操作①→洗涤→注入→混匀→定容→操作②→装瓶贴标签,下列图示中,操作①②分别为________ (填序号)。 溶液的体积为
溶液的体积为________ ;产品中钒的质量分数为________ %(用含b、c、M的代数式表示)。
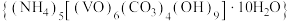 是制备多种含钒产品的前驱体。已知:氧钒(Ⅳ)碱式碳酸铵晶体呈紫红色,难溶于水和乙醇。实验室制备该晶体的流程如图所示。
是制备多种含钒产品的前驱体。已知:氧钒(Ⅳ)碱式碳酸铵晶体呈紫红色,难溶于水和乙醇。实验室制备该晶体的流程如图所示。 溶液
溶液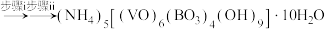
步骤i:用
 排除装置中的氧气,将
排除装置中的氧气,将 溶液缓慢加入足量
溶液缓慢加入足量 溶液中,有气泡产生,析出紫红色晶体。
溶液中,有气泡产生,析出紫红色晶体。步骤ii:待反应结束后,在
 保护气的环境中,将混合液静置一段时间,抽滤,所得晶体用饱和
保护气的环境中,将混合液静置一段时间,抽滤,所得晶体用饱和 溶液洗涤3次,再用无水乙醇洗涤2次,得到粗产品。
溶液洗涤3次,再用无水乙醇洗涤2次,得到粗产品。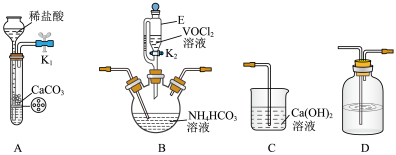
(1)仪器E的名称为
(2)装置B中发生反应的化学方程式是
(3)①预测
 保护气排除氧气的目的是
保护气排除氧气的目的是 基本上排尽的方法是
基本上排尽的方法是②晶体用无水乙醇代替水洗涤的目的是
(4)称bg粗品,用
 溶液氧化,再除去多余的
溶液氧化,再除去多余的 (方法略),滴入2滴
(方法略),滴入2滴 溶液,最后用
溶液,最后用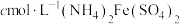 标准溶液滴定,滴定终点消耗标准溶液的体积如下图(已知钒的相对原子质量为M,滴定反应为
标准溶液滴定,滴定终点消耗标准溶液的体积如下图(已知钒的相对原子质量为M,滴定反应为 )。
)。I.配制
 标准溶液:称量→溶解→冷却→操作①→洗涤→注入→混匀→定容→操作②→装瓶贴标签,下列图示中,操作①②分别为
标准溶液:称量→溶解→冷却→操作①→洗涤→注入→混匀→定容→操作②→装瓶贴标签,下列图示中,操作①②分别为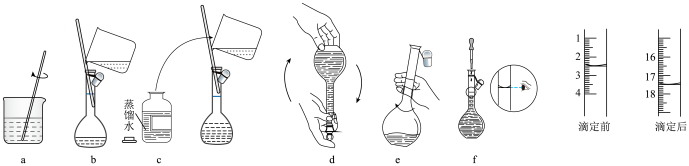
 溶液的体积为
溶液的体积为
您最近一年使用:0次
2024-06-04更新
|
170次组卷
|
2卷引用:2024届四川省成都石室中学高三下学期5月高考适应性考试(一)理科综合试卷-高中化学
名校
4 . 配合物在许多尖端领域如激光材料、超导材料、抗癌药物的研究、催化剂的研制、自组装超分子等方面有广泛的应用。回答下列问题:
(1)《诗经》言“缟衣茹藘(茜草)”,茜草中的茜素与矾土中的 、
、 生成的红色配合物X是最早的媒染染料。
生成的红色配合物X是最早的媒染染料。 的核外电子的运动状态有
的核外电子的运动状态有________ 种,配合物X中 的配体有
的配体有________ ,茜素的水溶性较好的主要原因是________ 。
(2)Ni与CO形成的配合物 为无色液体,易溶于
为无色液体,易溶于 、
、 等有机溶剂。
等有机溶剂。 为
为________ (填“极性”或“非极性”)分子,分子中 键与
键与 键的个数之比为
键的个数之比为________ 。
(3)向 溶液中滴加铁氰化钾溶液后,经提纯、结晶可得到一种蓝色晶体
溶液中滴加铁氰化钾溶液后,经提纯、结晶可得到一种蓝色晶体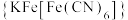 。实验表明,
。实验表明, 、
、 、
、 通过配位键构成了晶体的骨架,其局部结构如图1,记为Ⅰ型立方结构。将Ⅰ型立方结构平移、旋转、并置,可得到晶体的复晶胞(如图2,记为Ⅱ型立方结构,下层左后的小立方体g未标出)。
通过配位键构成了晶体的骨架,其局部结构如图1,记为Ⅰ型立方结构。将Ⅰ型立方结构平移、旋转、并置,可得到晶体的复晶胞(如图2,记为Ⅱ型立方结构,下层左后的小立方体g未标出)。________ 实验,可确定该晶体结构。
② 的配位数为
的配位数为________ 。
③若 位于Ⅱ型立方结构的棱心和体心,则
位于Ⅱ型立方结构的棱心和体心,则 位于Ⅱ型立方结构的
位于Ⅱ型立方结构的________ ;一个Ⅱ型立方结构中含________ 个 ;若该蓝色晶体的密度为
;若该蓝色晶体的密度为 ,Ⅱ型立方结构的边长为anm,则阿伏加德罗常数的值可表示为
,Ⅱ型立方结构的边长为anm,则阿伏加德罗常数的值可表示为________ 。
(1)《诗经》言“缟衣茹藘(茜草)”,茜草中的茜素与矾土中的
 、
、 生成的红色配合物X是最早的媒染染料。
生成的红色配合物X是最早的媒染染料。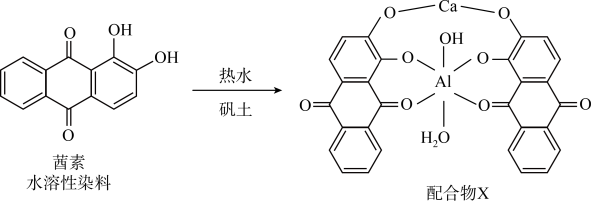
 的核外电子的运动状态有
的核外电子的运动状态有 的配体有
的配体有(2)Ni与CO形成的配合物
 为无色液体,易溶于
为无色液体,易溶于 、
、 等有机溶剂。
等有机溶剂。 为
为 键与
键与 键的个数之比为
键的个数之比为(3)向
 溶液中滴加铁氰化钾溶液后,经提纯、结晶可得到一种蓝色晶体
溶液中滴加铁氰化钾溶液后,经提纯、结晶可得到一种蓝色晶体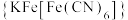 。实验表明,
。实验表明, 、
、 、
、 通过配位键构成了晶体的骨架,其局部结构如图1,记为Ⅰ型立方结构。将Ⅰ型立方结构平移、旋转、并置,可得到晶体的复晶胞(如图2,记为Ⅱ型立方结构,下层左后的小立方体g未标出)。
通过配位键构成了晶体的骨架,其局部结构如图1,记为Ⅰ型立方结构。将Ⅰ型立方结构平移、旋转、并置,可得到晶体的复晶胞(如图2,记为Ⅱ型立方结构,下层左后的小立方体g未标出)。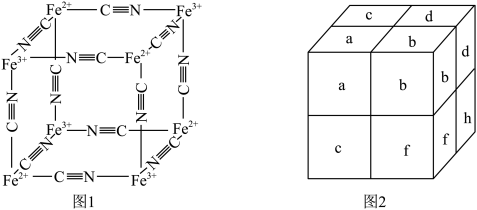
②
 的配位数为
的配位数为③若
 位于Ⅱ型立方结构的棱心和体心,则
位于Ⅱ型立方结构的棱心和体心,则 位于Ⅱ型立方结构的
位于Ⅱ型立方结构的 ;若该蓝色晶体的密度为
;若该蓝色晶体的密度为 ,Ⅱ型立方结构的边长为anm,则阿伏加德罗常数的值可表示为
,Ⅱ型立方结构的边长为anm,则阿伏加德罗常数的值可表示为
您最近一年使用:0次
解题方法
5 . 肼为二元弱碱,在水中的电离方式与氨相似。常温下,向一定浓度肼 水溶液中通入
水溶液中通入 (忽略溶液体积变化),测得
(忽略溶液体积变化),测得 与
与 [X为
[X为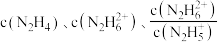 ]的变化关系如图所示。下列说法正确的是
]的变化关系如图所示。下列说法正确的是
 水溶液中通入
水溶液中通入 (忽略溶液体积变化),测得
(忽略溶液体积变化),测得 与
与 [X为
[X为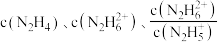 ]的变化关系如图所示。下列说法正确的是
]的变化关系如图所示。下列说法正确的是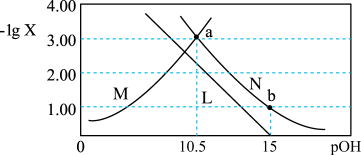
A.曲线N表示 与 与 的变化关系 的变化关系 |
B.常温下,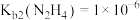 |
C.a点溶液中: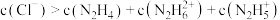 |
D.b点溶液中: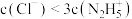 |
您最近一年使用:0次
2024-04-16更新
|
296次组卷
|
2卷引用:2024届四川省雅安市天全中学高三下学期模拟预测化学试题
6 . Si、S、Se在自然界中形成多种多样的物质结构。回答下列问题:
(1)Se与O同族,电负性较大的是_____ ;基态Se原子的价电子运动状态有_____ 种。
(2)已知液态的二氧化硫可以发生类似水的自电离: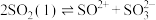 。
。 中各原子满足8电子结构,则其
中各原子满足8电子结构,则其 键和
键和 键数目之比为
键数目之比为__ , 的空间结构为
的空间结构为_______ 。
(3)有一种观点认为:由于硅的价层有可以利用的空d轨道,而碳没有,因此两者化合物结构和性质存在较大差异。化合物 和
和 的结构如图所示,
的结构如图所示, 为平面形,二者中N的杂化方式分别为
为平面形,二者中N的杂化方式分别为_______ ,二者中更易与 形成配位键的是
形成配位键的是_______ 。 熔点(>1700℃)明显高于
熔点(>1700℃)明显高于 (315℃),原因是
(315℃),原因是_______ 。
(5) -硒为六方晶胞结构,原子排列为相互平行的螺旋长链(如图1),沿着螺旋链方向的晶胞投影图如图2。
-硒为六方晶胞结构,原子排列为相互平行的螺旋长链(如图1),沿着螺旋链方向的晶胞投影图如图2。 -硒六方晶胞参数为
-硒六方晶胞参数为 、
、 、
、 (其中
(其中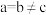 ),a轴与b轴间夹角为120°,c轴垂直于a轴与b轴,阿伏加德罗常数的值为
),a轴与b轴间夹角为120°,c轴垂直于a轴与b轴,阿伏加德罗常数的值为 。
。_______ 。晶胞中含有Se原子的数目为_______ ;则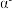 -硒晶胞的摩尔体积为
-硒晶胞的摩尔体积为______  (列出算式)。
(列出算式)。
(1)Se与O同族,电负性较大的是
(2)已知液态的二氧化硫可以发生类似水的自电离:
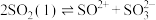 。
。 中各原子满足8电子结构,则其
中各原子满足8电子结构,则其 键和
键和 键数目之比为
键数目之比为 的空间结构为
的空间结构为(3)有一种观点认为:由于硅的价层有可以利用的空d轨道,而碳没有,因此两者化合物结构和性质存在较大差异。化合物
 和
和 的结构如图所示,
的结构如图所示, 为平面形,二者中N的杂化方式分别为
为平面形,二者中N的杂化方式分别为 形成配位键的是
形成配位键的是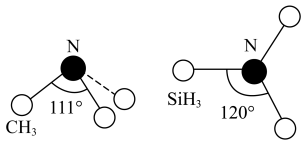
 熔点(>1700℃)明显高于
熔点(>1700℃)明显高于 (315℃),原因是
(315℃),原因是(5)
 -硒为六方晶胞结构,原子排列为相互平行的螺旋长链(如图1),沿着螺旋链方向的晶胞投影图如图2。
-硒为六方晶胞结构,原子排列为相互平行的螺旋长链(如图1),沿着螺旋链方向的晶胞投影图如图2。 -硒六方晶胞参数为
-硒六方晶胞参数为 、
、 、
、 (其中
(其中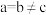 ),a轴与b轴间夹角为120°,c轴垂直于a轴与b轴,阿伏加德罗常数的值为
),a轴与b轴间夹角为120°,c轴垂直于a轴与b轴,阿伏加德罗常数的值为 。
。
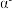 -硒晶胞的摩尔体积为
-硒晶胞的摩尔体积为 (列出算式)。
(列出算式)。
您最近一年使用:0次
7 . 研究二氧化碳的转化与减排具有重要的社会意义。用 还原
还原 的反应过程如下:
的反应过程如下:
①
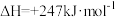
②

回答下列问题:
(1)

_______ 。
(2)同时提高 与
与 的平衡转化率和速率的措施是
的平衡转化率和速率的措施是_______ 。
(3)在密闭容器中分别充入0.1mol 与0.3mol
与0.3mol 。
。
①保持密闭容器体积为10L,只发生①②反应,经10min反应达到平衡,测定出 和
和 均为0.05mol。10min内
均为0.05mol。10min内 的平均反应速率为
的平均反应速率为____ ;该条件下,反应②的平衡常数为_____ 。
②在150℃时,改变密闭容器的体积,测得 和
和 平衡转化率随压强变化如图所示。
平衡转化率随压强变化如图所示。 平衡转化率随压强增大而减小的主要原因是
平衡转化率随压强增大而减小的主要原因是____ ; 后
后 平衡转化率随压强增大而减小缓慢甚至增大,可能的原因是
平衡转化率随压强增大而减小缓慢甚至增大,可能的原因是_______ 。 和
和 ,加入催化剂,仅发生反应①②。经实验测出两步反应过程的能量变化示意图如下:
,加入催化剂,仅发生反应①②。经实验测出两步反应过程的能量变化示意图如下: 体积分数很低,主要原因是活化能
体积分数很低,主要原因是活化能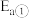
_______ 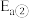 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
②随温度升高, 的体积分数变化趋势为先增后减小,其可能原因是
的体积分数变化趋势为先增后减小,其可能原因是_______ 。
 还原
还原 的反应过程如下:
的反应过程如下:①

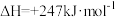
②


回答下列问题:
(1)


(2)同时提高
 与
与 的平衡转化率和速率的措施是
的平衡转化率和速率的措施是(3)在密闭容器中分别充入0.1mol
 与0.3mol
与0.3mol 。
。①保持密闭容器体积为10L,只发生①②反应,经10min反应达到平衡,测定出
 和
和 均为0.05mol。10min内
均为0.05mol。10min内 的平均反应速率为
的平均反应速率为②在150℃时,改变密闭容器的体积,测得
 和
和 平衡转化率随压强变化如图所示。
平衡转化率随压强变化如图所示。 平衡转化率随压强增大而减小的主要原因是
平衡转化率随压强增大而减小的主要原因是 后
后 平衡转化率随压强增大而减小缓慢甚至增大,可能的原因是
平衡转化率随压强增大而减小缓慢甚至增大,可能的原因是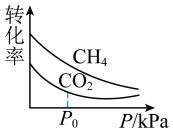
 和
和 ,加入催化剂,仅发生反应①②。经实验测出两步反应过程的能量变化示意图如下:
,加入催化剂,仅发生反应①②。经实验测出两步反应过程的能量变化示意图如下: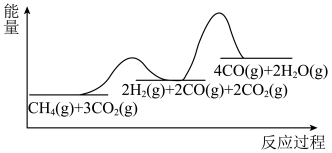
 体积分数很低,主要原因是活化能
体积分数很低,主要原因是活化能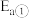
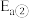 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②随温度升高,
 的体积分数变化趋势为先增后减小,其可能原因是
的体积分数变化趋势为先增后减小,其可能原因是
您最近一年使用:0次
8 . 实验室用废铁屑制取无水氯化铁并测其纯度。实验方案如下:
Ⅰ. 制备
制备
①将废铁屑加入30%NaOH溶液中,煮沸30分钟,过滤,洗涤2~3次。
②将洗涤后废铁屑加入20%盐酸,控制温度在40~50℃之间,至反应完毕,过滤。
③向滤液中逐滴加入10%双氧水,同时加入25%盐酸,充分搅拌至溶液呈棕黄色。
④将溶液转移至蒸发皿中,加热浓缩,缓慢冷却至大量晶体析出,抽滤,洗涤。
回答下列问题:
(1)用NaOH溶液洗涤废铁屑的目的是_______ 。
(2)控制温度在40~50℃的原因是_______ 。
(3)滴加10%双氧水时,滴加速率过快会产生气泡。该气体为_______ 。
Ⅱ.无水 制备
制备
已知 熔点―156℃,沸点77℃,易水解生成
熔点―156℃,沸点77℃,易水解生成 和HCl。
和HCl。
(4)按图装置进行实验。锥形瓶中生成无水 的总化学方程式为
的总化学方程式为_______ ;仪器A的作用是_______ 。
(5)称取3.250g产品试样,配制成100.00mL溶液,取20.00mL于锥形瓶中,加入足量KI溶液,经充分反应后,滴入淀粉溶液3~5滴,然后用 溶液滴定(
溶液滴定(
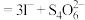 ),经三次平行实验,平均消耗
),经三次平行实验,平均消耗 溶液19.00ml。
溶液19.00ml。
①所制产品的纯度为_______ (以无水 质量分数表示,保留三位有效数字);
质量分数表示,保留三位有效数字);
②所制产品中可能含有 杂质,检验
杂质,检验 的试剂为
的试剂为_______ (填化学式)溶液;产生 的原因可能是
的原因可能是_______ 。
Ⅰ.
 制备
制备①将废铁屑加入30%NaOH溶液中,煮沸30分钟,过滤,洗涤2~3次。
②将洗涤后废铁屑加入20%盐酸,控制温度在40~50℃之间,至反应完毕,过滤。
③向滤液中逐滴加入10%双氧水,同时加入25%盐酸,充分搅拌至溶液呈棕黄色。
④将溶液转移至蒸发皿中,加热浓缩,缓慢冷却至大量晶体析出,抽滤,洗涤。
回答下列问题:
(1)用NaOH溶液洗涤废铁屑的目的是
(2)控制温度在40~50℃的原因是
(3)滴加10%双氧水时,滴加速率过快会产生气泡。该气体为
Ⅱ.无水
 制备
制备已知
 熔点―156℃,沸点77℃,易水解生成
熔点―156℃,沸点77℃,易水解生成 和HCl。
和HCl。(4)按图装置进行实验。锥形瓶中生成无水
 的总化学方程式为
的总化学方程式为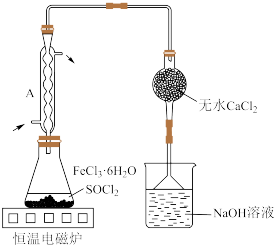
(5)称取3.250g产品试样,配制成100.00mL溶液,取20.00mL于锥形瓶中,加入足量KI溶液,经充分反应后,滴入淀粉溶液3~5滴,然后用
 溶液滴定(
溶液滴定(
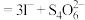 ),经三次平行实验,平均消耗
),经三次平行实验,平均消耗 溶液19.00ml。
溶液19.00ml。①所制产品的纯度为
 质量分数表示,保留三位有效数字);
质量分数表示,保留三位有效数字);②所制产品中可能含有
 杂质,检验
杂质,检验 的试剂为
的试剂为 的原因可能是
的原因可能是
您最近一年使用:0次
解题方法
9 . 化合物Ⅰ是一种具有多种药理学活性的黄烷酮类药物。由化合物A制备Ⅰ的合成路线如图:
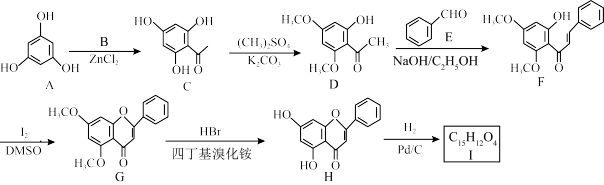
回答下列问题:
(1)A中官能团的名称为___________ 。
(2)若B为乙酸则由A生成C的化学方程式为___________ 。
(3)由C生成D的反应类型是___________ ,E的化学名称是___________ 。
(4)Ⅰ的结构简式为___________ 。
(5)芳香化合物X是C的同分异构体,同时满足如下条件的X有___________ 种,其中核磁共振氢谱峰面积比为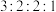 的X的结构简式是
的X的结构简式是___________ 、___________ (写出两种)。
条件:
a.苯环上只有三个取代基,且甲基不与苯环直接相连;
b.能与 溶液发生显色反应;
溶液发生显色反应;
c. 可与
可与 反应。
反应。

回答下列问题:
(1)A中官能团的名称为
(2)若B为乙酸则由A生成C的化学方程式为
(3)由C生成D的反应类型是
(4)Ⅰ的结构简式为
(5)芳香化合物X是C的同分异构体,同时满足如下条件的X有
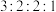 的X的结构简式是
的X的结构简式是条件:
a.苯环上只有三个取代基,且甲基不与苯环直接相连;
b.能与
 溶液发生显色反应;
溶液发生显色反应;c.
 可与
可与 反应。
反应。
您最近一年使用:0次
10 . 铁、镍、铜在医药、催化及材料等领域中都有广泛的应用。回答下列问题:
(1)在元素周期表中,某元素和铁、镍既处于同一周期又位于同一族,该元素的基态原子的价电子排布图为___________ (填轨道表示式)。
(2)硝普钠(Na2[Fe(CN)5(NO)·2H2O])可用于治疗急性心率衰竭。在硝普钠中:
①第二周期元素第一电离能从大到小的顺序为___________ 。
②不存在的化学键有___________ (填序号)。
a.离子键 b.金属键 c.配位键 d.极性共价键
(3)甘氨酸铜有顺式和反式两种同分异构体,结构如下图。
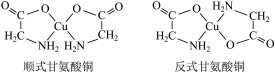
①甘氨酸铜中氮原子的杂化类型为___________ 。
②已知顺式甘氨酸铜能溶于水,反式甘氨酸铜难溶于水的原因可能是___________ 。
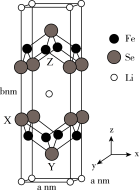
(4)Li、Fe、Se可形成新型超导材料,晶胞如图所示(Fe原子均位于面上)。晶胞棱边夹角均为90°,X的坐标为(0,1, ),Y的坐标为(
),Y的坐标为( ,
, ,
, ),设NA为阿伏加德罗常数的值。坐标为(
),设NA为阿伏加德罗常数的值。坐标为( ,1,
,1, )的是
)的是___________ 原子,Se原子X与Se原子Y之间的距离为___________ nm,该晶体的密度为___________ g·cm-3。
(1)在元素周期表中,某元素和铁、镍既处于同一周期又位于同一族,该元素的基态原子的价电子排布图为
(2)硝普钠(Na2[Fe(CN)5(NO)·2H2O])可用于治疗急性心率衰竭。在硝普钠中:
①第二周期元素第一电离能从大到小的顺序为
②不存在的化学键有
a.离子键 b.金属键 c.配位键 d.极性共价键
(3)甘氨酸铜有顺式和反式两种同分异构体,结构如下图。

①甘氨酸铜中氮原子的杂化类型为
②已知顺式甘氨酸铜能溶于水,反式甘氨酸铜难溶于水的原因可能是
(4)Li、Fe、Se可形成新型超导材料,晶胞如图所示(Fe原子均位于面上)。晶胞棱边夹角均为90°,X的坐标为(0,1,
 ),Y的坐标为(
),Y的坐标为( ,
, ,
, ),设NA为阿伏加德罗常数的值。坐标为(
),设NA为阿伏加德罗常数的值。坐标为( ,1,
,1, )的是
)的是
您最近一年使用:0次



