名校
解题方法
1 . 工业上常通过高温分解FeSO4的方法制备Fe2O3,其化学方程式为:2FeSO4 Fe2O3+SO2↑+SO3↑。为检验FeSO4高温分解的产物,进行如下实验:
Fe2O3+SO2↑+SO3↑。为检验FeSO4高温分解的产物,进行如下实验:
①取少量FeSO4高温分解得到的固体,加一定量稀盐酸溶解,向该溶液中加入适量的KSCN溶液,观察溶液颜色的变化以检验Fe3+是否存在。
②将FeSO4高温分解产生的气体通入如图所示的装置中,以检验产生的气体中是否含有SO2、SO3。
请回答下列问题:

(1)写出KSCN溶液与Fe3+反应的离子方程式:____ 。
(2)操作②中观察到的现象和结论是____ ;_____ 。
(3)操作②中最后要将通过品红溶液的气体通入NaOH溶液中的原因是___ ,有关反应的离子方程式____ 。
 Fe2O3+SO2↑+SO3↑。为检验FeSO4高温分解的产物,进行如下实验:
Fe2O3+SO2↑+SO3↑。为检验FeSO4高温分解的产物,进行如下实验:①取少量FeSO4高温分解得到的固体,加一定量稀盐酸溶解,向该溶液中加入适量的KSCN溶液,观察溶液颜色的变化以检验Fe3+是否存在。
②将FeSO4高温分解产生的气体通入如图所示的装置中,以检验产生的气体中是否含有SO2、SO3。
请回答下列问题:

(1)写出KSCN溶液与Fe3+反应的离子方程式:
(2)操作②中观察到的现象和结论是
(3)操作②中最后要将通过品红溶液的气体通入NaOH溶液中的原因是
您最近一年使用:0次
2 . 实验室中用如图所示装置制取干燥的氨气。
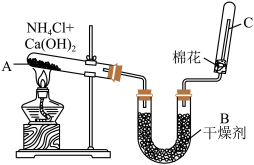
(1)写出A处发生反应的化学方程式:__________________________________________ 。
(2)能否用排水法收集氨气?为什么?________________________________________________________________________ 。
(3)检验试管C中氨气是否集满,除用湿润的红色石蕊试纸外,还可采用哪种简易方法(简述操作、现象和结论)?________________________________________________________________________ 。

(1)写出A处发生反应的化学方程式:
(2)能否用排水法收集氨气?为什么?
(3)检验试管C中氨气是否集满,除用湿润的红色石蕊试纸外,还可采用哪种简易方法(简述操作、现象和结论)?
您最近一年使用:0次
名校
3 . 甲同学采用如图Ⅰ所示装置验证铜与稀硝酸的反应,并用排水法收集NO气体。
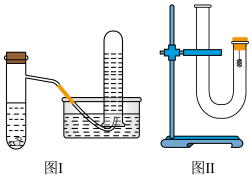
(1)反应过程中的实验现象是__________________________________________________ 。
(2)乙同学认为虽然收集到的气体为一氧化氮,但并不能说明反应中一定生成一氧化氮。你认为他的理由是______________________________________________________________ 。
(3)丙同学采用如图Ⅱ所示装置进行实验,证明了铜与稀硝酸反应生成一氧化氮。该同学的步骤如下表所示,请回答实验中的有关问题。
(4)从环境保护的角度看,丙同学的实验存在__________ 缺陷?你认为应如何改进__________ ?

(1)反应过程中的实验现象是
(2)乙同学认为虽然收集到的气体为一氧化氮,但并不能说明反应中一定生成一氧化氮。你认为他的理由是
(3)丙同学采用如图Ⅱ所示装置进行实验,证明了铜与稀硝酸反应生成一氧化氮。该同学的步骤如下表所示,请回答实验中的有关问题。
| 实验步骤 | 问题 |
| ①从U形管左端加入稀硝酸,直至充满U形管右端 | |
| ②用附有铜丝的胶塞塞住U形管右端,观察现象 | 实验现象是 |
| ③待反应停止后打开胶塞,观察实验现象 | 打开胶塞后的实验现象是 |
(4)从环境保护的角度看,丙同学的实验存在
您最近一年使用:0次
名校
4 . 某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以确保化学实验的绿色化。

(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c。其目的是_____________________________________________________________________ 。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL的浓硝酸。反应一段时间后,再由a向c中加2 mL蒸馏水,c中的实验现象有什么变化___________ 。
(3)如表所示是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是__________ ,理由是________________________________________________________________________ 。

(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c。其目的是
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL的浓硝酸。反应一段时间后,再由a向c中加2 mL蒸馏水,c中的实验现象有什么变化
| 方案 | 甲 | 乙 | 丙 |
| 反应物 | Cu、浓HNO3 | Cu、稀HNO3 | Cu、O2、稀HNO3 |
您最近一年使用:0次
名校
5 . 如图所示是制取SO2并验证SO2某些性质的装置图。
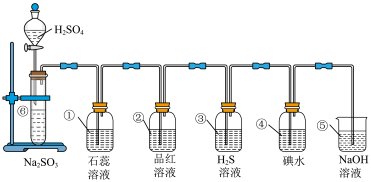
试回答:
(1)⑥中发生反应的化学方程式为___ 。
(2)①中的实验现象为___ ,此实验证明SO2是___ 氧化物。
(3)②中的品红溶液___ ,证明SO2有___ 。
(4)③中的H2S溶液____ ,证明SO2有___ 。
(5)④中的碘水___ ,证明SO2有____ 。
(6)⑤中NaOH溶液的作用是___ ,有关反应的化学方程式为____ 。

试回答:
(1)⑥中发生反应的化学方程式为
(2)①中的实验现象为
(3)②中的品红溶液
(4)③中的H2S溶液
(5)④中的碘水
(6)⑤中NaOH溶液的作用是
您最近一年使用:0次
13-14高二·全国·课时练习
名校
6 . 晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅;
②粗硅与干燥HCl气体反应制得SiHCl3:Si+3HCl SiHCl3+H2;
SiHCl3+H2;
③SiHCl3与过量H2在1 000~1 100 ℃反应制得纯硅已知SiHCl3能与H2O强烈反应,在空气中易自燃。
请回答下列问题:
(1)第①步制备粗硅的化学方程式为_____________________________________________ 。
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3(沸点33.0 ℃)中含有少量SiCl4(沸点57.6 ℃)和HCl(沸点-84.7 ℃),提纯SiHCl3采用的方法为___________________________ 。
(3)用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):
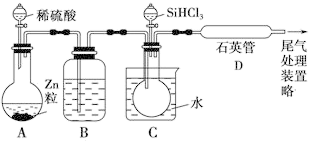
①装置B中的试剂是________ 。装置C中的烧瓶需要加热,其目的是________________________________________________________________ 。
②反应一段时间后,装置D中观察到的现象是________ ,装置D不能采用普通玻璃管的原因是____________ ,装置D中发生反应的化学方程式为_____________________________________________________________ 。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及___________________________________________________________ 。
①高温下用碳还原二氧化硅制得粗硅;
②粗硅与干燥HCl气体反应制得SiHCl3:Si+3HCl
 SiHCl3+H2;
SiHCl3+H2;③SiHCl3与过量H2在1 000~1 100 ℃反应制得纯硅已知SiHCl3能与H2O强烈反应,在空气中易自燃。
请回答下列问题:
(1)第①步制备粗硅的化学方程式为
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3(沸点33.0 ℃)中含有少量SiCl4(沸点57.6 ℃)和HCl(沸点-84.7 ℃),提纯SiHCl3采用的方法为
(3)用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):

①装置B中的试剂是
②反应一段时间后,装置D中观察到的现象是
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及
您最近一年使用:0次



