名校
1 . 苯巴比妥(F)是我国化学家近期合成的一种能抗击新冠病毒的新型药物,其合成路线如图所示:
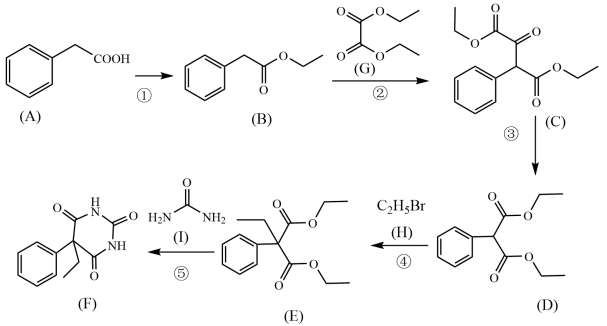
(1)有机物A的名称为___________ ;有机物A、J(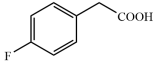 )、K(
)、K( )三种物质中酸性最强的是
)三种物质中酸性最强的是___________ (填“A”“J”或“K”)。
(2)有机物C的含氧官能团名称为___________ 。
(3)下列说法正确的是___________。
(4)写出D与足量的NaOH溶液反应的化学方程式:___________ 。
(5)化合物N与B是同分异构体,则符合以下条件的N有___________ 种。
①能使 溶液显色;②能发生银镜反应;③苯环上的取代基数目为2个。
溶液显色;②能发生银镜反应;③苯环上的取代基数目为2个。
其中不含有手性碳原子且核磁共振氢谱只有5组的同分异构体为___________ 。
(6)以1,2-二溴乙烷(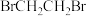 )、乙醇、尿素(
)、乙醇、尿素(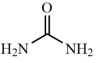 )为原料(无机试剂任选)设计制备
)为原料(无机试剂任选)设计制备 的合成路线:
的合成路线:___________ 。

(1)有机物A的名称为
 )、K(
)、K( )三种物质中酸性最强的是
)三种物质中酸性最强的是(2)有机物C的含氧官能团名称为
(3)下列说法正确的是___________。
| A.有机物D易溶于水 | B.有机物E存在顺反异构体 |
C.有机物F的氮原子杂化类型为 | D.有机物G的名称为二乙酸乙二酯 |
(5)化合物N与B是同分异构体,则符合以下条件的N有
①能使
 溶液显色;②能发生银镜反应;③苯环上的取代基数目为2个。
溶液显色;②能发生银镜反应;③苯环上的取代基数目为2个。其中不含有手性碳原子且核磁共振氢谱只有5组的同分异构体为
(6)以1,2-二溴乙烷(
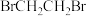 )、乙醇、尿素(
)、乙醇、尿素( )为原料(无机试剂任选)设计制备
)为原料(无机试剂任选)设计制备 的合成路线:
的合成路线:
您最近一年使用:0次
2023-03-13更新
|
268次组卷
|
4卷引用:湖南省湘西州吉首市2024届高三上学期第二届中小学生教师解题大赛化学试题
2 . 甘氨酸亚铁晶体是一种新型的固体整合补铁剂。其实验室合成路线为:铁片 FeSO4
FeSO4 FeCO3
FeCO3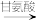 甘氨酸亚铁晶体粗品
甘氨酸亚铁晶体粗品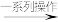 甘氨酸亚铁晶体纯品。
甘氨酸亚铁晶体纯品。
已知:相关物质的信息如表所示:
(一)FeCO3固体的制备
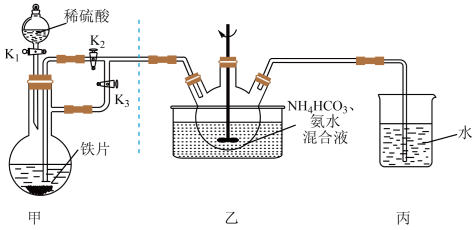
(1)实验开始时应先开K1和________ ,关________ (填“K2”或“K3”)一段时间后,改变开关状态,生成FeCO3。
(2)三颈瓶中生成FeCO3的离子方程式为________ 。
(二)甘氨酸亚铁的制备
(3)用如图装置制备甘氨酸亚铁。反应开始时,先通过滴液口滴入适量的NaOH溶液调节pH为5左右,pH过高或过低都会使产率下降,原因是_________ 。
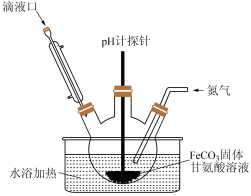
(4)当FeCO3固体完全溶解后,再通过滴液口加入乙醇,其作用是________ 。
(5)反应结束后,过滤出产品粗品,依次用________ 、_______ (填序号)洗涤,再经过一系列操作得纯品。
a.热水 b.冰水 c.乙醇
(三)甘氨酸亚铁晶体结构的分析
步骤1:准确称取甘氨酸亚铁晶体纯品0.4800g于锥形瓶中,加3mol/LH2SO4溶液15mL将样品溶解完全后,加入指示剂,立即用0.1000mol/L(NH4)2Ce(SO4)3,标准液滴定至终点,用去标准液20.20mL(反应为Ce4++Fe2+=Ce3++Fe3+)。
步骤2:不加产品,重复步骤1操作,滴定至终点,用去标准液0.20mL。
回答下列问题:
(6)甘氨酸亚铁晶体中Fe的质量分数为_________  (保留小数点后一位)。
(保留小数点后一位)。
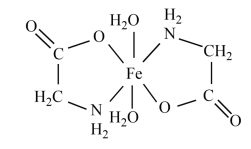
(7)进一步分析表明:甘氨酸亚铁晶体中,阴阳离子只有H2NCH2COO-和Fe2+且存在五元整合环,甘氨酸亚铁晶体的结构简式如图所示,则Fe2+的配位数为________ 。
 FeSO4
FeSO4 FeCO3
FeCO3 甘氨酸亚铁晶体粗品
甘氨酸亚铁晶体粗品 甘氨酸亚铁晶体纯品。
甘氨酸亚铁晶体纯品。已知:相关物质的信息如表所示:
| 物质 | 化学式 | 摩尔质量 | 性质 |
| 甘氨酸 | H2NCH2COOH | 75g/mol | 两性物质,易溶于水,微溶于乙醇 |
| 甘氨酸亚铁晶体 | 易溶于水,溶解度随温度升高而增大;难溶于乙醇,在潮湿的空气中易被氯化 |

(1)实验开始时应先开K1和
(2)三颈瓶中生成FeCO3的离子方程式为
(二)甘氨酸亚铁的制备
(3)用如图装置制备甘氨酸亚铁。反应开始时,先通过滴液口滴入适量的NaOH溶液调节pH为5左右,pH过高或过低都会使产率下降,原因是

(4)当FeCO3固体完全溶解后,再通过滴液口加入乙醇,其作用是
(5)反应结束后,过滤出产品粗品,依次用
a.热水 b.冰水 c.乙醇
(三)甘氨酸亚铁晶体结构的分析
步骤1:准确称取甘氨酸亚铁晶体纯品0.4800g于锥形瓶中,加3mol/LH2SO4溶液15mL将样品溶解完全后,加入指示剂,立即用0.1000mol/L(NH4)2Ce(SO4)3,标准液滴定至终点,用去标准液20.20mL(反应为Ce4++Fe2+=Ce3++Fe3+)。
步骤2:不加产品,重复步骤1操作,滴定至终点,用去标准液0.20mL。
回答下列问题:
(6)甘氨酸亚铁晶体中Fe的质量分数为
 (保留小数点后一位)。
(保留小数点后一位)。(7)进一步分析表明:甘氨酸亚铁晶体中,阴阳离子只有H2NCH2COO-和Fe2+且存在五元整合环,甘氨酸亚铁晶体的结构简式如图所示,则Fe2+的配位数为

您最近一年使用:0次
2023-10-04更新
|
108次组卷
|
2卷引用:湖南省湘西州吉首市2024届高三上学期第二届中小学生教师解题大赛化学试题
3 . 我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染,这一材料是由我国某公司最新研发成功的新材料。PETG的结构简式为:

已知:I.


II.RCOOR1+R2OH→RCOOR2+R1OH
这种材料可采用下列合成路线:

试回答下列问题:
(1)反应②、⑥中加入的试剂X是___________ ;
(2)⑤的反应类型是___________ ;
(3)写出结构简式:B:___________ ,I:___________ ;
(4)写出化学方程式:反应③:___________ ;反应⑥:___________ 。

已知:I.



II.RCOOR1+R2OH→RCOOR2+R1OH
这种材料可采用下列合成路线:

试回答下列问题:
(1)反应②、⑥中加入的试剂X是
(2)⑤的反应类型是
(3)写出结构简式:B:
(4)写出化学方程式:反应③:
您最近一年使用:0次
4 . 某化工厂以甲烷为原料合成甲醇的反应为:
CH4(g)+H2O(g)→CO(g)+3H2(g) ①(反应中CH4转化率:1)
CO(g)+2H2(g)→CH3OH(g) ②(反应中CO转化率: )
)
合成工艺如下(虚线框内为改进后的工艺中新增流程):

请回答下列问题(所有气体体积均折算为标准状况):
(1)原工艺中,当充入反应器①的甲烷和水蒸气的体积分别为672m3和1750m3时,最终反应剩余物中n(CO)=___________ ,n(H2)=___________ 。
(2)为充分利用反应剩余物,该厂在原工艺的基础上,将下列反应运用于生产甲醇原料气:2CH4(g)+O2(g)→2CO(g)+4H2(g) ③(反应中CH4转化率:1),若新工艺中充入反应器①的甲烷和水蒸气的体积分别为a、3a,反应剩余物中:V(H2):V(N2):V(CO)=3:1:1。计算:
①充入反应器③的甲烷的体积为___________ 。
②若富氧空气中除O2、N2外,其他成分忽略不计,则充入反应器③中的富氧空气的体积为___________ ;应选择氧气体积分数为___________ 的富氧空气。
CH4(g)+H2O(g)→CO(g)+3H2(g) ①(反应中CH4转化率:1)
CO(g)+2H2(g)→CH3OH(g) ②(反应中CO转化率:
 )
)合成工艺如下(虚线框内为改进后的工艺中新增流程):

请回答下列问题(所有气体体积均折算为标准状况):
(1)原工艺中,当充入反应器①的甲烷和水蒸气的体积分别为672m3和1750m3时,最终反应剩余物中n(CO)=
(2)为充分利用反应剩余物,该厂在原工艺的基础上,将下列反应运用于生产甲醇原料气:2CH4(g)+O2(g)→2CO(g)+4H2(g) ③(反应中CH4转化率:1),若新工艺中充入反应器①的甲烷和水蒸气的体积分别为a、3a,反应剩余物中:V(H2):V(N2):V(CO)=3:1:1。计算:
①充入反应器③的甲烷的体积为
②若富氧空气中除O2、N2外,其他成分忽略不计,则充入反应器③中的富氧空气的体积为
您最近一年使用:0次



