1 . 酮基布洛芬片具有镇痛、消炎及解热作用,副作用小,毒性低。其合成路线如图所示:
(1)①写出A的名称______________ 。
②写出1个A分子中含有σ键的数目______________ 。
(2)写出B→C反应的化学方程式______________ 。
(3)判断D→E的反应类型______________ 。
(4)写出E→F反应的化学方程式______________ 。
(5)以乙烯和碳酸二甲酯( )为原料(无机试剂任选),设计制备2-甲基丙酸的一种合成路线
)为原料(无机试剂任选),设计制备2-甲基丙酸的一种合成路线______________ 。

(1)①写出A的名称
②写出1个A分子中含有σ键的数目
(2)写出B→C反应的化学方程式
(3)判断D→E的反应类型
(4)写出E→F反应的化学方程式
(5)以乙烯和碳酸二甲酯(
 )为原料(无机试剂任选),设计制备2-甲基丙酸的一种合成路线
)为原料(无机试剂任选),设计制备2-甲基丙酸的一种合成路线
您最近一年使用:0次
2023-05-11更新
|
168次组卷
|
2卷引用:重庆市2022-2023学年高二下学期化学竞赛试题
2 . H是某种药物合成的中间体,其合成路线如下:
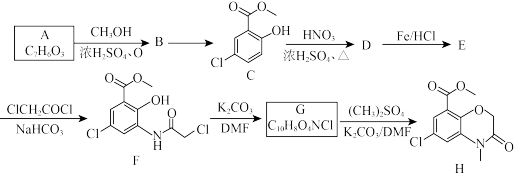
(1)写出A中所含官能团的名称_______ ,B→C反应的试剂和条件是_______ ?
(2)写出有机物D、G的结构简式_______ 、_______ 。
(3)写出E→F反应的化学方程式_______ 。
(4)根据上述路线,设计一条以苯酚和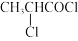 为原料合成
为原料合成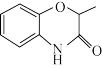 的路线(其它试剂任选)
的路线(其它试剂任选)_______ 。

(1)写出A中所含官能团的名称
(2)写出有机物D、G的结构简式
(3)写出E→F反应的化学方程式
(4)根据上述路线,设计一条以苯酚和
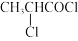 为原料合成
为原料合成 的路线(其它试剂任选)
的路线(其它试剂任选)
您最近一年使用:0次
解题方法
3 . 莫西赛利(化合物 )是一种治疗脑血管疾病的药物,可改善脑梗塞或脑出血后遗症等症状。以下为其合成路线之一:
)是一种治疗脑血管疾病的药物,可改善脑梗塞或脑出血后遗症等症状。以下为其合成路线之一: 的名称
的名称___________ ;写出 分子中最多处于同一个平面上的碳原子数
分子中最多处于同一个平面上的碳原子数___________ 。
(2)下列说法错误的是___________(填编号)。
(3)写出 的结构简式
的结构简式___________ 。
(4)写出 转化为
转化为 的化学方程式
的化学方程式___________ 。
(5)根据上述路线,设计由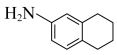 合成
合成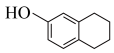 的合成路线(其他试剂任选)
的合成路线(其他试剂任选)___________ 。
 )是一种治疗脑血管疾病的药物,可改善脑梗塞或脑出血后遗症等症状。以下为其合成路线之一:
)是一种治疗脑血管疾病的药物,可改善脑梗塞或脑出血后遗症等症状。以下为其合成路线之一: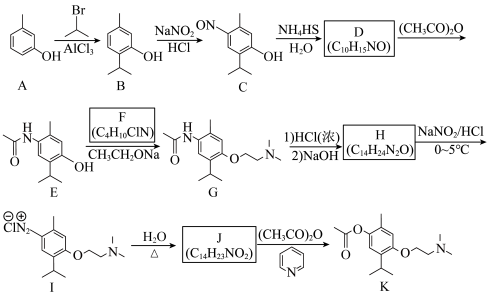
 的名称
的名称 分子中最多处于同一个平面上的碳原子数
分子中最多处于同一个平面上的碳原子数(2)下列说法错误的是___________(填编号)。
A.在 的反应中, 的反应中, 作还原剂 作还原剂 |
B. 和 和 的反应类型均为取代反应 的反应类型均为取代反应 |
C.化合物 能与 能与 溶液发生显色反应 溶液发生显色反应 |
D. 与 与 溶液反应最多消耗 溶液反应最多消耗 |
(3)写出
 的结构简式
的结构简式(4)写出
 转化为
转化为 的化学方程式
的化学方程式(5)根据上述路线,设计由
 合成
合成 的合成路线(其他试剂任选)
的合成路线(其他试剂任选)
您最近一年使用:0次
4 . A是一种常见的烃,它的产量可以衡量一个国家的石油化工发展水平,E常用作还原剂、媒染剂、除锈剂等,是一种常见的二元弱酸。以A为原料合成E的路线如下:

(1)判断A分子中官能团的名称______ 。
(2)写出B→C的反应类型______ 。
(3)写出C→D的反应方程式______ 。
(4)E可使酸性高锰酸钾溶液褪色, 还原为
还原为 ,写出该反应中E与高锰酸钾的物质的量之比
,写出该反应中E与高锰酸钾的物质的量之比______ 。
(5)C可与E反应生成一种六元环酯,请写出该六元环酯的结构简式______ 。

(1)判断A分子中官能团的名称
(2)写出B→C的反应类型
(3)写出C→D的反应方程式
(4)E可使酸性高锰酸钾溶液褪色,
 还原为
还原为 ,写出该反应中E与高锰酸钾的物质的量之比
,写出该反应中E与高锰酸钾的物质的量之比(5)C可与E反应生成一种六元环酯,请写出该六元环酯的结构简式
您最近一年使用:0次
解题方法
5 . 尼龙(主要成分为聚酰胺)为重要的工业产品,下面是尼龙-66的合成路线:

(1)写出A、B、C的结构简式______________ 。
(2)写出A中所含官能团的名称______________ 。
(3)已知在生成F的同时,产生两种有刺激性气味的气体,写出生成F的化学方程式______________ 。
(4)聚酰胺分子链间缠结使尼龙纤维有很高的强度,指出聚酰胺分子链间的主要作用力______________ 。
(5)指出与E具有相同官能团的同分异构体的数目________ (不考虑立体异构),其中一种同分异构体G的核磁共振碳谱有三组峰,写出G的结构简式______________ 。

(1)写出A、B、C的结构简式
(2)写出A中所含官能团的名称
(3)已知在生成F的同时,产生两种有刺激性气味的气体,写出生成F的化学方程式
(4)聚酰胺分子链间缠结使尼龙纤维有很高的强度,指出聚酰胺分子链间的主要作用力
(5)指出与E具有相同官能团的同分异构体的数目
您最近一年使用:0次
解题方法
6 . 聚四氟乙烯(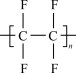 )是家用不粘锅内侧涂层的主要成分,其中一种合成路线如下。下列说法正确的是
)是家用不粘锅内侧涂层的主要成分,其中一种合成路线如下。下列说法正确的是

 )是家用不粘锅内侧涂层的主要成分,其中一种合成路线如下。下列说法正确的是
)是家用不粘锅内侧涂层的主要成分,其中一种合成路线如下。下列说法正确的是
| A.二氟一氯甲烷分子中所有原子共平面 | B.乙炔与 发生加成反应生成四氟乙烯 发生加成反应生成四氟乙烯 |
| C.反应①为取代反应,反应②为加聚反应 | D.聚四氟乙烯不能使酸性 溶液褪色 溶液褪色 |
您最近一年使用:0次
7 . 亚硫酰氯( ,熔点
,熔点 ,沸点
,沸点 ,易水解生成
,易水解生成 和
和 )是一种重要的化学试剂,广泛用于有机合成。制备亚硫酰氯的两种方法:
)是一种重要的化学试剂,广泛用于有机合成。制备亚硫酰氯的两种方法:
方法1:以五氯化磷和二氧化硫为原料,发生反应:
方法2:以三氧化硫和二氯化硫为原料。
(1)方法1反应的过程中是否存在电子转移_______ ?
(2)写出方法2的化学方程式_______ 。
(3)某科研小组测定亚硫酰氯产品的纯度。步骤如下:
步骤一、用分析天平准确称取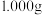 样品,小心地将样品溶于
样品,小心地将样品溶于 的氢氧化钠溶液中,充分反应后,配成
的氢氧化钠溶液中,充分反应后,配成 试样溶液。
试样溶液。
步骤二、用移液管吸取 试样溶液于
试样溶液于 碘量瓶中,加入两滴对硝基苯酚指示剂,滴加
碘量瓶中,加入两滴对硝基苯酚指示剂,滴加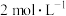 盐酸至黄色刚好消失,加入
盐酸至黄色刚好消失,加入 碘标准溶液,避光放置
碘标准溶液,避光放置 。
。
步骤三、用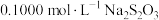 标准溶液返滴定过量的
标准溶液返滴定过量的 ,近终点时加入淀粉溶液,继续滴定至终点,消耗标准溶液
,近终点时加入淀粉溶液,继续滴定至终点,消耗标准溶液 。
。
①指出步骤一中“配成 试样溶液”所必需的定量玻璃仪器的名称
试样溶液”所必需的定量玻璃仪器的名称_______ 。
②指出步骤二中滴加盐酸的目的_______ 。
③叙述步骤三中滴定终点的现象_______ 。
④计算样品的纯度(用含有V的代数式表示)_______ 。
 ,熔点
,熔点 ,沸点
,沸点 ,易水解生成
,易水解生成 和
和 )是一种重要的化学试剂,广泛用于有机合成。制备亚硫酰氯的两种方法:
)是一种重要的化学试剂,广泛用于有机合成。制备亚硫酰氯的两种方法:方法1:以五氯化磷和二氧化硫为原料,发生反应:

方法2:以三氧化硫和二氯化硫为原料。
(1)方法1反应的过程中是否存在电子转移
(2)写出方法2的化学方程式
(3)某科研小组测定亚硫酰氯产品的纯度。步骤如下:
步骤一、用分析天平准确称取
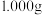 样品,小心地将样品溶于
样品,小心地将样品溶于 的氢氧化钠溶液中,充分反应后,配成
的氢氧化钠溶液中,充分反应后,配成 试样溶液。
试样溶液。步骤二、用移液管吸取
 试样溶液于
试样溶液于 碘量瓶中,加入两滴对硝基苯酚指示剂,滴加
碘量瓶中,加入两滴对硝基苯酚指示剂,滴加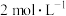 盐酸至黄色刚好消失,加入
盐酸至黄色刚好消失,加入 碘标准溶液,避光放置
碘标准溶液,避光放置 。
。步骤三、用
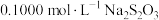 标准溶液返滴定过量的
标准溶液返滴定过量的 ,近终点时加入淀粉溶液,继续滴定至终点,消耗标准溶液
,近终点时加入淀粉溶液,继续滴定至终点,消耗标准溶液 。
。①指出步骤一中“配成
 试样溶液”所必需的定量玻璃仪器的名称
试样溶液”所必需的定量玻璃仪器的名称②指出步骤二中滴加盐酸的目的
③叙述步骤三中滴定终点的现象
④计算样品的纯度(用含有V的代数式表示)
您最近一年使用:0次
名校
8 .  是制造电信器材软磁铁氧体,合成二氧化锰和制造其他锰盐的原料。用
是制造电信器材软磁铁氧体,合成二氧化锰和制造其他锰盐的原料。用 粉与
粉与 矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备
矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备 的工艺如下图所示:
的工艺如下图所示:
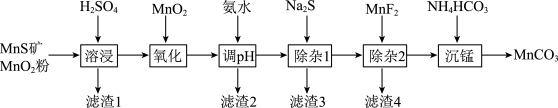
相关金属离子 形成氢氧化物沉淀的pH范围如下:
形成氢氧化物沉淀的pH范围如下:
(1)已知“滤渣1”含有S和 ,写出“溶浸”中生成S的化学方程式
,写出“溶浸”中生成S的化学方程式______ 。
(2)加入 氧化的是哪种离子
氧化的是哪种离子______ ?
(3)“调pH”控制的pH为4.7~6.0之间,写出“滤渣2”的化学式______ 。
(4)“除杂1”的目的是加入 除去
除去 和
和 ,分析该步骤不能通过调节pH除杂的原因
,分析该步骤不能通过调节pH除杂的原因______ 。
(5)写出“沉锰”的离子方程式______ 。
(6) 在空气中加热易转化为不同价态的锰的氧化物,某小组称取一定质量的
在空气中加热易转化为不同价态的锰的氧化物,某小组称取一定质量的 固体在空气中加热,测得固体质量的残留率随着温度的变化如图所示。
固体在空气中加热,测得固体质量的残留率随着温度的变化如图所示。

①写出从开始加热到A点过程中发生反应的化学方程式______ 。
②若D点对应的固体残留率为64.52%,写出D点残留固体的成分及物质的量之比______ 。
 是制造电信器材软磁铁氧体,合成二氧化锰和制造其他锰盐的原料。用
是制造电信器材软磁铁氧体,合成二氧化锰和制造其他锰盐的原料。用 粉与
粉与 矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备
矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备 的工艺如下图所示:
的工艺如下图所示:
相关金属离子
 形成氢氧化物沉淀的pH范围如下:
形成氢氧化物沉淀的pH范围如下:| 金属离子 |  |  |  |  |  |  |  |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)已知“滤渣1”含有S和
 ,写出“溶浸”中生成S的化学方程式
,写出“溶浸”中生成S的化学方程式(2)加入
 氧化的是哪种离子
氧化的是哪种离子(3)“调pH”控制的pH为4.7~6.0之间,写出“滤渣2”的化学式
(4)“除杂1”的目的是加入
 除去
除去 和
和 ,分析该步骤不能通过调节pH除杂的原因
,分析该步骤不能通过调节pH除杂的原因(5)写出“沉锰”的离子方程式
(6)
 在空气中加热易转化为不同价态的锰的氧化物,某小组称取一定质量的
在空气中加热易转化为不同价态的锰的氧化物,某小组称取一定质量的 固体在空气中加热,测得固体质量的残留率随着温度的变化如图所示。
固体在空气中加热,测得固体质量的残留率随着温度的变化如图所示。
①写出从开始加热到A点过程中发生反应的化学方程式
②若D点对应的固体残留率为64.52%,写出D点残留固体的成分及物质的量之比
您最近一年使用:0次



