1 . 按要求填空
(1)0.5mol SO2共约含有____ 个原子,它与___ 克SO3所含硫原子数相等。
(2)将质量比为14 :15的N2和NO混合,则N2和NO的物质的量之比为_____ ,混合气体中氮原子和氧原子的个数比为________ 。
(3)同温同压下,质量相同的五种气体:①CO2 ②H2 ③O2 ④CH4 ,所占的体积由大到小的顺序是(填序号)__________ 。
(4)标准状况下,有N2和CO2混合气体质量为18g,体积为11.2L,则此混合气体中N2的物质的量为_____ mol; CO2的质量是____ 克。
(1)0.5mol SO2共约含有
(2)将质量比为14 :15的N2和NO混合,则N2和NO的物质的量之比为
(3)同温同压下,质量相同的五种气体:①CO2 ②H2 ③O2 ④CH4 ,所占的体积由大到小的顺序是(填序号)
(4)标准状况下,有N2和CO2混合气体质量为18g,体积为11.2L,则此混合气体中N2的物质的量为
您最近一年使用:0次
2 . 某纯碱样品中含有少量氯化钠。江津中学化学兴趣小组为测定样品中碳酸钠的质量分数,现称取该样品 ,加入到盛有
,加入到盛有 稀盐酸的烧杯中,恰好完全反应,最后称得烧杯中溶液的质量为
稀盐酸的烧杯中,恰好完全反应,最后称得烧杯中溶液的质量为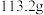 。计算:
。计算:
(1)产生的二氧化碳质量是多少_____ ?
(2)纯碱样品中碳酸钠的质量分数_____ ;(结果精确到 )
)
(3)反应后所得溶液的溶质质量分数_____ 。(结果精确到 )
)
 ,加入到盛有
,加入到盛有 稀盐酸的烧杯中,恰好完全反应,最后称得烧杯中溶液的质量为
稀盐酸的烧杯中,恰好完全反应,最后称得烧杯中溶液的质量为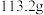 。计算:
。计算:(1)产生的二氧化碳质量是多少
(2)纯碱样品中碳酸钠的质量分数
 )
)(3)反应后所得溶液的溶质质量分数
 )
)
您最近一年使用:0次
3 . 碳酸氢铵,又称碳铵,是一种碳酸盐,含氮17.7%左右。可作为氮肥,由于其可分解为NH3、CO2和H2O三种气体而消失,故又称气肥。

在一定条件下,mgNH4HCO3完全分解生成NH3、CO2、H2O(g),按要求填空。
(1)若所得混合气体对H2的相对密度为d,则混合气体的物质的量为:____ 。NH4HCO3的摩尔质量为____ (用含m、d的代数式表示)。
(2)若所得混合气体的密度折合成标准状况为ρg·L-1,则混合气体的平均摩尔质量为____ (用含ρ的代数式表示)。
(3)若在该条件下,所得NH3、CO2、H2O(g)的体积分数分别为a%、b%、c%,则混合气体的平均相对分子质量为____ (用含a、b、c的代数式表示)。

在一定条件下,mgNH4HCO3完全分解生成NH3、CO2、H2O(g),按要求填空。
(1)若所得混合气体对H2的相对密度为d,则混合气体的物质的量为:
(2)若所得混合气体的密度折合成标准状况为ρg·L-1,则混合气体的平均摩尔质量为
(3)若在该条件下,所得NH3、CO2、H2O(g)的体积分数分别为a%、b%、c%,则混合气体的平均相对分子质量为
您最近一年使用:0次
4 . 物质的量是高中化学常用的物理量,请完成以下有关计算。
(1)含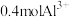 的
的 中所含的
中所含的 的物质的量是
的物质的量是_______ 。
(2)_______ 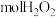 所含原子数与
所含原子数与 所含原子数相等。
所含原子数相等。
(3)某硫酸钠溶液中含有 个
个 ,则溶液中
,则溶液中 的物质的量是
的物质的量是_______ 。
(4)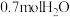 的质量为
的质量为_______ 。
(5)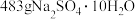 中所含的
中所含的 的物质的量是
的物质的量是_______ mol,所含 分子的数目是
分子的数目是_______ 个。
(1)含
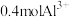 的
的 中所含的
中所含的 的物质的量是
的物质的量是(2)
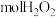 所含原子数与
所含原子数与 所含原子数相等。
所含原子数相等。(3)某硫酸钠溶液中含有
 个
个 ,则溶液中
,则溶液中 的物质的量是
的物质的量是(4)
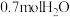 的质量为
的质量为(5)
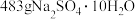 中所含的
中所含的 的物质的量是
的物质的量是 分子的数目是
分子的数目是
您最近一年使用:0次
解题方法
5 . 碱式碳酸铜[Cu2(OH)2CO3]用作农药防治小麦黑穗病。实验室用加热法测定某农药中碱式碳酸铜的质量分数(假设杂质受热不参与反应)。充分加热100 g样品,得到固体84.5 g。已知反应的化学方程式为:Cu2(OH)2CO3 2CuO+H2O+CO2↑,Cu2(OH)2CO3的相对分子质量为222。
2CuO+H2O+CO2↑,Cu2(OH)2CO3的相对分子质量为222。
试计算:(1)Cu2(OH)2CO3中铜元素与氧元素的质量比___________ 。(最简整数比)
(2)质量分数最大的元素是___________ 。(填元素名称)
(3)样品中碱式碳酸铜的质量分数是多少__________ ?(保留1位小数)
 2CuO+H2O+CO2↑,Cu2(OH)2CO3的相对分子质量为222。
2CuO+H2O+CO2↑,Cu2(OH)2CO3的相对分子质量为222。试计算:(1)Cu2(OH)2CO3中铜元素与氧元素的质量比
(2)质量分数最大的元素是
(3)样品中碱式碳酸铜的质量分数是多少
您最近一年使用:0次
6 . 现有 ,请通过计算填空:
,请通过计算填空:
(1)该气体的摩尔质量是多少?___________ 它的密度是相同条件下氢气密度的___________ 倍
(2)该气体物质的量为___________ ,所含H原子数目为___________ 。
(3)该气体在标准状况下的体积为___________ 。
(4)若将该气体溶于水配成V L溶液,所得溶液溶质的物质的量浓度为___________ 。
 ,请通过计算填空:
,请通过计算填空:(1)该气体的摩尔质量是多少?
(2)该气体物质的量为
(3)该气体在标准状况下的体积为
(4)若将该气体溶于水配成V L溶液,所得溶液溶质的物质的量浓度为
您最近一年使用:0次
名校
7 . 恒温下,将amolN2与bmolH2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g) 2NH3(g)。
2NH3(g)。
(1)某时刻t时,测得nt(N2)=10mol,nt(NH3)=6mol,则a=___ 。
(2)反应达平衡时,混合气体的体积为716.8L(标准状况),其中NH3的体积分数为25%。则平衡时NH3的物质的量为___ 。
(3)原混合气体与平衡混合气体的总物质的量之比n(始)∶n(平)=___ 。
(4)原混合气体中,a∶b=___ 。
(5)达到平衡时,N2和H2的转化率之比,α(N2)∶α(H2)=___ 。
 2NH3(g)。
2NH3(g)。(1)某时刻t时,测得nt(N2)=10mol,nt(NH3)=6mol,则a=
(2)反应达平衡时,混合气体的体积为716.8L(标准状况),其中NH3的体积分数为25%。则平衡时NH3的物质的量为
(3)原混合气体与平衡混合气体的总物质的量之比n(始)∶n(平)=
(4)原混合气体中,a∶b=
(5)达到平衡时,N2和H2的转化率之比,α(N2)∶α(H2)=
您最近一年使用:0次
2020-12-21更新
|
883次组卷
|
3卷引用:重庆市第七中学2020-2021学年高二上学期第一次月考化学试题
名校
解题方法
8 . 填空
(1)已知C(s,石墨)=C(s,金刚石) ΔH>0,则稳定性:金刚石___ (填“>”或“<”)石墨。
(2)已知:2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2;则ΔH1____ (填“>”或“<”)ΔH2。
(3)“嫦娥五号”发射时,用肼(N2H4)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
①N2(g)+2O2(g)=N2O4(g) ΔH=+10.7 kJ·mol-1;
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1
写出气态肼和N2O4反应的热化学方程式:________ 。
(4)25 ℃、101 kPa时,14 g CO在足量的O2中充分燃烧,放出141.3 kJ热量,则CO的燃烧热ΔH=____ 。
(5)0.50 L 2.00 mol·L-1H2SO4溶液与2.10 L 1.00 mol·L-1 KOH溶液完全反应,放出114.6 kJ热量,该反应的中和热ΔH=______ 。
(6)已知断开1 mol H-H键、1 mol N-H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式是________ 。
(1)已知C(s,石墨)=C(s,金刚石) ΔH>0,则稳定性:金刚石
(2)已知:2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2;则ΔH1
(3)“嫦娥五号”发射时,用肼(N2H4)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
①N2(g)+2O2(g)=N2O4(g) ΔH=+10.7 kJ·mol-1;
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1
写出气态肼和N2O4反应的热化学方程式:
(4)25 ℃、101 kPa时,14 g CO在足量的O2中充分燃烧,放出141.3 kJ热量,则CO的燃烧热ΔH=
(5)0.50 L 2.00 mol·L-1H2SO4溶液与2.10 L 1.00 mol·L-1 KOH溶液完全反应,放出114.6 kJ热量,该反应的中和热ΔH=
(6)已知断开1 mol H-H键、1 mol N-H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式是
您最近一年使用:0次
2020-12-15更新
|
320次组卷
|
6卷引用:重庆市沙坪坝实验中学校2021-2022学年高二上学期12月月考化学试题
重庆市沙坪坝实验中学校2021-2022学年高二上学期12月月考化学试题2015届四川省成都郫县高三第二次阶诊断性考试理综化学试卷河北省安平中学2017-2018学年高一下学期期末考试化学试题1贵州省毕节市七星关区毕节市实验高级中学2020-2021学年高二上学期期中考试化学试题(已下线)第六章能力提升检测卷(精练)-2022年高考化学一轮复习讲练测(已下线)专题18 化学反应与能量(限时精练)-2022年高三毕业班化学常考点归纳与变式演练
10-11高一上·江苏南通·期中
名校
解题方法
9 . 现有m g某气体,它由双原子分子构成,它的摩尔质量为M g/mol。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为________ mol。
(2)该气体所含原子总数为__________ 个。
(3)该气体在标准状况下的体积为____________ L。
(4)该气体溶于1 L水中(不考虑反应),其溶液中溶质的质量分数为___________ 。
(5)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为_______ mol/L。
(1)该气体的物质的量为
(2)该气体所含原子总数为
(3)该气体在标准状况下的体积为
(4)该气体溶于1 L水中(不考虑反应),其溶液中溶质的质量分数为
(5)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为
您最近一年使用:0次
2020-10-31更新
|
99次组卷
|
23卷引用:2014-2015学年重庆复旦中学高一上学期期中化学试卷
2014-2015学年重庆复旦中学高一上学期期中化学试卷2015-2016学年重庆市杨家坪中学高一上学期第一次月考化学试卷(已下线)2010年江苏省启东中学高一上学期期中考试化学卷(已下线)2011-2012学年湖北省武汉市江夏区部分中学高一上学期期中考试化学试卷2014-2015学年河南省扶沟县高中高一上学期月考化学试卷2015-2016学年湖北省黄石市有色一中高一上学期10月月考化学试卷2015-2016学年宁夏银川市第九中学高一上学期期中测试化学试卷2015-2016学年宁夏银川唐徕回民中学高一上10月化学卷2015-2016学年贵州省凯里一中高一下开学考试化学试卷2016-2017学年黑龙江省双鸭山一中高一上9月月考化学卷2016-2017学年甘肃省武威二中高一上10月月考化学试卷2016-2017学年山西省怀仁一中高一上期中化学试卷(已下线)2018年9月15日 《每日一题》人教必修1- 周末培优河南省焦作市沁阳一中2018-2019学年高一上学期第一次月考化学试题【全国百强校】吉林省长春外国语学校2018-2019学年高一上学期第一次月考化学试题湖南省株洲市茶陵县第三中学2019-2020学年高一上学期第一次月考化学试题河北省石家庄市普通高中2019-2020学年高一10月月考化学试题黑龙江省哈尔滨市阿城区龙涤中学2019-2020学年高一上学期第一次段考化学试题湖南省衡阳县第四中学2021届高三8月月考化学试题甘肃省庆阳市宁县第二中学2020-2021学年高一上学期第一次月考化学试题云南省保山市第九中学2020-2021学年高一上学期10月阶段性测试化学试题广西壮族自治区贺州高级中学2020-2021学年高一上学期第一次月考化学试题河北省唐山市丰润区2023-2024学年高一上学期期中考试化学试题
解题方法
10 . 欲测定某生铁 主要成分是铁,还含有少量的碳
主要成分是铁,还含有少量的碳 的组成,进行了如下实验:称取粉末状样品
的组成,进行了如下实验:称取粉末状样品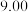 克,加入某浓度的盐酸100mL,充分反应后,收集到标准状况下气体
克,加入某浓度的盐酸100mL,充分反应后,收集到标准状况下气体 ;然后,继续往样品中加入同浓度的盐酸100mL,充分反应后又收集到标准状况下气体
;然后,继续往样品中加入同浓度的盐酸100mL,充分反应后又收集到标准状况下气体 。试求:
。试求: 写出具体计算过程
写出具体计算过程
(1)所取盐酸的物质的量浓度。________
(2)该生铁样品中铁的质量分数 保留3位有效数字
保留3位有效数字 。
。________
 主要成分是铁,还含有少量的碳
主要成分是铁,还含有少量的碳 的组成,进行了如下实验:称取粉末状样品
的组成,进行了如下实验:称取粉末状样品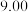 克,加入某浓度的盐酸100mL,充分反应后,收集到标准状况下气体
克,加入某浓度的盐酸100mL,充分反应后,收集到标准状况下气体 ;然后,继续往样品中加入同浓度的盐酸100mL,充分反应后又收集到标准状况下气体
;然后,继续往样品中加入同浓度的盐酸100mL,充分反应后又收集到标准状况下气体 。试求:
。试求: 写出具体计算过程
写出具体计算过程
(1)所取盐酸的物质的量浓度。
(2)该生铁样品中铁的质量分数
 保留3位有效数字
保留3位有效数字 。
。
您最近一年使用:0次



