解题方法
1 . 计算题(要求写出必要的计算过程,只有答案不给分)
(1)在14.8g由碳酸钠和碳酸氢钠组成的混合物中加入足量盐酸后充分反应,收集到0.15mol的二氧化碳,计算混合物中碳酸氢钠的物质的量是多少_______ 。
(2)铅笔芯的主要成分是石墨和黏土,这些物质按照不同的比例加以混合压制,就可以制成铅笔芯。如果铅笔芯质量的一半是石墨,且用铅笔写一个字消耗的质量约为0.5mg,那么一个铅笔字含有的碳原子数约为多少_______ ?
(1)在14.8g由碳酸钠和碳酸氢钠组成的混合物中加入足量盐酸后充分反应,收集到0.15mol的二氧化碳,计算混合物中碳酸氢钠的物质的量是多少
(2)铅笔芯的主要成分是石墨和黏土,这些物质按照不同的比例加以混合压制,就可以制成铅笔芯。如果铅笔芯质量的一半是石墨,且用铅笔写一个字消耗的质量约为0.5mg,那么一个铅笔字含有的碳原子数约为多少
您最近一年使用:0次
2 . 某混合物由FeSO4和Cu(NO3)2两种物质组成,为测定其中各组分的含量,进行以下实验操作,同时得到相关实验数据:

假设NO 的还原产物只有NO,且完全反应。
的还原产物只有NO,且完全反应。
(1)原混合物中FeSO4和Cu(NO3)2的物质的量之比为_______ ;
(2)上述步骤②中n=_______ , 请简要写出计算过程_______ 。

假设NO
 的还原产物只有NO,且完全反应。
的还原产物只有NO,且完全反应。(1)原混合物中FeSO4和Cu(NO3)2的物质的量之比为
(2)上述步骤②中n=
您最近一年使用:0次
3 . 某有机化合物A广泛存在于多种水果中。经测定,A的相对分子质量为134,A仅含碳、氢、氧三种元素。A既可以与乙醇发生酯化反应,又可以与乙酸发生酯化反应,且测得0.1molA与乙醇完全酯化得有机产物的质量为19.0g。
(1)每个有机化合物A分子中含有___________ 个羧基;
(2)有机化合物A的分子式___________ 。(书写计算过程)
(1)每个有机化合物A分子中含有
(2)有机化合物A的分子式
您最近一年使用:0次
2022-01-03更新
|
590次组卷
|
2卷引用:浙江省创新致远协作体2021-2022学年高三上学期12月适应性考试化学试题
名校
4 . 某兴趣小组用盐酸溶解法测定镀锌铁皮锌层厚度,分别取A、B、C三块镀锌铁皮(均截自同一块规则的镀锌铁皮)进行实验,实验数据记录如表。
该镀锌层平均厚度(单侧)为___ cm。(保留两位有效数字)写出简要计算过程:已知:锌的密度为7.14g/cm3。
| 镀锌铁皮 | 长度/cm | 宽度/cm | 反应前固体质量/g | 反应后固体质量/g |
| A | 5.00 | 4.00 | 4.360 | 4.212 |
| B | 5.10 | 4.00 | 4.447 | 4.295 |
| C | 4.90 | 5.10 | 4.438 | 4.330 |
您最近一年使用:0次
2021-12-20更新
|
603次组卷
|
3卷引用:浙江省学军中学2021-2022学年高三上学期模拟测试(一)化学试题
浙江省学军中学2021-2022学年高三上学期模拟测试(一)化学试题(已下线)解密02 物质的量(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)湖南省株洲市第二中学2022-2023学年高一上学期第三次月考化学试题
5 . 我国《居室空气中甲醛的卫生标准》规定,居室空气中甲醛的最高允许浓度为0.08mg·m-3,可以用KMnO4溶液来检测室内甲醛浓度。用移液管准确量取2.00mL1.00×10-5mol·L-1的KMnO4溶液,注入一支带有双孔橡胶塞的试管中,加入1滴6.00mol·L-1的H2SO4溶液,塞好橡胶塞。取一个附针头的50mL注射器,按图组装好装置。将此装置置于待测地点,缓慢抽气,每次抽气50mL,直到试管内溶液的红色褪尽。重复实验,结果如下:

已知:4 +5HCHO+12H+=4Mn2++5CO2↑+11H2O,求:
+5HCHO+12H+=4Mn2++5CO2↑+11H2O,求:
(1)甲醛气体的浓度为___________ mol·L-1。
(2)该居室甲醛浓度是否符合国家标准(写出列式过程)___________ 。
| 实验次数 | KMnO4溶液的浓度/mol·L-1 | KMnO4溶液的体积/mL | 每组实验抽气总体积/mL |
| 1 | 1.00×10-5 | 2.00 | 990 |
| 2 | 1.00×10-5 | 2.00 | 1000 |
| 3 | 1.00×10-5 | 2.00 | 1010 |

已知:4
 +5HCHO+12H+=4Mn2++5CO2↑+11H2O,求:
+5HCHO+12H+=4Mn2++5CO2↑+11H2O,求:(1)甲醛气体的浓度为
(2)该居室甲醛浓度是否符合国家标准(写出列式过程)
您最近一年使用:0次
名校
6 . 取一定量的 样品在空气中加热,其固体残留率随温度的变化如图。已知:样品的固体残留率=固体样品的剩余质量/固体样品的起始质量×100;样品在300℃时已完全失去结晶水,900℃以上残余固体为金属氧化物。
样品在空气中加热,其固体残留率随温度的变化如图。已知:样品的固体残留率=固体样品的剩余质量/固体样品的起始质量×100;样品在300℃时已完全失去结晶水,900℃以上残余固体为金属氧化物。
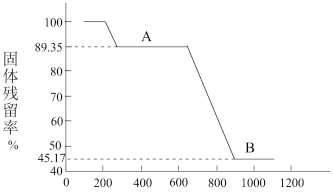
请回答:
(1)加热至500℃时的过程中,样品固体发生分解的化学方程式是_______ 。
(2)曲线B段所表示物质的化学式是_______ (写出计算过程)。
 样品在空气中加热,其固体残留率随温度的变化如图。已知:样品的固体残留率=固体样品的剩余质量/固体样品的起始质量×100;样品在300℃时已完全失去结晶水,900℃以上残余固体为金属氧化物。
样品在空气中加热,其固体残留率随温度的变化如图。已知:样品的固体残留率=固体样品的剩余质量/固体样品的起始质量×100;样品在300℃时已完全失去结晶水,900℃以上残余固体为金属氧化物。
请回答:
(1)加热至500℃时的过程中,样品固体发生分解的化学方程式是
(2)曲线B段所表示物质的化学式是
您最近一年使用:0次
2021-07-30更新
|
190次组卷
|
3卷引用:浙江省台州市2020-2021学年高二下学期期末质量评估化学试题
7 . 硫粉和S2-反应可以生成多硫离子S ,如:S+S2-→S
,如:S+S2-→S 、2S+S2-→S
、2S+S2-→S 。 在10 mL S2-溶液中加入0.080 g硫粉,控制条件使硫粉完全反应,检测到溶液中最大聚合度的多硫离子是S32-,且离子浓度之比符合等比数列1,10,……10n-1。,若不考虑其他副反应,计算反应后溶液中S2-的浓度c1=
。 在10 mL S2-溶液中加入0.080 g硫粉,控制条件使硫粉完全反应,检测到溶液中最大聚合度的多硫离子是S32-,且离子浓度之比符合等比数列1,10,……10n-1。,若不考虑其他副反应,计算反应后溶液中S2-的浓度c1=_______ ,其起始浓度c0=_______ 。
 ,如:S+S2-→S
,如:S+S2-→S 、2S+S2-→S
、2S+S2-→S 。 在10 mL S2-溶液中加入0.080 g硫粉,控制条件使硫粉完全反应,检测到溶液中最大聚合度的多硫离子是S32-,且离子浓度之比符合等比数列1,10,……10n-1。,若不考虑其他副反应,计算反应后溶液中S2-的浓度c1=
。 在10 mL S2-溶液中加入0.080 g硫粉,控制条件使硫粉完全反应,检测到溶液中最大聚合度的多硫离子是S32-,且离子浓度之比符合等比数列1,10,……10n-1。,若不考虑其他副反应,计算反应后溶液中S2-的浓度c1=
您最近一年使用:0次
2021-07-15更新
|
100次组卷
|
3卷引用:浙江省丽水市缙云中学等三校2021-2022学年高三12月份联考化学试题
浙江省丽水市缙云中学等三校2021-2022学年高三12月份联考化学试题(已下线)解密02 物质的量(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)第32届中国化学奥林匹克竞赛(江苏赛区)初赛试题
解题方法
8 . 某固体可能含 、
、 、
、 中的其中二种成分,某实验研究小组取该固体把它配成溶液。用一定浓度的盐酸逐滴加入该溶液中,产生的
中的其中二种成分,某实验研究小组取该固体把它配成溶液。用一定浓度的盐酸逐滴加入该溶液中,产生的 气体的体积(标准状况下)与加入盐酸的体积示意图如下:
气体的体积(标准状况下)与加入盐酸的体积示意图如下:
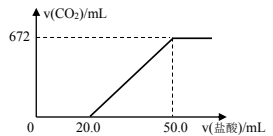
(1)盐酸的物质的量浓度为___________  ;
;
(2)该固体中两种化合物的物质的量之比为___________ (写出计算过程)。
 、
、 、
、 中的其中二种成分,某实验研究小组取该固体把它配成溶液。用一定浓度的盐酸逐滴加入该溶液中,产生的
中的其中二种成分,某实验研究小组取该固体把它配成溶液。用一定浓度的盐酸逐滴加入该溶液中,产生的 气体的体积(标准状况下)与加入盐酸的体积示意图如下:
气体的体积(标准状况下)与加入盐酸的体积示意图如下:
(1)盐酸的物质的量浓度为
 ;
;(2)该固体中两种化合物的物质的量之比为
您最近一年使用:0次
2021-07-08更新
|
699次组卷
|
2卷引用:浙江省”共美联盟“2020-2021学年高二下学期期末模拟化学试题
9 . 将24.5gKClO3固体与8.7gMnO2固体混合加热片刻,得到标况下VL气体,冷却后固体质量为25.52g;再将剩余固体溶于水并加入足量亚硝酸钠和硝酸银溶液,再加足量的稀硝酸,过滤、洗涤、干燥得到m克固体。求:
(1)标准状况下气体体积V为___ 。
(2)最后所得固体质量m为___ g。
(1)标准状况下气体体积V为
(2)最后所得固体质量m为
您最近一年使用:0次
解题方法
10 . 现有含Na2CO3、NaHCO3的固体混合物54.8g,溶于水搅拌均匀分成两等份。向其中一份中加足量Ba(OH)2溶液,经过滤、洗涤、干燥,得白色沉淀59.1g。求:
(1)所得白色沉淀的物质的量n=_______ mol
(2)原固体中NaHCO3的物质的量为_______
(1)所得白色沉淀的物质的量n=
(2)原固体中NaHCO3的物质的量为
您最近一年使用:0次



