解题方法
1 . 将某质量的镁铝合金溶解在500 mL盐酸中,向反应后的溶液中逐滴加入2 mol/L NaOH溶液,产生沉淀质量与碱溶液体积的关系如图所示。请填写下列空白:
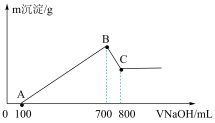
(1)写出BC段发生反应的化学方程式:_______ 。
(2)合金中铝的质量为_______ 。
(3)盐酸的物质的量浓度(假设反应后溶液体积不变)是_______ 。

(1)写出BC段发生反应的化学方程式:
(2)合金中铝的质量为
(3)盐酸的物质的量浓度(假设反应后溶液体积不变)是
您最近一年使用:0次
2 . 实验室通常利用质量分数36.5%盐酸(密度为1.14g/mL)与二氧化锰通过反应制取Cl2。通过计算回答下列问题:
(1)质量分数36.5%(密度为1.14g/mL)盐酸的物质的量浓度为_______ 。
(2)若要制取2.24L Cl2(标准状况),理论上需要消耗MnO2质量为_______ 克。
(3)此时,被氧化HCl的物质的量为_______ 。
(1)质量分数36.5%(密度为1.14g/mL)盐酸的物质的量浓度为
(2)若要制取2.24L Cl2(标准状况),理论上需要消耗MnO2质量为
(3)此时,被氧化HCl的物质的量为
您最近一年使用:0次
解题方法
3 . 某有机化合物A由碳、氢两种元素组成,0.1mol该有机物充分燃烧后将产物依次通入浓硫酸和碱石灰,最后浓硫酸质量增加9g,碱石灰质量增加17.6g,求
(1)写出该化合物的分子式___________ 。
(2)写出该化合物所有可能具有的结构简式___________ 。
(1)写出该化合物的分子式
(2)写出该化合物所有可能具有的结构简式
您最近一年使用:0次
解题方法
4 . 将硝酸钠(NaNO3)和硝酸钡[Ba(NO3)2]的混合物29.1g放入烧杯,加入100.0g水使其完全溶解,再加入94.2g硫酸钠溶液恰好完全反应,过滤(忽略溶液的损失),称得滤液的质量为200.0g。请计算:
(1)恰好完全反应后产生的沉淀质量为______ g。
(2)所得滤液的溶质质量分数(写出完整的解题过程)________ 。
(1)恰好完全反应后产生的沉淀质量为
(2)所得滤液的溶质质量分数(写出完整的解题过程)
您最近一年使用:0次
5 . 有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色粘稠液体,易溶于水。
(1)为研究A的组成与结构,进行如下实验:
(2)综上所述,A的结构简式为___________ 。
(3)两分子A可反应生成一个六元环状化合物,写出该反应的化学方程式___________ 。
(1)为研究A的组成与结构,进行如下实验:
| 实验步骤: | 实验结论 |
| ①称取9.0 g A,升温使其汽化,测其密度是相同条件下H2的45倍 | A的相对分子质量为 |
| ②将此9.0 g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4 g和13.2 g | A的分子式为 |
| ③另取9.0 g A,与足量的NaHCO3粉末反应,生成2.24 LCO2(标准状况);若与足量金属钠反应则生成2.24 LH2 (标准状况) | 用结构简式表示A中含有的官能团 |
④A的核磁共振氢谱如图: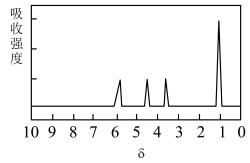 | A中含有 |
(3)两分子A可反应生成一个六元环状化合物,写出该反应的化学方程式
您最近一年使用:0次
2023-07-31更新
|
132次组卷
|
2卷引用:陕西省延安市宜川中学2020-2021学年高二上学期期末考试化学试题
名校
解题方法
6 . 71gNa2SO4的物质的量为______ mol,含有Na+_____ mol,完全溶于水,配成2L溶液,则所得溶液中Na2SO4的物质的量浓度为_____ mol/L。
您最近一年使用:0次
7 . 9.03×1023个NH3的物质的量为_____ 摩尔,含_____ 摩尔质子,在标准状况下的体积是_____ L。
您最近一年使用:0次
21-22高一上·浙江·阶段练习
解题方法
8 . 向含CuCl2和HCl的100g混合溶液中,逐滴加溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图[仅考虑沉淀为Cu(OH)2]。求:_____ 。
(2)图像中,m1=_____ 。
(3)计算M点时溶液中溶质的质量分数_____ (结果保留到0.1%)。

(2)图像中,m1=
(3)计算M点时溶液中溶质的质量分数
您最近一年使用:0次
名校
解题方法
9 . 苯乙烯(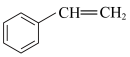 )常用来合成橡胶,还广泛应用于制药、染料、农药等行业,是石化行业的重要基础原料,苯乙烯与各物质之间反应的能量变化如下:
)常用来合成橡胶,还广泛应用于制药、染料、农药等行业,是石化行业的重要基础原料,苯乙烯与各物质之间反应的能量变化如下:
I.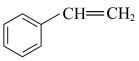


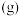

II.

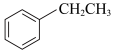
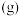
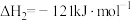
III.


IV.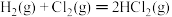

回答下列问题:
(1)①根据上述反应计算得△H3=___________ kJ/mol。
②设NA为阿伏加德罗常数的值。反应II每生成5.3 g苯乙烷,放出的热量为___________ kJ,转移的电子数为___________ NA。
(2)相关化学键的键能数据如下表所示。
①x=___________ 。
②完全燃烧5.2 g苯乙烯,消耗氧气___________ mol。
 )常用来合成橡胶,还广泛应用于制药、染料、农药等行业,是石化行业的重要基础原料,苯乙烯与各物质之间反应的能量变化如下:
)常用来合成橡胶,还广泛应用于制药、染料、农药等行业,是石化行业的重要基础原料,苯乙烯与各物质之间反应的能量变化如下:I.



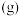

II.



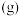
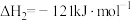
III.



IV.
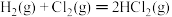

回答下列问题:
(1)①根据上述反应计算得△H3=
②设NA为阿伏加德罗常数的值。反应II每生成5.3 g苯乙烷,放出的热量为
(2)相关化学键的键能数据如下表所示。
| 化学键 | Cl-Cl | H-Cl | H-H |
| 键能/(kJ/mol) | 243 | x | 436 |
②完全燃烧5.2 g苯乙烯,消耗氧气
您最近一年使用:0次
2022-09-04更新
|
522次组卷
|
4卷引用:云南省梁河县第一中学2021-2022学年高二上学期第二次月考化学试题
解题方法
10 . 如图是某硫酸试剂瓶标签上的部分文字说明。请计算:
(1)H2SO4的摩尔质量为_____ g/mol。
(2)该试剂瓶中H2SO4的物质的量浓度为______ mol/L。
(3)取10mL该硫酸稀释至100mL,与足量锌粒充分反应求生成氢气的质量______ (写出计算过程)。
| 硫酸 500mL 化学式: H2SO4 密度: 1.84 g/cm3 质量分数: 98% |
(2)该试剂瓶中H2SO4的物质的量浓度为
(3)取10mL该硫酸稀释至100mL,与足量锌粒充分反应求生成氢气的质量
您最近一年使用:0次
2023-01-07更新
|
310次组卷
|
2卷引用:2021年河南省普通高中学生学业水平考试化学试题



