名校
解题方法
1 . 氮元素的单质及其化合物在工农业生产、生活中有着重要作用。回答下列问题:
I.一定条件下,在2 L密闭容器中发生反应:3A(g) + B(g) 2C(g)。开始时加入4 mol A,6 mol B,2molC,在2 min末测得C的物质的量是3mol。
2C(g)。开始时加入4 mol A,6 mol B,2molC,在2 min末测得C的物质的量是3mol。
(1)用A的浓度变化表示反应的平均速率:___________ 。
(2)在2 min末,B的浓度为___________ 。
II.某反应过程的能量变化如下图所示。
(3)反应过程___________ (填“a”或“b”)有催化剂参与。
(4)①该反应为___________ 反应(填“放热”或“吸热”)。
②已知:
反应i:
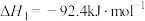
反应ii:
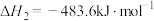
则氨气完全燃烧生成氮气和水蒸气的热化学方程式为___________ 。
III.已知反应i断开化学键所需的能量如下表。
(5)则断开 N—H键所需的能量是
N—H键所需的能量是___________ 。
I.一定条件下,在2 L密闭容器中发生反应:3A(g) + B(g)
 2C(g)。开始时加入4 mol A,6 mol B,2molC,在2 min末测得C的物质的量是3mol。
2C(g)。开始时加入4 mol A,6 mol B,2molC,在2 min末测得C的物质的量是3mol。(1)用A的浓度变化表示反应的平均速率:
(2)在2 min末,B的浓度为
II.某反应过程的能量变化如下图所示。
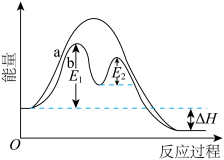
(3)反应过程
(4)①该反应为
②已知:
反应i:

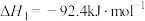
反应ii:

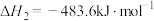
则氨气完全燃烧生成氮气和水蒸气的热化学方程式为
III.已知反应i断开化学键所需的能量如下表。
| 化学键 |  | H—H | N—H |
键能/ | 945 | 436 | ? |
(5)则断开
 N—H键所需的能量是
N—H键所需的能量是
您最近一年使用:0次
名校
解题方法
2 . 为测定某铝镁铜合金中铝、镁的质量分数,进行如下实验(忽略反应中水的蒸发):①向30.0g合金粉末中加入200g 30.0% NaOH溶液,充分反应后,称得固液混合物质量为227.0g。②再向混合液中加入过量稀硫酸,充分反应后剩余固体洗涤干燥后称得质量为0.6g。(计算结果保留一位小数)
(1)查得室温下30.0% NaOH溶液密度为1.33g/mL,则该NaOH溶液的物质的量浓度为___________ mol/L。
(2)30.0g合金中Al的质量为___________ g。
(3)合金中Mg元素的质量分数为___________ 。
(1)查得室温下30.0% NaOH溶液密度为1.33g/mL,则该NaOH溶液的物质的量浓度为
(2)30.0g合金中Al的质量为
(3)合金中Mg元素的质量分数为
您最近一年使用:0次
3 . 常温下, 、HCOOH(甲酸)、二元弱酸
、HCOOH(甲酸)、二元弱酸 的电离常数见下表,下列说法正确的是
的电离常数见下表,下列说法正确的是
 、HCOOH(甲酸)、二元弱酸
、HCOOH(甲酸)、二元弱酸 的电离常数见下表,下列说法正确的是
的电离常数见下表,下列说法正确的是| 分子式 |  | HCOOH |  |
| 电离常数 |  |  |  、 、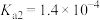 |
A.等物质的量浓度的几种溶液pH大小关系: |
B.HCOONa溶液中滴入少量 ,发生反应 ,发生反应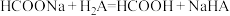 |
C.NaHA溶液中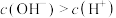 |
D. 的电离常数小于 的电离常数小于 |
您最近一年使用:0次
名校
解题方法
4 . 工业上常用纯碱( )溶液吸收尾气中的NO、
)溶液吸收尾气中的NO、 。某纯碱样品中含杂质NaCl,取质量为a g的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到b g固体物质,则此样品中
。某纯碱样品中含杂质NaCl,取质量为a g的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到b g固体物质,则此样品中 的质量分数为
的质量分数为___________ 。
 )溶液吸收尾气中的NO、
)溶液吸收尾气中的NO、 。某纯碱样品中含杂质NaCl,取质量为a g的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到b g固体物质,则此样品中
。某纯碱样品中含杂质NaCl,取质量为a g的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到b g固体物质,则此样品中 的质量分数为
的质量分数为
您最近一年使用:0次
名校
解题方法
5 . “微生物法”处理含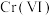 废水具有效率高、选择性强、吸附容量大等优点。一种微生物法是用硫酸盐还原菌(SRB)处理含
废水具有效率高、选择性强、吸附容量大等优点。一种微生物法是用硫酸盐还原菌(SRB)处理含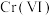 废水。
废水。
(1)硫酸盐还原菌能将水中的 转化为
转化为 ,
, 与
与 可反应生成
可反应生成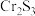 和
和 两种沉淀。写出
两种沉淀。写出 与
与 反应的离子方程式:
反应的离子方程式:___________ 。
(2)用硫酸盐还原菌(SRB)处理含铬废水时,温度常控制在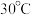 左右,温度过高,
左右,温度过高,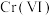 的去除率低的原因是
的去除率低的原因是___________ 。
(3)硫酸盐还原菌(SRB)常存在于水体中,会腐蚀许多金属及合金。一种Fe合金在硫酸盐还原菌存在条件下腐蚀的机理如图所示。已知溶液中的 会完全转化为
会完全转化为 ,则
,则 腐蚀后生成
腐蚀后生成 和
和 的物质的量之比为
的物质的量之比为___________ 。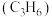 为原料脱硝除去NO,将NO转化为对环境友好的物质。研究表明催化剂添加助剂后催化活性提高的原因是形成活性
为原料脱硝除去NO,将NO转化为对环境友好的物质。研究表明催化剂添加助剂后催化活性提高的原因是形成活性 参与反应,图2为丙烯脱硝机理。
参与反应,图2为丙烯脱硝机理。___________ ,乙为___________ 。(用化学式表示)
②若参加反应的丙烯与 物质的量之比为
物质的量之比为 ,则反应的化学方程式为
,则反应的化学方程式为___________ 。
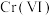 废水具有效率高、选择性强、吸附容量大等优点。一种微生物法是用硫酸盐还原菌(SRB)处理含
废水具有效率高、选择性强、吸附容量大等优点。一种微生物法是用硫酸盐还原菌(SRB)处理含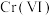 废水。
废水。(1)硫酸盐还原菌能将水中的
 转化为
转化为 ,
, 与
与 可反应生成
可反应生成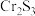 和
和 两种沉淀。写出
两种沉淀。写出 与
与 反应的离子方程式:
反应的离子方程式:(2)用硫酸盐还原菌(SRB)处理含铬废水时,温度常控制在
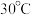 左右,温度过高,
左右,温度过高,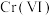 的去除率低的原因是
的去除率低的原因是(3)硫酸盐还原菌(SRB)常存在于水体中,会腐蚀许多金属及合金。一种Fe合金在硫酸盐还原菌存在条件下腐蚀的机理如图所示。已知溶液中的
 会完全转化为
会完全转化为 ,则
,则 腐蚀后生成
腐蚀后生成 和
和 的物质的量之比为
的物质的量之比为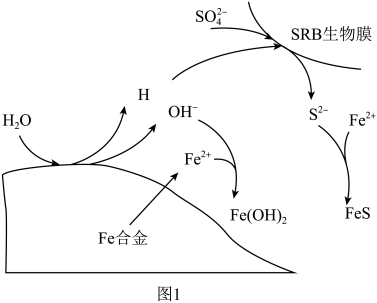
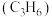 为原料脱硝除去NO,将NO转化为对环境友好的物质。研究表明催化剂添加助剂后催化活性提高的原因是形成活性
为原料脱硝除去NO,将NO转化为对环境友好的物质。研究表明催化剂添加助剂后催化活性提高的原因是形成活性 参与反应,图2为丙烯脱硝机理。
参与反应,图2为丙烯脱硝机理。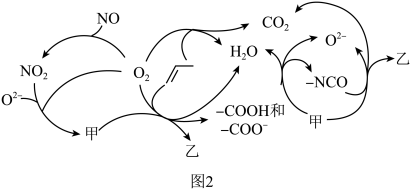
②若参加反应的丙烯与
 物质的量之比为
物质的量之比为 ,则反应的化学方程式为
,则反应的化学方程式为
您最近一年使用:0次
名校
解题方法
6 . 天然气的主要成分为 ,一般还含有
,一般还含有 、
、 等烃类,是重要的燃料和化工原料。
等烃类,是重要的燃料和化工原料。
(1)乙烷在一定条件可发生如下反应:
 ,相关物质的摩尔燃烧焓数据如表所示:
,相关物质的摩尔燃烧焓数据如表所示:
则
_____ 
(2)甲烷是常见的燃料, 加氢可制备甲烷,其反应为
加氢可制备甲烷,其反应为
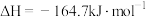 。
。
①
_____ 。
②对于 加氢制备甲烷的反应,有关说法错误的是
加氢制备甲烷的反应,有关说法错误的是_____ 。
A.该反应理论上可以设计成原电池
B.该反应过程中有旧键断裂吸收的能量大于新键形成释放的能量
C.反应结束,体系中物质的总能量降低
D.此反应可以变废为宝,有利于碳中和和碳达峰的实现
③已知:标准摩尔生成焓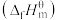 是指标况下,由元素最稳定的单质生成1mol纯净物时的反应焓变。298K时,几种气态物质标准摩尔生成焓如表:
是指标况下,由元素最稳定的单质生成1mol纯净物时的反应焓变。298K时,几种气态物质标准摩尔生成焓如表:
则
_____ 。
(3)丙烷燃烧可以通过以下两种途径:
途径I:
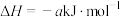
途径Ⅱ: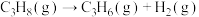
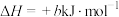

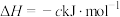

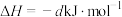 (a、b、c、d均为正值)
(a、b、c、d均为正值)
按途径Ⅱ反应,常温下,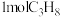 完全燃烧时放出的热量为
完全燃烧时放出的热量为_____ kJ(用含b、c、d的代数式表示);相同条件下,等量的丙烷通过两种途径完全燃烧时,途径I放出的热量_____ (填“大于”、“小于”或“等于”)途径Ⅱ放出的热量。
 ,一般还含有
,一般还含有 、
、 等烃类,是重要的燃料和化工原料。
等烃类,是重要的燃料和化工原料。(1)乙烷在一定条件可发生如下反应:

 ,相关物质的摩尔燃烧焓数据如表所示:
,相关物质的摩尔燃烧焓数据如表所示:| 物质 | 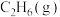 |  |  |
摩尔燃烧焓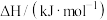 | -1560 | -1411 | -286 |


(2)甲烷是常见的燃料,
 加氢可制备甲烷,其反应为
加氢可制备甲烷,其反应为
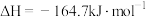 。
。| 物质 |  |  |  |  |
| 键能:1mol化学键断裂时需要吸收的能量/kJ | 436 | 465 | 413 | a |

②对于
 加氢制备甲烷的反应,有关说法错误的是
加氢制备甲烷的反应,有关说法错误的是A.该反应理论上可以设计成原电池
B.该反应过程中有旧键断裂吸收的能量大于新键形成释放的能量
C.反应结束,体系中物质的总能量降低
D.此反应可以变废为宝,有利于碳中和和碳达峰的实现
③已知:标准摩尔生成焓
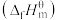 是指标况下,由元素最稳定的单质生成1mol纯净物时的反应焓变。298K时,几种气态物质标准摩尔生成焓如表:
是指标况下,由元素最稳定的单质生成1mol纯净物时的反应焓变。298K时,几种气态物质标准摩尔生成焓如表:| 物质 |  |  |  |  |
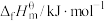 | -393.5 | -241.5 | x | 0 |

(3)丙烷燃烧可以通过以下两种途径:
途径I:

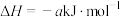
途径Ⅱ:
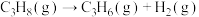
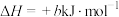

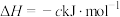

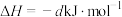 (a、b、c、d均为正值)
(a、b、c、d均为正值)按途径Ⅱ反应,常温下,
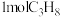 完全燃烧时放出的热量为
完全燃烧时放出的热量为
您最近一年使用:0次
名校
7 . 硝酸工业废气中含有 有害气体,需处理后才能排放.常用NaOH溶液吸收,其反应原理如下:
有害气体,需处理后才能排放.常用NaOH溶液吸收,其反应原理如下:
①
②
现有一定条件下0.5mol 和0.1molNO的混合气体恰好被300mLNaOH溶液完全吸收.则NaOH溶液的物质的量浓度为
和0.1molNO的混合气体恰好被300mLNaOH溶液完全吸收.则NaOH溶液的物质的量浓度为________  。(写出具体计算过程)
。(写出具体计算过程)
 有害气体,需处理后才能排放.常用NaOH溶液吸收,其反应原理如下:
有害气体,需处理后才能排放.常用NaOH溶液吸收,其反应原理如下:①

②

现有一定条件下0.5mol
 和0.1molNO的混合气体恰好被300mLNaOH溶液完全吸收.则NaOH溶液的物质的量浓度为
和0.1molNO的混合气体恰好被300mLNaOH溶液完全吸收.则NaOH溶液的物质的量浓度为 。(写出具体计算过程)
。(写出具体计算过程)
您最近一年使用:0次
8 .  可用于光电材料,为测定某实验小组制得的产品中硫化氢的质量分数(设该产品中的其他成分不与
可用于光电材料,为测定某实验小组制得的产品中硫化氢的质量分数(设该产品中的其他成分不与 溶液反应):
溶液反应):
Ⅰ.取0.68000 g 产品,与足量
产品,与足量 溶液充分反应后。
溶液充分反应后。
Ⅱ.将生成的CuS置于已恒重、质量为31.230 g的坩埚中煅烧,恒重后总质量为32.814 g。
请计算:
(1)实验过程中化学科研工作者使用了950 mL 0.60000 mol/L 溶液,该试剂的物质的量为
溶液,该试剂的物质的量为___________ mol。
(2)Ⅱ中CuS煅烧成CuO,CuO的物质的量为___________ mol。
(3)产品中硫化氢的质量分数为___________ 。
 可用于光电材料,为测定某实验小组制得的产品中硫化氢的质量分数(设该产品中的其他成分不与
可用于光电材料,为测定某实验小组制得的产品中硫化氢的质量分数(设该产品中的其他成分不与 溶液反应):
溶液反应):Ⅰ.取0.68000 g
 产品,与足量
产品,与足量 溶液充分反应后。
溶液充分反应后。Ⅱ.将生成的CuS置于已恒重、质量为31.230 g的坩埚中煅烧,恒重后总质量为32.814 g。
请计算:
(1)实验过程中化学科研工作者使用了950 mL 0.60000 mol/L
 溶液,该试剂的物质的量为
溶液,该试剂的物质的量为(2)Ⅱ中CuS煅烧成CuO,CuO的物质的量为
(3)产品中硫化氢的质量分数为
您最近一年使用:0次
解题方法
9 . 我国科学家制备了高选择性的二氧化碳加氢合成甲醇的催化剂氧化锆,其晶胞如下图所示。
(2)结合图中数据,计算该晶胞的密度ρ=___________ g·cm−3。(设NA为阿伏加德罗常数,用含a、b和NA的代数式表示)

| A.ZrO2 | B.ZrO | C.Zr2O | D.Zr2O3 |
(2)结合图中数据,计算该晶胞的密度ρ=
您最近一年使用:0次
名校
解题方法
10 . 土壤中的硝酸盐会被细菌分解。有一种脱氧硫杆菌能够利用土壤中的硫化物来分解硝酸盐,其主要化学原理为:
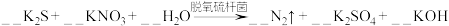 。
。
(1)配平上述反应方程式,并用单线桥标出电子转移的方向和数目___________ 。
(2)被氧化的元素是___________ 。
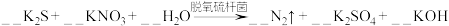 。
。(1)配平上述反应方程式,并用单线桥标出电子转移的方向和数目
(2)被氧化的元素是
您最近一年使用:0次



