解题方法
1 . 以石英砂(主要成分为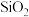 )为原料,经三步反应制得高纯硅,其中第一步反应的化学方程式如下。
)为原料,经三步反应制得高纯硅,其中第一步反应的化学方程式如下。
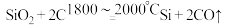
(1)作还原剂的物质是_______ ,碳元素的化合价_______ (填“升高”或“降低”)。
(2)若反应中消耗了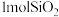 ,则生成
,则生成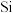 的物质的量为
的物质的量为_______  ,转移电子的物质的量为
,转移电子的物质的量为_______  。
。
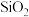 )为原料,经三步反应制得高纯硅,其中第一步反应的化学方程式如下。
)为原料,经三步反应制得高纯硅,其中第一步反应的化学方程式如下。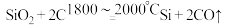
(1)作还原剂的物质是
(2)若反应中消耗了
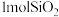 ,则生成
,则生成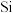 的物质的量为
的物质的量为 ,转移电子的物质的量为
,转移电子的物质的量为 。
。
您最近一年使用:0次
解题方法
2 . 食品包装中的铁系脱氧剂由还原铁粉、氯化钠和炭粉等组成,利用铁的吸氧腐蚀除去氧气,主要反应有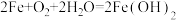 ,
,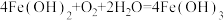 。已知某脱氧剂中含有2.24g还原铁粉,请计算:
。已知某脱氧剂中含有2.24g还原铁粉,请计算:
(1)还原铁粉的物质的量是_______ mol。
(2)若还原铁粉完全转化为Fe(OH)3,则转移电子的物质的量是_______ mol。
(3)在25 和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理
和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理_______ mL包装盒中的空气。
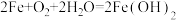 ,
,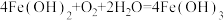 。已知某脱氧剂中含有2.24g还原铁粉,请计算:
。已知某脱氧剂中含有2.24g还原铁粉,请计算:(1)还原铁粉的物质的量是
(2)若还原铁粉完全转化为Fe(OH)3,则转移电子的物质的量是
(3)在25
 和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理
和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理
您最近一年使用:0次
解题方法
3 . 从1L NaOH溶液取出100mL,若将取出的这100mL NaOH溶液加水稀释至500mL,所得溶液中溶质的物质的量浓度是
NaOH溶液取出100mL,若将取出的这100mL NaOH溶液加水稀释至500mL,所得溶液中溶质的物质的量浓度是______  ?含NaOH的质量
?含NaOH的质量______ 克?
 NaOH溶液取出100mL,若将取出的这100mL NaOH溶液加水稀释至500mL,所得溶液中溶质的物质的量浓度是
NaOH溶液取出100mL,若将取出的这100mL NaOH溶液加水稀释至500mL,所得溶液中溶质的物质的量浓度是 ?含NaOH的质量
?含NaOH的质量
您最近一年使用:0次
解题方法
4 . 在氧气中燃烧0.22g硫和铁组成的混合物,使其中的硫全部转化为二氧化硫,把这些二氧化硫全部氧化成三氧化硫并转变为硫酸,这些硫酸可用10mL 氢氧化钠溶液完全中和,则原混合物中硫的百分含量为
氢氧化钠溶液完全中和,则原混合物中硫的百分含量为______ ?
 氢氧化钠溶液完全中和,则原混合物中硫的百分含量为
氢氧化钠溶液完全中和,则原混合物中硫的百分含量为
您最近一年使用:0次
解题方法
5 . 铝是典型的两性金属,既能与酸反应,又能与强碱溶液反应。回答下列问题:
(1)在铝分别与盐酸和氢氧化钠溶液的反应中,铝元素化合价的变化都是___________ (升高/降低),还原剂都是___________ 。
(2)1mol的铝分别与足量的稀盐酸和氢氧化钠溶液反应,生成氢气的体积在相同状况下比值为___________ ,消耗氯化氢和氢氧化钠的物质的量之比为___________ 。
甲、乙两个烧杯中分别盛有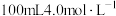 的盐酸和
的盐酸和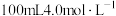 氢氧化钠溶液,向两个烧杯中都加入5.4g铝粉,在相同状况下产生气体的体积比为
氢氧化钠溶液,向两个烧杯中都加入5.4g铝粉,在相同状况下产生气体的体积比为___________ 。反应中消耗的NaOH与HCl的物质的量之比为___________ 。
(1)在铝分别与盐酸和氢氧化钠溶液的反应中,铝元素化合价的变化都是
(2)1mol的铝分别与足量的稀盐酸和氢氧化钠溶液反应,生成氢气的体积在相同状况下比值为
甲、乙两个烧杯中分别盛有
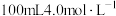 的盐酸和
的盐酸和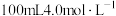 氢氧化钠溶液,向两个烧杯中都加入5.4g铝粉,在相同状况下产生气体的体积比为
氢氧化钠溶液,向两个烧杯中都加入5.4g铝粉,在相同状况下产生气体的体积比为
您最近一年使用:0次
解题方法
6 . 工业上常以铝土矿为原料来冶炼金属铝。已知:铝土矿的主要成分是 (其中含有
(其中含有 、
、 等杂质)。为检测某铝土矿样品中
等杂质)。为检测某铝土矿样品中 的含量,进行如下实验过程:
的含量,进行如下实验过程:
①取矿样10.0g加入过量稀盐酸溶解,过滤弃去不溶残渣。
②将滤液稀释并在250mL容量瓶中定容后,取25.0mL逐滴加入 的NaOH溶液。得到如右图所示的变化关系。
的NaOH溶液。得到如右图所示的变化关系。___________ 。
(2)最后所得不溶于NaOH溶液的沉淀的化学式为___________ ,其物质的量为___________ 。
(3)该铝土矿样中 的质量分数为
的质量分数为___________ 。
 (其中含有
(其中含有 、
、 等杂质)。为检测某铝土矿样品中
等杂质)。为检测某铝土矿样品中 的含量,进行如下实验过程:
的含量,进行如下实验过程:①取矿样10.0g加入过量稀盐酸溶解,过滤弃去不溶残渣。
②将滤液稀释并在250mL容量瓶中定容后,取25.0mL逐滴加入
 的NaOH溶液。得到如右图所示的变化关系。
的NaOH溶液。得到如右图所示的变化关系。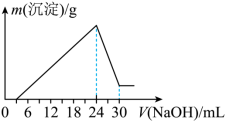
(2)最后所得不溶于NaOH溶液的沉淀的化学式为
(3)该铝土矿样中
 的质量分数为
的质量分数为
您最近一年使用:0次
解题方法
7 . 如图是某学校实验室从化学试剂商店买回来的氢氧化钠试剂标签上的部分内容。某同学从该试剂瓶中取出24.0 g固体,配成1 L溶液,请计算:
(1)所得氢氧化钠溶液的物质的量浓度为___________ 。
(2)从所得氢氧化钠溶液中取出200 mL于一烧杯中,投入2.7 g的金属铝,产生的气体在标准状况下的体积为___________ 。(写出解答步骤)
| 氢氧化钠 化学纯(CP) 500 g 品名:氢氧化钠 化学式:NaOH 相对分子质量:40 |
(2)从所得氢氧化钠溶液中取出200 mL于一烧杯中,投入2.7 g的金属铝,产生的气体在标准状况下的体积为
您最近一年使用:0次
解题方法
8 . 生活离不开化学,家庭厨卫用品中有许多常见的化学物质,括号内为厨卫用品的主要成分:①漂白粉;②NaClO;③Cl2;④Na2CO3;⑤小苏打(NaHCO3);⑥生铁;⑦甲烷。回答下列问题:
(1)漂白液的有效成分NaClO在水溶液的电离方程式:___________ 。
(2)厨卫用品的主要成分(括号内的物质):是电解质的有___________ (填序号,下同),是非电解质的有___________ 。
(3)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常用的消毒药品:
84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。0.5mol过氧乙酸(CH3COOOH)的质量为___________ g。
(4)实验室制Cl2的化学方程式___________ ,收集到33.6L(折算到标准状态)氯气时该反应总共转移的电子数___________ 。
(1)漂白液的有效成分NaClO在水溶液的电离方程式:
(2)厨卫用品的主要成分(括号内的物质):是电解质的有
(3)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常用的消毒药品:
84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。0.5mol过氧乙酸(CH3COOOH)的质量为
(4)实验室制Cl2的化学方程式
您最近一年使用:0次
解题方法
9 . 写出下列反应的离子方程式。
(1)往澄清石灰水中通入少量二氧化碳:______ 。
(2) 与
与 溶液反应:
溶液反应:______ 。
(3)小苏打可以用于治疗胃酸过多:______ 。
(4)向 溶液中加入少量
溶液中加入少量 溶液:
溶液:______ 。
(5)常温下, 溶液与
溶液与 溶液反应至溶液
溶液反应至溶液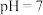 :
:______ 。
(6)高铁酸钠( )是水处理过程中的一种新型的绿色多功能净水剂。湿法制备高铁酸钾(
)是水处理过程中的一种新型的绿色多功能净水剂。湿法制备高铁酸钾( )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:______
(1)往澄清石灰水中通入少量二氧化碳:
(2)
 与
与 溶液反应:
溶液反应:(3)小苏打可以用于治疗胃酸过多:
(4)向
 溶液中加入少量
溶液中加入少量 溶液:
溶液:(5)常温下,
 溶液与
溶液与 溶液反应至溶液
溶液反应至溶液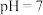 :
:(6)高铁酸钠(
 )是水处理过程中的一种新型的绿色多功能净水剂。湿法制备高铁酸钾(
)是水处理过程中的一种新型的绿色多功能净水剂。湿法制备高铁酸钾( )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:
您最近一年使用:0次
解题方法
10 . 填空题。
(1)有下列七种物质:①石灰水②KOH③稀硫酸④液氯⑤蔗糖⑥CuSO4•5H2O⑦SO2。其中属于氧化物的是_______ (填序号,下同);属于混合物的是_______ ;属于电解质的是_______ ;属于非电解质的是_______ 。
(2)3.4克NH3中所含氢原子数目与标准状况下约______ LH2S所含氢原子数目相等。
(3)15.6gNa2X中含有Na+0.4mol,则X的摩尔质量为_______ 。
(4)标准状态下,672mL某气体质量为1.92g,该气体的摩尔质量为_______ 。
(5)同温同压下,同质量的甲烷(CH4)和氨气物质的量之比为_______ ;氢原子总数之比为_______ ;体积之比为_______ ;密度之比为_______ 。
(1)有下列七种物质:①石灰水②KOH③稀硫酸④液氯⑤蔗糖⑥CuSO4•5H2O⑦SO2。其中属于氧化物的是
(2)3.4克NH3中所含氢原子数目与标准状况下约
(3)15.6gNa2X中含有Na+0.4mol,则X的摩尔质量为
(4)标准状态下,672mL某气体质量为1.92g,该气体的摩尔质量为
(5)同温同压下,同质量的甲烷(CH4)和氨气物质的量之比为
您最近一年使用:0次



