解题方法
1 . 维生素C是人体必须的营养素,又称抗坏血酸,还具备提高免疫力的功效,体内维生素C含量高的人不容易吸收铅、镉、铬等有害元素。维生素C主要存在于新鲜蔬菜和水果中,所以提倡多吃蔬菜和水果。维生素C的化学式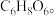 请据此计算:
请据此计算:
(1)维生素C的相对分子质量_______ 。
(2)维生素C中碳元素的质量分数_______ 。(精确到0.1)
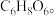 请据此计算:
请据此计算:(1)维生素C的相对分子质量
(2)维生素C中碳元素的质量分数
您最近一年使用:0次
名校
2 . 三聚氰胺最早被李比希于1834年合成。它有毒,不可用于食品加工或食品添加剂。经李比希法分析得知,三聚氰胺分了中,氮元素的含量高达 ,氢元素的质量分数为
,氢元素的质量分数为 ,其余为碳元素。它的相对分子质量大于100,但小于150。回答下列问题:
,其余为碳元素。它的相对分子质量大于100,但小于150。回答下列问题:
(1)分子式中原子个数比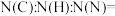
_______ 。
(2)三聚氰胺分子中碳原子数为_______ 。
(3)三聚氰胺的分子式为_______ 。
(4)若核磁共振氢谱显示只有1个吸收峰,红外光谱表征有1个由碳氮两种元素组成的六元杂环。则三聚氰胺的结构简式为_______ 。
 ,氢元素的质量分数为
,氢元素的质量分数为 ,其余为碳元素。它的相对分子质量大于100,但小于150。回答下列问题:
,其余为碳元素。它的相对分子质量大于100,但小于150。回答下列问题:(1)分子式中原子个数比
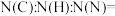
(2)三聚氰胺分子中碳原子数为
(3)三聚氰胺的分子式为
(4)若核磁共振氢谱显示只有1个吸收峰,红外光谱表征有1个由碳氮两种元素组成的六元杂环。则三聚氰胺的结构简式为
您最近一年使用:0次
3 . 镍氢电池是一种新型绿色电池,利用废旧镍氢电池的金属电极芯(主要成分为Ni(OH)2、Co(OH)2及少量铁、铝的氧化物等)生产硫酸镍、碳酸钴工艺流程如下图:
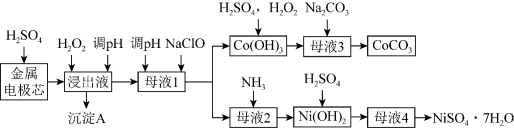
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
回答下列问题:
(1)用硫酸浸取金属电极芯时,提高浸取效率的方法有______ (写出一种合理方法即可),向Co(OH)3中加入H2O2的目的是_______ 。
(2)沉淀A的主要成分是_______ (填化学式),“浸出液”调节pH的范围为________ 。
(3)“母液3”中控制Na2CO3用量使终点pH为9.5,此时c(Co2+)小于________ mol∙L-1(已知:Ksp[Co(OH)2]=1.6×10-15)。
(4)用滴定法测定NiSO4∙7H2O产品中镍元素含量。取2.00g样品,酸溶后配成100mL溶液,取20.00mL于锥形瓶中进行滴定,滴入几滴紫脲酸胺指示剂,用浓度为0.100mol∙L-1的Na2H2Y标准液滴定,重复操作2~3次,消耗Na2H2Y标准液平均值为12.40mL。
已知:i.Ni2++H2Y2-=[NiY]2-+2H+
ii.紫脲酸胺:紫色试剂,遇Ni2+显橙黄色。
①滴定终点的操作和现象是_______ 。
②样品中镍元素的质量分数为_______ %(精确到0.01)。
(5)NiSO4在强碱溶液中和NaClO反应,可制得碱性镍镉电池电极材料NiOOH。该反应的离子方程式为_______ 。

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 离子 | Fe2+ | Fe3+ | Al3+ | Ni2+ | Co2+ |
| 开始沉淀时pH | 6.3 | 1.5 | 3.4 | 6.2 | 7.15 |
| 完全沉淀时pH | 8.3 | 2.8 | 4.7 | 8.9 | 9.15 |
(1)用硫酸浸取金属电极芯时,提高浸取效率的方法有
(2)沉淀A的主要成分是
(3)“母液3”中控制Na2CO3用量使终点pH为9.5,此时c(Co2+)小于
(4)用滴定法测定NiSO4∙7H2O产品中镍元素含量。取2.00g样品,酸溶后配成100mL溶液,取20.00mL于锥形瓶中进行滴定,滴入几滴紫脲酸胺指示剂,用浓度为0.100mol∙L-1的Na2H2Y标准液滴定,重复操作2~3次,消耗Na2H2Y标准液平均值为12.40mL。
已知:i.Ni2++H2Y2-=[NiY]2-+2H+
ii.紫脲酸胺:紫色试剂,遇Ni2+显橙黄色。
①滴定终点的操作和现象是
②样品中镍元素的质量分数为
(5)NiSO4在强碱溶液中和NaClO反应,可制得碱性镍镉电池电极材料NiOOH。该反应的离子方程式为
您最近一年使用:0次
2022-03-18更新
|
843次组卷
|
4卷引用:甘肃省2022届高三第一次高考诊断考试理综化学试题
解题方法
4 . 二氧化氯( ,极易溶于水)消毒泡腾片常用作消毒剂,主要含有亚氯酸钠(
,极易溶于水)消毒泡腾片常用作消毒剂,主要含有亚氯酸钠( )、泡腾剂(
)、泡腾剂( )、固体酸(例如柠檬酸)等成分。当将少量二氧化氯泡腾片投入大量水中时,
)、固体酸(例如柠檬酸)等成分。当将少量二氧化氯泡腾片投入大量水中时, 与酸反应得到亚氯酸(HClO2),亚氯酸分解释放二氧化氯:
与酸反应得到亚氯酸(HClO2),亚氯酸分解释放二氧化氯: ,同时泡腾剂(
,同时泡腾剂( )与酸反应释放
)与酸反应释放 ,加速泡腾片在水中的崩解和溶解,使得泡腾片迅速溶于水,形成低浓度二氧化氯的稀水溶液消毒剂。请回答下列问题:
,加速泡腾片在水中的崩解和溶解,使得泡腾片迅速溶于水,形成低浓度二氧化氯的稀水溶液消毒剂。请回答下列问题:
(1) 中Cl的化合价为
中Cl的化合价为_______ 价, 在水中的电离方程式为
在水中的电离方程式为________ 。
(2)从氧化还原角度分析, 可能具有的性质为
可能具有的性质为________ 。
(3)用上述泡腾片配制 溶液。(已知泡腾片中
溶液。(已知泡腾片中 的质量分数为45.25%)
的质量分数为45.25%)
①需要用托盘天平称取泡腾片的质量为_______ g,亚氯酸分解释放二氧化氯的过程中转移的电子数为_______  。
。
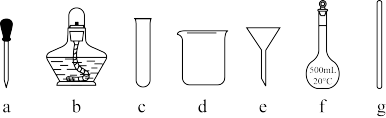
②配制溶液时,除天平(带砝码,最小砝码为1g)、镊子,还缺少的仪器是_______ (填标号)。
③下列操作使配制的 溶液浓度偏低的有
溶液浓度偏低的有________ (填标号)。
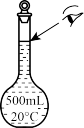
A.称量时,砝码与泡腾片放反了
B.选用的容量瓶内有少量蒸馏水
C.定容摇匀后,液面下降,又加水至刻度线
D.砝码上沾有杂质
E.某同学观察液面的情况如上图所示
(4)已知“有效氯”的含量定义为从KI中氧化出相同量的 所需
所需 的质量与指定化合物的质量之比,常以百分数表示。如纯LiClO的“有效氯”为121%,则
的质量与指定化合物的质量之比,常以百分数表示。如纯LiClO的“有效氯”为121%,则 的“有效氯”为
的“有效氯”为_____ (保留三位有效数字)%。
 ,极易溶于水)消毒泡腾片常用作消毒剂,主要含有亚氯酸钠(
,极易溶于水)消毒泡腾片常用作消毒剂,主要含有亚氯酸钠( )、泡腾剂(
)、泡腾剂( )、固体酸(例如柠檬酸)等成分。当将少量二氧化氯泡腾片投入大量水中时,
)、固体酸(例如柠檬酸)等成分。当将少量二氧化氯泡腾片投入大量水中时, 与酸反应得到亚氯酸(HClO2),亚氯酸分解释放二氧化氯:
与酸反应得到亚氯酸(HClO2),亚氯酸分解释放二氧化氯: ,同时泡腾剂(
,同时泡腾剂( )与酸反应释放
)与酸反应释放 ,加速泡腾片在水中的崩解和溶解,使得泡腾片迅速溶于水,形成低浓度二氧化氯的稀水溶液消毒剂。请回答下列问题:
,加速泡腾片在水中的崩解和溶解,使得泡腾片迅速溶于水,形成低浓度二氧化氯的稀水溶液消毒剂。请回答下列问题:(1)
 中Cl的化合价为
中Cl的化合价为 在水中的电离方程式为
在水中的电离方程式为(2)从氧化还原角度分析,
 可能具有的性质为
可能具有的性质为(3)用上述泡腾片配制
 溶液。(已知泡腾片中
溶液。(已知泡腾片中 的质量分数为45.25%)
的质量分数为45.25%)①需要用托盘天平称取泡腾片的质量为
 。
。②配制溶液时,除天平(带砝码,最小砝码为1g)、镊子,还缺少的仪器是

③下列操作使配制的
 溶液浓度偏低的有
溶液浓度偏低的有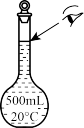
A.称量时,砝码与泡腾片放反了
B.选用的容量瓶内有少量蒸馏水
C.定容摇匀后,液面下降,又加水至刻度线
D.砝码上沾有杂质
E.某同学观察液面的情况如上图所示
(4)已知“有效氯”的含量定义为从KI中氧化出相同量的
 所需
所需 的质量与指定化合物的质量之比,常以百分数表示。如纯LiClO的“有效氯”为121%,则
的质量与指定化合物的质量之比,常以百分数表示。如纯LiClO的“有效氯”为121%,则 的“有效氯”为
的“有效氯”为
您最近一年使用:0次
名校
解题方法
5 . 某校化学研究性学习小组探究足量的镁与浓硫酸反应。回答下列问题:
Ⅰ.甲同学设计如图实验验证该过程产生的混合气体中含有 、
、 。
。
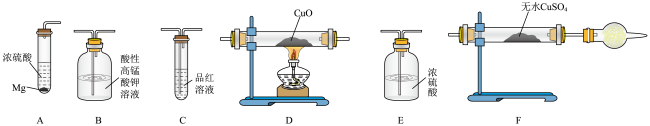
 若按气体从左到右的流向,各装置的连接顺序是
若按气体从左到右的流向,各装置的连接顺序是________  填字母编号
填字母编号 。
。
 已知装置A中浓硫酸的质量分数为90%,密度ρ=1.47g/mL,该浓硫酸的物质的量浓度为
已知装置A中浓硫酸的质量分数为90%,密度ρ=1.47g/mL,该浓硫酸的物质的量浓度为________ mol/L。
 装置C的作用是
装置C的作用是________ 。
 证明混合气体中含有H2的实验现象为
证明混合气体中含有H2的实验现象为________ 。
Ⅱ.乙同学设计如图实验测定混合气体中SO2的含量。
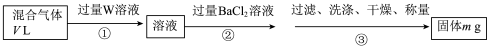
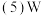 溶液可以是
溶液可以是________  填字母
填字母 。
。
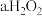 溶液
溶液
 酸性
酸性 溶液
溶液 硫酸酸化
硫酸酸化
 溴水
溴水
 步骤
步骤 中洗涤沉淀的操作为
中洗涤沉淀的操作为________ 。
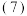 通过的混合气体体积为VL(已换算成标准状况)时,该混合气体中二氧化硫的含量
通过的混合气体体积为VL(已换算成标准状况)时,该混合气体中二氧化硫的含量 体积分数
体积分数 为
为________  用含V、m的代数式表示
用含V、m的代数式表示 。
。
Ⅰ.甲同学设计如图实验验证该过程产生的混合气体中含有
 、
、 。
。
 若按气体从左到右的流向,各装置的连接顺序是
若按气体从左到右的流向,各装置的连接顺序是 填字母编号
填字母编号 。
。 已知装置A中浓硫酸的质量分数为90%,密度ρ=1.47g/mL,该浓硫酸的物质的量浓度为
已知装置A中浓硫酸的质量分数为90%,密度ρ=1.47g/mL,该浓硫酸的物质的量浓度为 装置C的作用是
装置C的作用是 证明混合气体中含有H2的实验现象为
证明混合气体中含有H2的实验现象为Ⅱ.乙同学设计如图实验测定混合气体中SO2的含量。
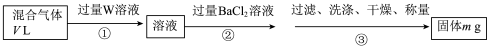
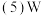 溶液可以是
溶液可以是 填字母
填字母 。
。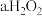 溶液
溶液 酸性
酸性 溶液
溶液 硫酸酸化
硫酸酸化
 溴水
溴水 步骤
步骤 中洗涤沉淀的操作为
中洗涤沉淀的操作为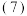 通过的混合气体体积为VL(已换算成标准状况)时,该混合气体中二氧化硫的含量
通过的混合气体体积为VL(已换算成标准状况)时,该混合气体中二氧化硫的含量 体积分数
体积分数 为
为 用含V、m的代数式表示
用含V、m的代数式表示 。
。
您最近一年使用:0次
2020-02-04更新
|
171次组卷
|
2卷引用:甘肃省金昌市永昌县第一高级中学2022-2023学年高三上学期第一次模拟考试化学试题
6 . 高一入学体检时,小明体检的血液化验单中,出现了如图所示的指标。表示该体检指标的物理量是
| 甘油三酯 | 0.52mmol/L |
| 总胆固醇 | 4.27mmol/L |
| 葡萄糖 | 4.95mmol/L |
| A.物质的量浓度 | B.溶解度 | C.质量分数 | D.摩尔质量 |
您最近一年使用:0次
2022-11-25更新
|
193次组卷
|
3卷引用:甘肃省酒泉市玉门油田第一中学2022-2023学年高一上学期期中考试化学(A卷)试题
名校
7 . t ℃时,将a g HCl完全溶于水,得到V mL饱和溶液,该溶液的密度为 ,质量分数为w,其中含
,质量分数为w,其中含 的物质的量为b mol。下列说法不正确的是
的物质的量为b mol。下列说法不正确的是
 ,质量分数为w,其中含
,质量分数为w,其中含 的物质的量为b mol。下列说法不正确的是
的物质的量为b mol。下列说法不正确的是A.t ℃时,HCl的溶解度为 | B.溶液中 |
C.溶质的质量分数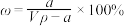 | D.溶质的物质的量浓度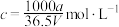 |
您最近一年使用:0次
2022-11-23更新
|
283次组卷
|
2卷引用:甘肃省永昌县第一高级中学2022-2023学年高一上学期期中考试化学试题
8 . 化学与生活、社会发展息息相关,下列说法错误的是
| A.“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应 |
| B.先秦文献《考工记》记录了六类青铜器物的合金成分配比,说明古人已经认识到合金的熔点比纯金属的高 |
| C.《齐民要术》对我国传统的酿造方法有较详细的叙述,酒、醋、酱油等通常是用粮食发酵酿制而成的 |
| D.Cu(OH)2•CuCO3中铜的质量分数高于Cu(OH)2•2CuCO3 |
您最近一年使用:0次
名校
解题方法
9 . 某化学实验室需要 0.8 mol·L-1 硫酸溶液 480 mL。根据溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是____ (填序号),配制上述溶液还需用到的玻璃仪器是____ (填仪器名称)。
A. B.
B.  C.
C.  D.
D. 
(2)现用质量分数为98%、密度为1.84 g·cm-3的浓硫酸来配制480 mL、0.8 mol·L-1 的稀硫酸。计算所需浓硫酸的体积为____ mL(保留 1 位小数)。
(3)配制时,一般可分为以下几个步骤:
①量取②计算③稀释④摇匀⑤转移并摇动⑥洗涤并转移⑦定容⑧冷却
其正确的操作顺序为:②→①→③→___________ →___________→___________→___________→④(填序号)。
(4)下列操作能引起浓度偏小的有___________ (填序号)。
①洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中
②量筒量取浓硫酸时俯视读数
③转移前,容量瓶先用蒸馏水清洗
④定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
⑤定容时,仰视刻度线
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至刻度线
(1)如图所示的仪器中配制溶液肯定不需要的是
A.
 B.
B.  C.
C.  D.
D. 
(2)现用质量分数为98%、密度为1.84 g·cm-3的浓硫酸来配制480 mL、0.8 mol·L-1 的稀硫酸。计算所需浓硫酸的体积为
(3)配制时,一般可分为以下几个步骤:
①量取②计算③稀释④摇匀⑤转移并摇动⑥洗涤并转移⑦定容⑧冷却
其正确的操作顺序为:②→①→③→
(4)下列操作能引起浓度偏小的有
①洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中
②量筒量取浓硫酸时俯视读数
③转移前,容量瓶先用蒸馏水清洗
④定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
⑤定容时,仰视刻度线
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至刻度线
您最近一年使用:0次
名校
10 . 回答下列问题:
(1)3.01×1023个OH-的物质的量是___________ ,含有电子___________ 个;
(2)在标准状况下,CO和CO2混合气体的质量为36 g,体积为22.4 L,则其中 CO2所占的体积为___________ ,CO所占的质量为___________ 。
(3)质量分数为36.5%浓盐酸(密度为1.25 g·mL-1)的物质的量浓度为___________ ,若配制 250 mL0.1 mol·L-1 的盐酸,需要量取浓盐酸的体积为___________ mL。
(4)某无土栽培用的营养液,要求KCl、K2SO4和NH4Cl三种固体原料的物质的量之比为 1:4:8。
①配制该营养液后 c( )=0.016 mol/L,溶液中 c(K+)=
)=0.016 mol/L,溶液中 c(K+)=___________ 。
②若采用(NH4)2SO4和KCl来配制该营养液,则(NH4)2SO4和KCl物质的量之比为_____ 。
(1)3.01×1023个OH-的物质的量是
(2)在标准状况下,CO和CO2混合气体的质量为36 g,体积为22.4 L,则其中 CO2所占的体积为
(3)质量分数为36.5%浓盐酸(密度为1.25 g·mL-1)的物质的量浓度为
(4)某无土栽培用的营养液,要求KCl、K2SO4和NH4Cl三种固体原料的物质的量之比为 1:4:8。
①配制该营养液后 c(
 )=0.016 mol/L,溶液中 c(K+)=
)=0.016 mol/L,溶液中 c(K+)=②若采用(NH4)2SO4和KCl来配制该营养液,则(NH4)2SO4和KCl物质的量之比为
您最近一年使用:0次
2022-10-11更新
|
386次组卷
|
2卷引用:甘肃省高台县第一中学2022-2023学年高一上学期10月月考化学试题



