解题方法
1 . 能正确表示下列反应的离子方程式为
A.明矾溶液与过量氨水混合: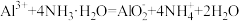 |
| B.氯水久置颜色逐渐褪去:4Cl2+4H2O = HClO4+7HCl |
C.用Na2S2O3做碘量法实验时,pH过低溶液变浑浊: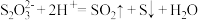 |
D.苯酚钠溶液中通入少量CO2,出现白色浑浊:2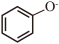 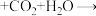 2 2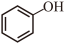 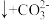 |
您最近一年使用:0次
2 . 臭氧能氧化CN-,故常被用来治理电镀工业中的含氰废水,其化学反应原理为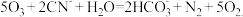 下列说法正确的是
下列说法正确的是
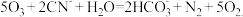 下列说法正确的是
下列说法正确的是| A.O3和O2互为同位素关系 |
| B.该反应是熵减的过程 |
| C.该反应中,每生成1 mol N2转移6 mol电子 |
| D.反应中所涉及的N2、O2为非极性分子,O3为极性分子 |
您最近一年使用:0次
3 . 下列化学用语使用正确的是
A.甲胺的电子式: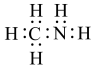 |
B.顺-2-丁烯的结构简式: |
C. 的VSEPR模型: 的VSEPR模型: |
D.基态Fe的价层电子排布式为: |
您最近一年使用:0次
解题方法
4 . 氧缺位体(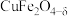 )是热化学循环分解水制氢的催化剂。一种以黄铜矿(主要成分是
)是热化学循环分解水制氢的催化剂。一种以黄铜矿(主要成分是 ,含
,含 、
、 等杂质)为原料制备
等杂质)为原料制备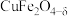 的流程如下:
的流程如下:
①酸浸后溶液中的金属离子有 、
、 、
、 和
和
②25°℃时已知几种金属离子沉淀的 如表所示:
如表所示:
回答下列问题:
(1) 位于元素周期表
位于元素周期表___________ 区。
(2) “焙烧”时生成三种氧化物(其中
“焙烧”时生成三种氧化物(其中 的氧化物形式为
的氧化物形式为 ),其化学方程式为
),其化学方程式为___________ 。
(3)加 “还原”的目的是
“还原”的目的是___________ 。
(4)滤渣2的主要成分为___________ 。
(5)已知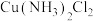 C有两种同分异构体,则“沉铁”过程中生成的
C有两种同分异构体,则“沉铁”过程中生成的 的空间构型是
的空间构型是___________ 。
(6)充分“煅烧”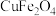 得到的氧缺位体(
得到的氧缺位体(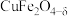 )的质量为原质量的98%,则
)的质量为原质量的98%,则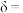
___________ 。
(7)氧缺位体分解水制氢分两步:
第一步___________ (完成方程式);
第二步: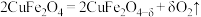 。
。
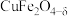 )是热化学循环分解水制氢的催化剂。一种以黄铜矿(主要成分是
)是热化学循环分解水制氢的催化剂。一种以黄铜矿(主要成分是 ,含
,含 、
、 等杂质)为原料制备
等杂质)为原料制备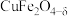 的流程如下:
的流程如下: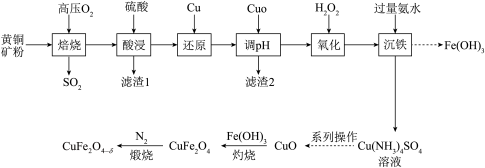
①酸浸后溶液中的金属离子有
 、
、 、
、 和
和
②25°℃时已知几种金属离子沉淀的
 如表所示:
如表所示:| 金属氢氧化物 |  |  |  |  |
开始沉淀的 | 1.9 | 3.4 | 6.4 | 7.0 |
完全沉淀的 | 3.2 | 4.7 | 7.6 | 9.0 |
(1)
 位于元素周期表
位于元素周期表(2)
 “焙烧”时生成三种氧化物(其中
“焙烧”时生成三种氧化物(其中 的氧化物形式为
的氧化物形式为 ),其化学方程式为
),其化学方程式为(3)加
 “还原”的目的是
“还原”的目的是(4)滤渣2的主要成分为
(5)已知
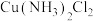 C有两种同分异构体,则“沉铁”过程中生成的
C有两种同分异构体,则“沉铁”过程中生成的 的空间构型是
的空间构型是(6)充分“煅烧”
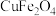 得到的氧缺位体(
得到的氧缺位体(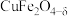 )的质量为原质量的98%,则
)的质量为原质量的98%,则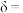
(7)氧缺位体分解水制氢分两步:
第一步
第二步:
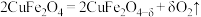 。
。
您最近一年使用:0次
5 . 三氯乙醛( )是一种易挥发的油状液体,溶于水和乙醇,沸点为97.7℃,可用于生产氯霉素、合霉素等。某小组在实验室模拟制备三氯乙醛并探究其性质(实验装置如图所示,夹持、加热装置均略去)。
)是一种易挥发的油状液体,溶于水和乙醇,沸点为97.7℃,可用于生产氯霉素、合霉素等。某小组在实验室模拟制备三氯乙醛并探究其性质(实验装置如图所示,夹持、加热装置均略去)。
①制备反应原理为: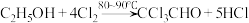 ,
,
②可能发生的副反应为: 。
。
③反应得到含三氯乙醛的混合物,再与浓硫酸反应,经蒸馏分离出三氯乙醛。回答下列问题:
(1) 中碳原子的杂化方式为
中碳原子的杂化方式为___________ 。
(2)a仪器的名称为___________ 。
(3)写出装置A中发生反应的离子方程式___________ 。
(4)进入装置D的是纯净、干燥的 ,若撤去装置B,对实验的影响是
,若撤去装置B,对实验的影响是___________ 。
(5)装置D的加热方式为___________ 。
(6)能作为E中装置的是___________ (填序号)。
① (硫酸氢乙酯,沸点:280℃)
(硫酸氢乙酯,沸点:280℃) ;
;
②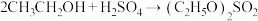 (硫酸二乙酯,沸点:209℃)
(硫酸二乙酯,沸点:209℃) 。
。
(8)蒸馏时,在粗产品中加入浓硫酸的目的是___________ 。
(9)探究 的性质:向溴水中滴加三氯乙醛,振荡,溶液褪色。经检验,反应后溶液的
的性质:向溴水中滴加三氯乙醛,振荡,溶液褪色。经检验,反应后溶液的 明显减小。写出三氯乙醛与溴水反应的化学方程式
明显减小。写出三氯乙醛与溴水反应的化学方程式___________ 。
 )是一种易挥发的油状液体,溶于水和乙醇,沸点为97.7℃,可用于生产氯霉素、合霉素等。某小组在实验室模拟制备三氯乙醛并探究其性质(实验装置如图所示,夹持、加热装置均略去)。
)是一种易挥发的油状液体,溶于水和乙醇,沸点为97.7℃,可用于生产氯霉素、合霉素等。某小组在实验室模拟制备三氯乙醛并探究其性质(实验装置如图所示,夹持、加热装置均略去)。
①制备反应原理为:
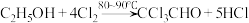 ,
,②可能发生的副反应为:
 。
。③反应得到含三氯乙醛的混合物,再与浓硫酸反应,经蒸馏分离出三氯乙醛。回答下列问题:
(1)
 中碳原子的杂化方式为
中碳原子的杂化方式为(2)a仪器的名称为
(3)写出装置A中发生反应的离子方程式
(4)进入装置D的是纯净、干燥的
 ,若撤去装置B,对实验的影响是
,若撤去装置B,对实验的影响是(5)装置D的加热方式为
(6)能作为E中装置的是
a.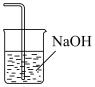 b.
b.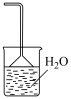 c.
c.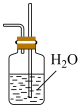 d.
d.

①
 (硫酸氢乙酯,沸点:280℃)
(硫酸氢乙酯,沸点:280℃) ;
;②
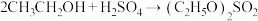 (硫酸二乙酯,沸点:209℃)
(硫酸二乙酯,沸点:209℃) 。
。(8)蒸馏时,在粗产品中加入浓硫酸的目的是
(9)探究
 的性质:向溴水中滴加三氯乙醛,振荡,溶液褪色。经检验,反应后溶液的
的性质:向溴水中滴加三氯乙醛,振荡,溶液褪色。经检验,反应后溶液的 明显减小。写出三氯乙醛与溴水反应的化学方程式
明显减小。写出三氯乙醛与溴水反应的化学方程式
您最近一年使用:0次
6 . 中国“大国重器”频频问世,彰显了中国科技发展的巨大成就。下列有关说法正确的是
| A.“天问一号”火星车的保温材料为纳米气凝胶,能产生丁达尔效应 |
| B.“梦天实验舱”原子钟利用电子跃迁计时,工作时发生化学变化 |
| C.中国天眼发现纳赫兹引力波,其使用的碳化硅材料为有机高分子材料 |
| D.“嫦娥五号”使用的锂离子电池组和太阳能电池阵,均可将化学能转变成电能 |
您最近一年使用:0次
7 . 下列化学用语或表述正确的是
A.基态氧原子的价层轨道表示式: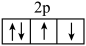 |
B. 的VSEPR模型: 的VSEPR模型: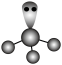 |
C.四氯乙烯的空间填充模型: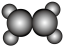 |
D.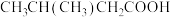 系统命名法名称为:2—甲基丁酸 系统命名法名称为:2—甲基丁酸 |
您最近一年使用:0次
2024-05-14更新
|
176次组卷
|
2卷引用:2024届东北三省四市教研联合体高三下学期高考模拟(二)化学试卷
解题方法
8 . 2023 年诺贝尔化学奖授予发现量子点的三位科学家,量子点的尺寸一般在1 nm~10 nm之间,是一种纳米级别的半导体。量子点的尺寸不同,则发光颜色不同,吸收光谱波长不同。实验室一种制备CdSe量子点的方法如下:
一、CdSe量子点前驱体的制备
Ⅰ.N2气氛中,取1 mmol Se粉于三颈烧瓶中,加入15 mL的十八烯溶剂,加热到280℃,Se粉完全溶解形成橙色透明溶液;
Ⅱ.N2气氛中,将1 mmol CdCl2溶于4 mL油酸,加热至120℃,使CdCl2完全溶于油酸,形成油酸镉澄清液体。
二、CdSe量子点的生长与制备
Ⅲ.将步骤Ⅱ中制备好的油酸镉溶液注射至步骤Ⅰ中含有Se粉的三颈烧瓶中,如下图所示,保持反应温度为260℃,反应45min。
Ⅳ.待反应液冷却后,加入20 mL乙醇溶液,CdSe析出,离心分离,加入正己烷分散后,再次加入乙醇,离心分离,重复2~3次后,用乙醇和丙酮洗涤 CdSe,即可得到干净的CdSe量子点。
回答下列问题:
(1)Cd为第五周期ⅡB族,则Cd的价层电子排布式为___________ 。
(2)步骤Ⅱ中N2的作用为___________ ,油酸与镉配位的原子为___________ 。
(3)Se的一种制备方法如下:向Na2SeO3水溶液中加入 进行还原,得Se单质,过滤,洗涤,干燥,静置。制备过程中,会产生一种对环境无污染的气体,则该反应的离子方程式为
进行还原,得Se单质,过滤,洗涤,干燥,静置。制备过程中,会产生一种对环境无污染的气体,则该反应的离子方程式为___________ ;此方法获得Se单质过程中无需使用的仪器是___________ (填名称)。___________ 现象时,证明CdSe量子点生长基本停止,制备完成。除此方法外,还可利用___________ 物理现象初步鉴定CdSe量子点制备成功。
(5)步骤Ⅳ中加入20 mL乙醇的作用是___________ 。
(6)CdSe洗涤干净的标志是___________ 。
一、CdSe量子点前驱体的制备
Ⅰ.N2气氛中,取1 mmol Se粉于三颈烧瓶中,加入15 mL的十八烯溶剂,加热到280℃,Se粉完全溶解形成橙色透明溶液;
Ⅱ.N2气氛中,将1 mmol CdCl2溶于4 mL油酸,加热至120℃,使CdCl2完全溶于油酸,形成油酸镉澄清液体。
二、CdSe量子点的生长与制备
Ⅲ.将步骤Ⅱ中制备好的油酸镉溶液注射至步骤Ⅰ中含有Se粉的三颈烧瓶中,如下图所示,保持反应温度为260℃,反应45min。
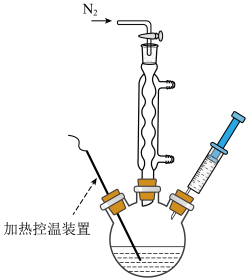
Ⅳ.待反应液冷却后,加入20 mL乙醇溶液,CdSe析出,离心分离,加入正己烷分散后,再次加入乙醇,离心分离,重复2~3次后,用乙醇和丙酮洗涤 CdSe,即可得到干净的CdSe量子点。
回答下列问题:
(1)Cd为第五周期ⅡB族,则Cd的价层电子排布式为
(2)步骤Ⅱ中N2的作用为
(3)Se的一种制备方法如下:向Na2SeO3水溶液中加入
 进行还原,得Se单质,过滤,洗涤,干燥,静置。制备过程中,会产生一种对环境无污染的气体,则该反应的离子方程式为
进行还原,得Se单质,过滤,洗涤,干燥,静置。制备过程中,会产生一种对环境无污染的气体,则该反应的离子方程式为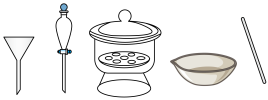
(5)步骤Ⅳ中加入20 mL乙醇的作用是
(6)CdSe洗涤干净的标志是
您最近一年使用:0次
2024-05-13更新
|
123次组卷
|
2卷引用:2024届东北三省四市教研联合体高三下学期高考模拟(二)化学试卷
9 .  为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.1 mol羟基(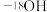 )中所含有的中子数为 )中所含有的中子数为 |
B.常温下,2.7 g Al片与足量浓硝酸反应转移的电子数为0.3 |
C.标准状况下,448 mL 与水反应转移电子数为0.02 与水反应转移电子数为0.02 |
D.常温下,1 L0.1 mol/L 溶液中含 溶液中含 的数目为0.1 的数目为0.1 |
您最近一年使用:0次
2024-05-13更新
|
133次组卷
|
2卷引用:2024届东北三省四市教研联合体高三下学期高考模拟(二)化学试卷
10 . 下列化学用语正确的是
A.正丁烷的结构式: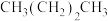 |
B.2—甲基丁烷的键线式为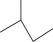 |
C.羟基的电子式: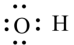 |
D.乙烯的结构简式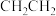 |
您最近一年使用:0次



