解题方法
1 . 2023 年诺贝尔化学奖授予发现量子点的三位科学家,量子点的尺寸一般在1 nm~10 nm之间,是一种纳米级别的半导体。量子点的尺寸不同,则发光颜色不同,吸收光谱波长不同。实验室一种制备CdSe量子点的方法如下:
一、CdSe量子点前驱体的制备
Ⅰ.N2气氛中,取1 mmol Se粉于三颈烧瓶中,加入15 mL的十八烯溶剂,加热到280℃,Se粉完全溶解形成橙色透明溶液;
Ⅱ.N2气氛中,将1 mmol CdCl2溶于4 mL油酸,加热至120℃,使CdCl2完全溶于油酸,形成油酸镉澄清液体。
二、CdSe量子点的生长与制备
Ⅲ.将步骤Ⅱ中制备好的油酸镉溶液注射至步骤Ⅰ中含有Se粉的三颈烧瓶中,如下图所示,保持反应温度为260℃,反应45min。
Ⅳ.待反应液冷却后,加入20 mL乙醇溶液,CdSe析出,离心分离,加入正己烷分散后,再次加入乙醇,离心分离,重复2~3次后,用乙醇和丙酮洗涤 CdSe,即可得到干净的CdSe量子点。
回答下列问题:
(1)Cd为第五周期ⅡB族,则Cd的价层电子排布式为___________ 。
(2)步骤Ⅱ中N2的作用为___________ ,油酸与镉配位的原子为___________ 。
(3)Se的一种制备方法如下:向Na2SeO3水溶液中加入 进行还原,得Se单质,过滤,洗涤,干燥,静置。制备过程中,会产生一种对环境无污染的气体,则该反应的离子方程式为
进行还原,得Se单质,过滤,洗涤,干燥,静置。制备过程中,会产生一种对环境无污染的气体,则该反应的离子方程式为___________ ;此方法获得Se单质过程中无需使用的仪器是___________ (填名称)。___________ 现象时,证明CdSe量子点生长基本停止,制备完成。除此方法外,还可利用___________ 物理现象初步鉴定CdSe量子点制备成功。
(5)步骤Ⅳ中加入20 mL乙醇的作用是___________ 。
(6)CdSe洗涤干净的标志是___________ 。
一、CdSe量子点前驱体的制备
Ⅰ.N2气氛中,取1 mmol Se粉于三颈烧瓶中,加入15 mL的十八烯溶剂,加热到280℃,Se粉完全溶解形成橙色透明溶液;
Ⅱ.N2气氛中,将1 mmol CdCl2溶于4 mL油酸,加热至120℃,使CdCl2完全溶于油酸,形成油酸镉澄清液体。
二、CdSe量子点的生长与制备
Ⅲ.将步骤Ⅱ中制备好的油酸镉溶液注射至步骤Ⅰ中含有Se粉的三颈烧瓶中,如下图所示,保持反应温度为260℃,反应45min。
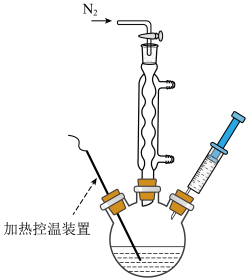
Ⅳ.待反应液冷却后,加入20 mL乙醇溶液,CdSe析出,离心分离,加入正己烷分散后,再次加入乙醇,离心分离,重复2~3次后,用乙醇和丙酮洗涤 CdSe,即可得到干净的CdSe量子点。
回答下列问题:
(1)Cd为第五周期ⅡB族,则Cd的价层电子排布式为
(2)步骤Ⅱ中N2的作用为
(3)Se的一种制备方法如下:向Na2SeO3水溶液中加入
 进行还原,得Se单质,过滤,洗涤,干燥,静置。制备过程中,会产生一种对环境无污染的气体,则该反应的离子方程式为
进行还原,得Se单质,过滤,洗涤,干燥,静置。制备过程中,会产生一种对环境无污染的气体,则该反应的离子方程式为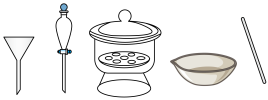
(5)步骤Ⅳ中加入20 mL乙醇的作用是
(6)CdSe洗涤干净的标志是
您最近半年使用:0次
昨日更新
|
8次组卷
|
2卷引用:2024届东北三省四市教研联合体高三下学期高考模拟(二)化学试卷
2 .  为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.1 mol羟基(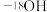 )中所含有的中子数为 )中所含有的中子数为 |
B.常温下,2.7 g Al片与足量浓硝酸反应转移的电子数为0.3 |
C.标准状况下,448 mL 与水反应转移电子数为0.02 与水反应转移电子数为0.02 |
D.常温下,1 L0.1 mol/L 溶液中含 溶液中含 的数目为0.1 的数目为0.1 |
您最近半年使用:0次
昨日更新
|
16次组卷
|
2卷引用:2024届东北三省四市教研联合体高三下学期高考模拟(二)化学试卷
3 . 下列化学用语正确的是
A.正丁烷的结构式: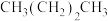 |
B.2—甲基丁烷的键线式为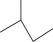 |
C.羟基的电子式: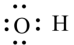 |
D.乙烯的结构简式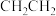 |
您最近半年使用:0次
名校
4 . 火药的发明推进了人类历史发展的进程。火药爆炸的原理为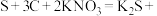
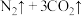 。下列说法错误的是
。下列说法错误的是
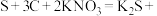
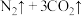 。下列说法错误的是
。下列说法错误的是A.从得失电子角度看,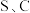 在反应中的作用不同 在反应中的作用不同 |
B.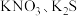 均属于钾盐 均属于钾盐 |
| C.该反应过程属于氮的固定 |
D.该反应每转移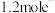 ,生成标准状况下 ,生成标准状况下 气体 气体 |
您最近半年使用:0次
7日内更新
|
65次组卷
|
2卷引用:吉林省白山市抚松县第一中学2023-2024学年高一下学期4月月考化学试题
名校
5 . 加热NH4Cl与MgO的固体混合物制备无水MgCl2,起始物质的量之比为3∶1,升温,从200℃开始有MgCl2生成,同时生成副产物Mg(OH)Cl。混合物中NH4Cl与MgO的质量分数 随温度的变化如图所示。已知:200℃时测得:
随温度的变化如图所示。已知:200℃时测得: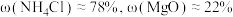 。
。
 随温度的变化如图所示。已知:200℃时测得:
随温度的变化如图所示。已知:200℃时测得: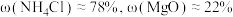 。
。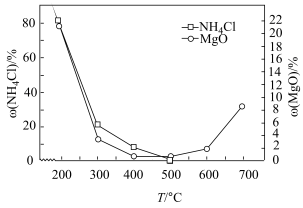
| A.200℃之前体系中没发生化学反应 |
B.200~400℃时体系中存在反应: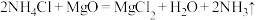 |
C.加热 与 与 的混合物可制备 的混合物可制备 ,原因之一是 ,原因之一是 可抑制 可抑制 转化为 转化为 和 和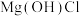 |
D.控制温度400℃,增大投料比 ,并使二者充分接触,利于提高 ,并使二者充分接触,利于提高 的产率 的产率 |
您最近半年使用:0次
6 . 利用水钴矿(主要成分为 ,含少量
,含少量 )制备二次电池添加剂
)制备二次电池添加剂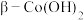 的流程如下。
的流程如下。 在碱性溶液中易被
在碱性溶液中易被 氧化。
氧化。
ii.部分金属离子浓度 与
与 的关系如图所示。
的关系如图所示。
(1)“酸浸”中 反应的离子方程式为
反应的离子方程式为___________ 。
(2)设“酸浸”后溶液中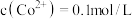 ,则“沉铁”中控制
,则“沉铁”中控制 的理论范围为
的理论范围为___________ (溶液中离子浓度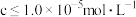 时,可认为已除尽)。
时,可认为已除尽)。
(3)萃取剂对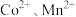 萃取率随
萃取率随 的影响如图,应选择萃取剂
的影响如图,应选择萃取剂___________ (填“M”或“N”)。(若萃取剂的量一定时,___________ (填“一次萃取”或“少量多次萃取”)的萃取效率更高。 的离子方程式为
的离子方程式为___________ 。
(5)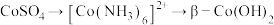 过程中,先加氨水再缓慢加
过程中,先加氨水再缓慢加 溶液的理由是
溶液的理由是___________ 。“沉钴”中使用热 溶液的目的是
溶液的目的是___________ 。
 ,含少量
,含少量 )制备二次电池添加剂
)制备二次电池添加剂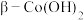 的流程如下。
的流程如下。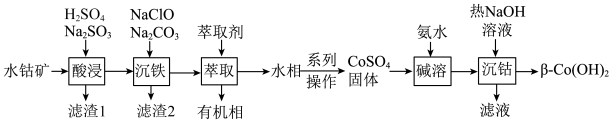
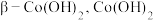 在碱性溶液中易被
在碱性溶液中易被 氧化。
氧化。ii.部分金属离子浓度
 与
与 的关系如图所示。
的关系如图所示。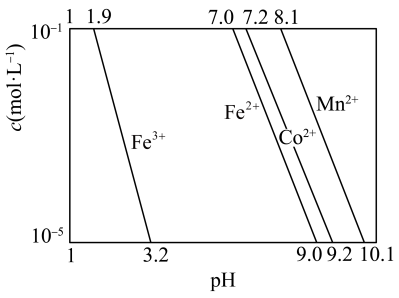
(1)“酸浸”中
 反应的离子方程式为
反应的离子方程式为(2)设“酸浸”后溶液中
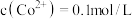 ,则“沉铁”中控制
,则“沉铁”中控制 的理论范围为
的理论范围为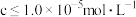 时,可认为已除尽)。
时,可认为已除尽)。(3)萃取剂对
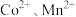 萃取率随
萃取率随 的影响如图,应选择萃取剂
的影响如图,应选择萃取剂
 的离子方程式为
的离子方程式为(5)
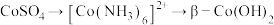 过程中,先加氨水再缓慢加
过程中,先加氨水再缓慢加 溶液的理由是
溶液的理由是 溶液的目的是
溶液的目的是
您最近半年使用:0次
名校
解题方法
7 . 1962年化学家N.Bartlett基于以下两点合成了第一个含有化学键的“惰性气体”化合物——登黄色固体配合物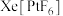 。
。
①一个现象: 能够氧化
能够氧化 生成
生成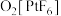 。
。
②一个事实: 的电离能
的电离能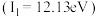 与
与 的电离能
的电离能 相近。
相近。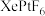 不溶于
不溶于 ,遇水则迅速分解,并放出气体:
,遇水则迅速分解,并放出气体: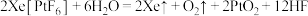 。
。
以 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是
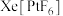 。
。①一个现象:
 能够氧化
能够氧化 生成
生成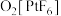 。
。②一个事实:
 的电离能
的电离能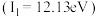 与
与 的电离能
的电离能 相近。
相近。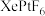 不溶于
不溶于 ,遇水则迅速分解,并放出气体:
,遇水则迅速分解,并放出气体: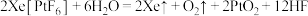 。
。以
 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是A.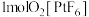 固体中阳离子含有的电子数为 固体中阳离子含有的电子数为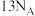 |
B. 中,含有 中,含有 键数为 键数为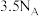 |
C.反应产生 (标况) (标况) ,转移的电子数为 ,转移的电子数为 |
D. 固体中中阴阳离子数共有 固体中中阴阳离子数共有 |
您最近半年使用:0次
名校
解题方法
8 . 下列有关海水综合利用涉及的离子方程式不正确的是
A.利用石灰乳沉镁: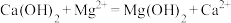 |
B.利用 溶液反萃取 溶液反萃取 中的 中的 : :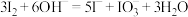 |
C.利用 吸收 吸收 二次富集溴: 二次富集溴: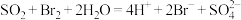 |
D.电解饱和食盐水: |
您最近半年使用:0次
名校
解题方法
9 . 能正确表示下列反应的离子方程式的是
A.少量 气体通入次氯酸钠溶液中: 气体通入次氯酸钠溶液中: |
B.向氢硫酸中通入氯气: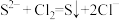 |
C.Fe和足量稀 的反应: 的反应: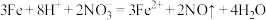 |
D.实验室用氯化铵和熟石灰制氨: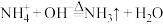 |
您最近半年使用:0次
10 . 下列化学用语或图示表达正确的是
A.HCl中σ键的电子云轮廓图为: |
| B.非极性分子O3的结构式:O=O=O |
C.乙炔的电子式: |
| D.Cr3+的价层电子排布式:3d3 |
您最近半年使用:0次



