名校
1 . 某同学为测定 和
和 混合粉末中
混合粉末中 的含量。将
的含量。将 和
和 混合粉末加入
混合粉末加入 的稀硝酸中,得到
的稀硝酸中,得到 气体
气体 (标准状况下),忽略溶液体积的变化。下列有关说法正确的是
(标准状况下),忽略溶液体积的变化。下列有关说法正确的是
 和
和 混合粉末中
混合粉末中 的含量。将
的含量。将 和
和 混合粉末加入
混合粉末加入 的稀硝酸中,得到
的稀硝酸中,得到 气体
气体 (标准状况下),忽略溶液体积的变化。下列有关说法正确的是
(标准状况下),忽略溶液体积的变化。下列有关说法正确的是| A.反应后有固体剩余 | B.反应后的溶液中 |
C. 单质在混合粉末中的质量分数约为 单质在混合粉末中的质量分数约为 | D.在反应后的溶液中加入足量铁粉,可畳换出 |
您最近一年使用:0次
2024-04-28更新
|
119次组卷
|
2卷引用:吉林省白山市抚松县第一中学2023-2024学年高一下学期4月月考化学试题
名校
2 . 水合肼(N2H4•H2O)是一种无色透明、具有腐蚀性和强还原性的碱性液体,它是一种重要的化工试剂。利用尿素法生产水合肼的原理为CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4•H2O+NaCl。回答下列问题:
实验一:制备NaClO溶液(实验装置如图所示)

(1)配制100mL10mol•L﹣1的NaOH溶液时,所需玻璃仪器除量筒外还有___________ (填字母)。
A.玻璃棒 B.烧杯 C.100mL容量瓶 D.干燥管 E.胶头滴管 F.锥形瓶
(2)装置M的作用是___________ 。
实验二:制取水合肼(实验装置如图所示)

(3)①仪器A的名称为___________ ,冷凝管的水流方向为 ___________ 。(用“a、b”作答)
②反应过程中需控制反应温度,同时将A中溶液缓慢滴入三颈烧瓶中,如果滴速过快则会导致产品产率降低,写出该过程的化学方程式:___________ ,A中盛装的溶液是 ___________ (填字母)。
A.CO(NH2)2溶液 B.NaOH和NaClO溶液
③充分反应后,加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分
实验三:测定馏分中水合肼含量
(4)称取馏分5.0g,加入适量NaHCO3固体,加水配成250mL溶液,取25.00mL该溶液置于锥形瓶中,用0.10mol•L﹣1的I2溶液滴定。滴定过程中,溶液的pH保持在6.5左右。(已知:N2H4•H2O+2I2=N2↑+4HI+H2O)
①滴定时,碘的标准溶液盛放在___________ (填“酸式”或“碱式”)滴定管中,本实验滴定终点的现象为 ___________ 。
②实验测得消耗I2溶液的平均值为18.00mL,馏分中水合肼(N2H4•H2O)的质量分数为___________ 。
实验一:制备NaClO溶液(实验装置如图所示)

(1)配制100mL10mol•L﹣1的NaOH溶液时,所需玻璃仪器除量筒外还有
A.玻璃棒 B.烧杯 C.100mL容量瓶 D.干燥管 E.胶头滴管 F.锥形瓶
(2)装置M的作用是
实验二:制取水合肼(实验装置如图所示)

(3)①仪器A的名称为
②反应过程中需控制反应温度,同时将A中溶液缓慢滴入三颈烧瓶中,如果滴速过快则会导致产品产率降低,写出该过程的化学方程式:
A.CO(NH2)2溶液 B.NaOH和NaClO溶液
③充分反应后,加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分
实验三:测定馏分中水合肼含量
(4)称取馏分5.0g,加入适量NaHCO3固体,加水配成250mL溶液,取25.00mL该溶液置于锥形瓶中,用0.10mol•L﹣1的I2溶液滴定。滴定过程中,溶液的pH保持在6.5左右。(已知:N2H4•H2O+2I2=N2↑+4HI+H2O)
①滴定时,碘的标准溶液盛放在
②实验测得消耗I2溶液的平均值为18.00mL,馏分中水合肼(N2H4•H2O)的质量分数为
您最近一年使用:0次
名校
3 . 维生素C是一种水溶性维生素,有强还原性、水溶液显酸性。化学式为 。某小组同学测定了某新鲜水果中维生素C的含量,实验报告如下:
。某小组同学测定了某新鲜水果中维生素C的含量,实验报告如下:
【实验目的】测定某新鲜水果中维生素C的含量。
【实验原理】 ,
,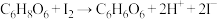 。
。
【实验用品】 标准溶液、指示剂、
标准溶液、指示剂、 溶液、
溶液、 溶液、蒸馏水等。
溶液、蒸馏水等。
【实验步骤】
(1)配制待测溶液:称取新鲜水果样品 ,加入适量蒸馏水进行粉碎、过滤,并将滤液转移至
,加入适量蒸馏水进行粉碎、过滤,并将滤液转移至 容量瓶中,定容,随后将待测溶液加到滴定管中。根据维生素C的性质,待测溶液应用
容量瓶中,定容,随后将待测溶液加到滴定管中。根据维生素C的性质,待测溶液应用___________ (填“酸式”或“碱式”)滴定管盛装。
(2)氧化还原滴定法:取(1)中配制好的待测溶液 于锥形瓶中,调节
于锥形瓶中,调节 至3,加入适量指示剂后,小心地滴入
至3,加入适量指示剂后,小心地滴入 标准溶液,直至滴定终点,记录相关数据。平行测定三次,计算新鲜水果中维生素
标准溶液,直至滴定终点,记录相关数据。平行测定三次,计算新鲜水果中维生素 的质量分数。
的质量分数。
①上述氧化还原滴定法应用___________ 作指示剂,滴定终点的现象为___________ 。
②除了样品的质量、待测溶液的体积外,计算新鲜水果中维生素C的质量分数还需要的数据有___________ 。
(3)库仑滴定法:取(1)中配制好的待测溶液 ,用库仑仪测定其中维生素C的含量。平行测定三次,计算新鲜水果中维生素C的质量分数。
,用库仑仪测定其中维生素C的含量。平行测定三次,计算新鲜水果中维生素C的质量分数。
已知:库仑仪中电解原理示意图如下。检测前,电解质溶液中 保持定值时,电解池不工作。将待测溶液加入电解池后,维生素C将
保持定值时,电解池不工作。将待测溶液加入电解池后,维生素C将 还原,库仑仪便立即自动进行电解到
还原,库仑仪便立即自动进行电解到 又回到原定值,测定结束,通过测定电解消托的电量可以求得维生素C的含量。
又回到原定值,测定结束,通过测定电解消托的电量可以求得维生素C的含量。

①库仑仪工作时电解池的阳极反应式为___________ 。
②若电解消耗的电量为Q库仑,维生素C的摩尔质量为 ,则新鲜水果中维生素C的质量分数为
,则新鲜水果中维生素C的质量分数为___________ 。(用含 的代数式表示)已知:电解中转移
的代数式表示)已知:电解中转移 电子所消耗的电量为96500库仑。
电子所消耗的电量为96500库仑。
③测定过程中,需控制电解质溶液 ,当
,当 时,部分
时,部分 易被空气中的
易被空气中的 直接氧化为
直接氧化为 ,该过程的离子方程式为
,该过程的离子方程式为___________ 。这部分非电解生成的 ;将导致测得的维生素C的含量
;将导致测得的维生素C的含量___________ 。(填“偏大”或“偏小”)。
 。某小组同学测定了某新鲜水果中维生素C的含量,实验报告如下:
。某小组同学测定了某新鲜水果中维生素C的含量,实验报告如下:【实验目的】测定某新鲜水果中维生素C的含量。
【实验原理】
 ,
,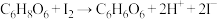 。
。【实验用品】
 标准溶液、指示剂、
标准溶液、指示剂、 溶液、
溶液、 溶液、蒸馏水等。
溶液、蒸馏水等。【实验步骤】
(1)配制待测溶液:称取新鲜水果样品
 ,加入适量蒸馏水进行粉碎、过滤,并将滤液转移至
,加入适量蒸馏水进行粉碎、过滤,并将滤液转移至 容量瓶中,定容,随后将待测溶液加到滴定管中。根据维生素C的性质,待测溶液应用
容量瓶中,定容,随后将待测溶液加到滴定管中。根据维生素C的性质,待测溶液应用(2)氧化还原滴定法:取(1)中配制好的待测溶液
 于锥形瓶中,调节
于锥形瓶中,调节 至3,加入适量指示剂后,小心地滴入
至3,加入适量指示剂后,小心地滴入 标准溶液,直至滴定终点,记录相关数据。平行测定三次,计算新鲜水果中维生素
标准溶液,直至滴定终点,记录相关数据。平行测定三次,计算新鲜水果中维生素 的质量分数。
的质量分数。①上述氧化还原滴定法应用
②除了样品的质量、待测溶液的体积外,计算新鲜水果中维生素C的质量分数还需要的数据有
(3)库仑滴定法:取(1)中配制好的待测溶液
 ,用库仑仪测定其中维生素C的含量。平行测定三次,计算新鲜水果中维生素C的质量分数。
,用库仑仪测定其中维生素C的含量。平行测定三次,计算新鲜水果中维生素C的质量分数。已知:库仑仪中电解原理示意图如下。检测前,电解质溶液中
 保持定值时,电解池不工作。将待测溶液加入电解池后,维生素C将
保持定值时,电解池不工作。将待测溶液加入电解池后,维生素C将 还原,库仑仪便立即自动进行电解到
还原,库仑仪便立即自动进行电解到 又回到原定值,测定结束,通过测定电解消托的电量可以求得维生素C的含量。
又回到原定值,测定结束,通过测定电解消托的电量可以求得维生素C的含量。
①库仑仪工作时电解池的阳极反应式为
②若电解消耗的电量为Q库仑,维生素C的摩尔质量为
 ,则新鲜水果中维生素C的质量分数为
,则新鲜水果中维生素C的质量分数为 的代数式表示)已知:电解中转移
的代数式表示)已知:电解中转移 电子所消耗的电量为96500库仑。
电子所消耗的电量为96500库仑。③测定过程中,需控制电解质溶液
 ,当
,当 时,部分
时,部分 易被空气中的
易被空气中的 直接氧化为
直接氧化为 ,该过程的离子方程式为
,该过程的离子方程式为 ;将导致测得的维生素C的含量
;将导致测得的维生素C的含量
您最近一年使用:0次
2023-12-11更新
|
105次组卷
|
3卷引用:吉林省梅河口市第五中学2023-2024学年高二下学期开学化学试题
名校
4 . 草酸又称乙二酸,是一种重要的化工原料,一般含有结晶水。现某化学兴趣小组欲测定某草酸样品【主要成分是水合草酸 (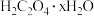 ),还含有少量的草酸钠(
),还含有少量的草酸钠( )】中结晶水的含量,采用如下测定步骤:
)】中结晶水的含量,采用如下测定步骤:
①准确称量质量为 的固体样品于锥形瓶中,加
的固体样品于锥形瓶中,加 蒸馏水,使样品完全溶解,加入2滴指示剂
蒸馏水,使样品完全溶解,加入2滴指示剂 。
。
②用物质的量浓度为 的标准
的标准 溶液滴定至
溶液滴定至 全部转化为
全部转化为 ,到达终点时消耗体积为
,到达终点时消耗体积为 。
。
③向步骤②反应后的溶液中加入一定量的 酸化,用物质的量浓度为
酸化,用物质的量浓度为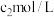 的标准
的标准 溶液滴定,到达终点时,消耗体积为
溶液滴定,到达终点时,消耗体积为 。
。
回答下列问题:
(1)草酸是一种二元弱酸则该酸二级电离平衡常数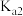 的表达式为
的表达式为___________ 。
(2)步骤①中使用的指示剂 是
是___________ (填“甲基橙溶液”或“酚酞溶液”),不选择另一种指示剂的原因是___________ 。
(3)进行步骤③时,盛放 溶液应使用
溶液应使用___________ 滴定管(填“A”或“B”),原因是___________ ,写出步骤③滴定过程中发生反应的离子方程式___________ 。
(4)如何判断步骤③达到滴定终点___________ 。
(5)通过计算得到,样品中杂质草酸钠的质量分数为___________ (用含有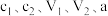 的代数式表示,不用化简)
的代数式表示,不用化简)

(6)下列操作会引起x的测定值偏小的是___________
A.在步骤①中称量药品时,药品和砝码放反,且使用了游码
B.在计算过程中,误认为草酸钠的分子式为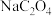
C.在步骤③达到终点且正确读数后,发现在滴定管管口悬有半滴标准 溶液尚未滴下
溶液尚未滴下
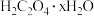 ),还含有少量的草酸钠(
),还含有少量的草酸钠( )】中结晶水的含量,采用如下测定步骤:
)】中结晶水的含量,采用如下测定步骤:①准确称量质量为
 的固体样品于锥形瓶中,加
的固体样品于锥形瓶中,加 蒸馏水,使样品完全溶解,加入2滴指示剂
蒸馏水,使样品完全溶解,加入2滴指示剂 。
。②用物质的量浓度为
 的标准
的标准 溶液滴定至
溶液滴定至 全部转化为
全部转化为 ,到达终点时消耗体积为
,到达终点时消耗体积为 。
。③向步骤②反应后的溶液中加入一定量的
 酸化,用物质的量浓度为
酸化,用物质的量浓度为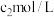 的标准
的标准 溶液滴定,到达终点时,消耗体积为
溶液滴定,到达终点时,消耗体积为 。
。回答下列问题:
(1)草酸是一种二元弱酸则该酸二级电离平衡常数
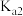 的表达式为
的表达式为(2)步骤①中使用的指示剂
 是
是(3)进行步骤③时,盛放
 溶液应使用
溶液应使用(4)如何判断步骤③达到滴定终点
(5)通过计算得到,样品中杂质草酸钠的质量分数为
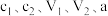 的代数式表示,不用化简)
的代数式表示,不用化简)
(6)下列操作会引起x的测定值偏小的是
A.在步骤①中称量药品时,药品和砝码放反,且使用了游码
B.在计算过程中,误认为草酸钠的分子式为
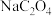
C.在步骤③达到终点且正确读数后,发现在滴定管管口悬有半滴标准
 溶液尚未滴下
溶液尚未滴下
您最近一年使用:0次
名校
解题方法
5 . 过氧化钙(CaO2)广泛应用于水产养殖、污水处理,是优良的供氧剂。
为了测定CaO2的含量,具体的操作:把样品中的过氧化钙转化为碳酸钙,通过测定碳酸钙沉淀的质量,根据钙元素守恒,求得过氧化钙的质量,具体流程如图:

(1)在流程中过氧化钙(CaO2)与水反应的离子反应方程式_______ 。
(2)滴加的Na2CO3溶液要过量的原因是_______ 。
(3)检验沉淀已经洗涤干净的方法是:_______ 。
(4)若供氧剂的质量m=5g,碳酸钙质量n=6g,请通过计算得出供氧剂中的过氧化钙含量的质量分数为_______ %。
(5)若CaCO3沉淀过滤后不洗涤,则过氧化钙的含量将_______ (填“偏大”、“偏小”或“无影响”)。
为了测定CaO2的含量,具体的操作:把样品中的过氧化钙转化为碳酸钙,通过测定碳酸钙沉淀的质量,根据钙元素守恒,求得过氧化钙的质量,具体流程如图:

(1)在流程中过氧化钙(CaO2)与水反应的离子反应方程式
(2)滴加的Na2CO3溶液要过量的原因是
(3)检验沉淀已经洗涤干净的方法是:
(4)若供氧剂的质量m=5g,碳酸钙质量n=6g,请通过计算得出供氧剂中的过氧化钙含量的质量分数为
(5)若CaCO3沉淀过滤后不洗涤,则过氧化钙的含量将
您最近一年使用:0次
名校
6 . 钛是航空、军工、电力等领域的重要原材料。地壳中的含钛矿石之一是金红石( ),其是冶炼钛的重要原料。生产钛的工艺流程如图:
),其是冶炼钛的重要原料。生产钛的工艺流程如图:

已知:①常温下,钛既不与常见非金属单质反应,也不与强酸反应;
②加热时,钛可以和常见的非金属单质反应。
(1)在反应I中:
①下列有关CO的说法正确的是_______ (填标号)。
A.属于酸性氧化物 B.摩尔质量为28 C.为可燃性气体 D.具有还原性
②反应I的化学方程式为_______ ,该反应中氧化剂与还原剂的质量之比为_______ 。
③每转移0.2mol电子,同时生成CO的体积为_______ (标准状况下)。
(2)在反应II中:
①氩气的作用为_______ 。
②该反应的基本反应类型为_______ 。
(3)为了测定反应II制得的金属钛(杂质仅含Mg)中的钛元素含量。常温下,取mg反应II制得的金属钛置于烧杯中,往烧杯中逐滴滴入物质的量浓度为 的稀硫酸,当不再出现气泡时,共消耗VmL稀硫酸:
的稀硫酸,当不再出现气泡时,共消耗VmL稀硫酸:
①上述反应的离子方程式为_______ 。
②金属钛的质量分数为_______ (用含m、c、V的代数式表示)。
 ),其是冶炼钛的重要原料。生产钛的工艺流程如图:
),其是冶炼钛的重要原料。生产钛的工艺流程如图:
已知:①常温下,钛既不与常见非金属单质反应,也不与强酸反应;
②加热时,钛可以和常见的非金属单质反应。
(1)在反应I中:
①下列有关CO的说法正确的是
A.属于酸性氧化物 B.摩尔质量为28 C.为可燃性气体 D.具有还原性
②反应I的化学方程式为
③每转移0.2mol电子,同时生成CO的体积为
(2)在反应II中:
①氩气的作用为
②该反应的基本反应类型为
(3)为了测定反应II制得的金属钛(杂质仅含Mg)中的钛元素含量。常温下,取mg反应II制得的金属钛置于烧杯中,往烧杯中逐滴滴入物质的量浓度为
 的稀硫酸,当不再出现气泡时,共消耗VmL稀硫酸:
的稀硫酸,当不再出现气泡时,共消耗VmL稀硫酸:①上述反应的离子方程式为
②金属钛的质量分数为
您最近一年使用:0次
2023-01-11更新
|
287次组卷
|
7卷引用:吉林省长春外国语学校2022-2023学年高一下学期第一次月考化学试题
7 . 硫酸肼(N2H4·H2SO4)又名硫酸联氨,在医药、染料、农业上用途广泛。
已知:①Cl2与NaOH溶液的反应为放热反应,Cl2与热的NaOH溶液反应会生成NaClO3
②利用尿素法生产水合肼的原理:CO(NH2)2+2NaOH+NaClO=N2H4·H2O+Na2CO3+NaCl
③硫酸肼的制备原理:N2H4·H2O+H2SO4=N2H4·H2SO4+H2O
回答下列问题:
Ⅰ.制备NaClO溶液
实验制备装置如图甲所示:
(1)欲配制220mL6mol/L的盐酸,则需要密度为1.2g/mL,质量分数为36.5%的浓盐酸体积为____ mL,此过程所需玻璃仪器有:量筒、烧杯、玻璃棒、胶头滴管和____ 。
(2)甲图装置C试管内发生主要化学反应的离子方程式为____ 。
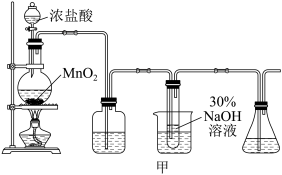
Ⅱ.乙图是尿素法生产水合肼的装置
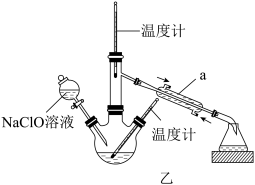
(3)把Ⅰ制得的NaClO溶液注入到图乙装置的分液漏斗中,三颈烧瓶内装入一定量的尿素和NaOH溶液,应采用____ 的方式降温,并控制低温(低于20℃)进行反应。温度高时水合肼会被氧化成无色无味的气体,该气体在标准状况下的密度为1.25g·L-1,其反应的化学方程式为_____ 。反应结束后,收集108~1149℃馏分。
(4)测定馏分中水合肼的含量。称取馏分5.0g,加入适量NaHCO3固体(调节溶液的pH保持在6.5左右),加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.30mol·L-1的碘标准溶液滴定(已知:N2H4·H2O+2I2=N2↑+4HI+H2O)。实验测得消耗I2溶液体积的平均值为20.00mL,则馏分中水合肼(N2H4H2O)的质量分数为____ 。(保留两位有效数字)
Ⅲ.硫酸肼的性质、制备
已知:硫酸肼(又可以表示为:N2H6SO4)是一种重要的化工原料,硫酸肼属于离子化合物,易溶于水,溶液呈酸性,水解原理与(NH4)2SO4类似。
(5)将水合肼转移到烧杯中,滴加一定量浓硫酸,控制温度,得硫酸肼沉淀。洗涤硫酸肼时用无水乙醇而不用水洗涤的原因是____ 。
(6)①写出硫酸肼第二步水解反应的离子方程式:____ 。
②硫酸肼水溶液中离子浓度关系表达正确的是____ (填英文字母)。
A.c(SO )=c(N2H
)=c(N2H )+c(N2H
)+c(N2H )+c(N2H4·H2O)
)+c(N2H4·H2O)
B.c(SO )>c([N2H5·H2O]+)>c(H+)>c(OH-)
)>c([N2H5·H2O]+)>c(H+)>c(OH-)
C.2c(N2H )+c([N2H5·H2O]+)=c(H+)+c(OH-)
)+c([N2H5·H2O]+)=c(H+)+c(OH-)
D.c(SO )>c(N2H
)>c(N2H )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
已知:①Cl2与NaOH溶液的反应为放热反应,Cl2与热的NaOH溶液反应会生成NaClO3
②利用尿素法生产水合肼的原理:CO(NH2)2+2NaOH+NaClO=N2H4·H2O+Na2CO3+NaCl
③硫酸肼的制备原理:N2H4·H2O+H2SO4=N2H4·H2SO4+H2O
回答下列问题:
Ⅰ.制备NaClO溶液
实验制备装置如图甲所示:
(1)欲配制220mL6mol/L的盐酸,则需要密度为1.2g/mL,质量分数为36.5%的浓盐酸体积为
(2)甲图装置C试管内发生主要化学反应的离子方程式为

Ⅱ.乙图是尿素法生产水合肼的装置

(3)把Ⅰ制得的NaClO溶液注入到图乙装置的分液漏斗中,三颈烧瓶内装入一定量的尿素和NaOH溶液,应采用
(4)测定馏分中水合肼的含量。称取馏分5.0g,加入适量NaHCO3固体(调节溶液的pH保持在6.5左右),加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.30mol·L-1的碘标准溶液滴定(已知:N2H4·H2O+2I2=N2↑+4HI+H2O)。实验测得消耗I2溶液体积的平均值为20.00mL,则馏分中水合肼(N2H4H2O)的质量分数为
Ⅲ.硫酸肼的性质、制备
已知:硫酸肼(又可以表示为:N2H6SO4)是一种重要的化工原料,硫酸肼属于离子化合物,易溶于水,溶液呈酸性,水解原理与(NH4)2SO4类似。
(5)将水合肼转移到烧杯中,滴加一定量浓硫酸,控制温度,得硫酸肼沉淀。洗涤硫酸肼时用无水乙醇而不用水洗涤的原因是
(6)①写出硫酸肼第二步水解反应的离子方程式:
②硫酸肼水溶液中离子浓度关系表达正确的是
A.c(SO
 )=c(N2H
)=c(N2H )+c(N2H
)+c(N2H )+c(N2H4·H2O)
)+c(N2H4·H2O)B.c(SO
 )>c([N2H5·H2O]+)>c(H+)>c(OH-)
)>c([N2H5·H2O]+)>c(H+)>c(OH-)C.2c(N2H
 )+c([N2H5·H2O]+)=c(H+)+c(OH-)
)+c([N2H5·H2O]+)=c(H+)+c(OH-)D.c(SO
 )>c(N2H
)>c(N2H )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
您最近一年使用:0次
名校
8 . FeS2/C纳米材料具有较高的可逆比容量以及优秀的倍率性能,可用于锂离子电池负极材料。采用热重分析法测定FeS2/C复合材料中各组分的含量。FeS2/C样品在空气中的热重曲线如图所示。[注:残留率(%)=剩余固体质量 样品质量
样品质量 100%]
100%]
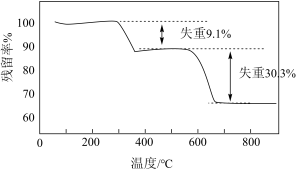
下列说法中不正确的是
 样品质量
样品质量 100%]
100%]
下列说法中不正确的是
| A.300~400℃之间的失重对应着碳的气化 |
B.550~700℃之间的失重反应方程式为: |
| C.FeS2/C复合材料中FeS2与C的物质的量之比约为1:2 |
| D.FeS2/C复合材料中碳的质量分数为9.1% |
您最近一年使用:0次
名校
解题方法
9 . 铁矿石是重要的炼铁原料,其主要成分为铁的氧化物,某研究性小组对某铁矿中铁的含量进行如下测定(不考虑杂质对本实验的影响):

已知:①铁矿石中即含有二价铁、又含有三价铁;
②Cr2O72﹣+6Fe2++14H+=2Cr3++6Fe3++7H2O
③ 中氮元素的化合价为-1,该物质受热易分解。
中氮元素的化合价为-1,该物质受热易分解。
(1)步骤③加入足量还原剂的目的是____________ ,下列物质可作为该步骤还原剂的是_________ 。
A.铁粉 B. C.
C. D.
D.
(2)设计实验方案判断步骤③所加还原剂是否足量_________ 。
(3)步骤④加热煮沸的目的是______________________ 。
(4)步骤需要的玻璃仪器除 容量瓶、烧杯、玻璃棒外,还需要
容量瓶、烧杯、玻璃棒外,还需要_________ ,在稀释过程中,若其他操作均正确,则下列操作会引起铁含量测定结果偏低的是_________ 。
A.烧杯不干燥,含有少量蒸馏水 B.转移滤液后,没有洗涤烧杯和玻璃棒
C.转移滤液时,不慎有少量洒出 D.定容时仰视刻度性
(5)该铁矿石中铁的质量分数为_________ 。

已知:①铁矿石中即含有二价铁、又含有三价铁;
②Cr2O72﹣+6Fe2++14H+=2Cr3++6Fe3++7H2O
③
 中氮元素的化合价为-1,该物质受热易分解。
中氮元素的化合价为-1,该物质受热易分解。(1)步骤③加入足量还原剂的目的是
A.铁粉 B.
 C.
C. D.
D.
(2)设计实验方案判断步骤③所加还原剂是否足量
(3)步骤④加热煮沸的目的是
(4)步骤需要的玻璃仪器除
 容量瓶、烧杯、玻璃棒外,还需要
容量瓶、烧杯、玻璃棒外,还需要A.烧杯不干燥,含有少量蒸馏水 B.转移滤液后,没有洗涤烧杯和玻璃棒
C.转移滤液时,不慎有少量洒出 D.定容时仰视刻度性
(5)该铁矿石中铁的质量分数为
您最近一年使用:0次
名校
10 . 实验室可通过反应;3Cl2+6KOH 5KCl+KC1O3+3H2O 制取KC1O3,再用稍潮湿的KC1O3和草酸(H2C2O4) 在60℃时反应制取ClO2气体,装置如图所示。ClO2是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。
5KCl+KC1O3+3H2O 制取KC1O3,再用稍潮湿的KC1O3和草酸(H2C2O4) 在60℃时反应制取ClO2气体,装置如图所示。ClO2是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。

请回答下列问题:
(1)A 中反应的主要产物有:某种正盐、ClO2和CO2等,写出该反应的化学方程式:_______________________________ 。
(2)请分析装置图,进行补充和完善。A部分缺___________ 装置,B部分还应补充____________ 装置,还有一处设计明显不合理的是___________ (填“A”“B”或“C”)
(3)C中的试剂为NaOH溶液时,反应生成NaClO3和NaClO2,写出该反应的离于方程式:______________________________________ 。
(4)在密闭容器中向9℃的KOH溶液中通入少量Cl2,此时Cl2的氧化产物主要是______________ ;继续通入适量Cl2,将溶液加热,溶液中主要离子的浓度随温度的变化如图所示,图中甲、乙、丙依次表示的离子是____________________ (不考虑Cl2的挥发)

(5)测定KClO3样品中C1O3-的含量,称取样品ag,准确配制成1000mL溶液,从上述溶液中取出10.00mL 于锥形瓶中,准确加入30.00mL 1.00 mol•L-1 (NH4)2Fe(SO4)2溶液(过量)。再在锥形瓶中加入100mL 蒸馏水及某种指示剂,用0.200 mol•L-1K2Cr2O7标准溶液滴定至终点,消耗5.00mL。样品中C1O3-的质量分数为_________ 。(已知Cr2O72-+6Fe2++14H+==2Cr3++6Fe3++7H2O,C1O3-可被Fe2+还原为Cl-)
 5KCl+KC1O3+3H2O 制取KC1O3,再用稍潮湿的KC1O3和草酸(H2C2O4) 在60℃时反应制取ClO2气体,装置如图所示。ClO2是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。
5KCl+KC1O3+3H2O 制取KC1O3,再用稍潮湿的KC1O3和草酸(H2C2O4) 在60℃时反应制取ClO2气体,装置如图所示。ClO2是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。
请回答下列问题:
(1)A 中反应的主要产物有:某种正盐、ClO2和CO2等,写出该反应的化学方程式:
(2)请分析装置图,进行补充和完善。A部分缺
(3)C中的试剂为NaOH溶液时,反应生成NaClO3和NaClO2,写出该反应的离于方程式:
(4)在密闭容器中向9℃的KOH溶液中通入少量Cl2,此时Cl2的氧化产物主要是

(5)测定KClO3样品中C1O3-的含量,称取样品ag,准确配制成1000mL溶液,从上述溶液中取出10.00mL 于锥形瓶中,准确加入30.00mL 1.00 mol•L-1 (NH4)2Fe(SO4)2溶液(过量)。再在锥形瓶中加入100mL 蒸馏水及某种指示剂,用0.200 mol•L-1K2Cr2O7标准溶液滴定至终点,消耗5.00mL。样品中C1O3-的质量分数为
您最近一年使用:0次
2018-01-18更新
|
314次组卷
|
2卷引用:【全国百强校】吉林省实验中学2019届高三上学期期中考试化学试题



