名校
1 .  具有强氧化性,
具有强氧化性, 具有还原性,某探究小组的同学学习氧化还原反应的知识后推测
具有还原性,某探究小组的同学学习氧化还原反应的知识后推测 与
与 可以发生反应。为了验证他们的猜想,设计了如图所示的实验进行验证。
可以发生反应。为了验证他们的猜想,设计了如图所示的实验进行验证。

Ⅰ.实验探究:
(1)装置A中盛装稀盐酸的仪器名称为___________ ,A装置发生的离子方程式为_____________________ ,B装置的作用是_____________________ ,里面盛放的试剂可以是___________ (填序号)。
A浓硫酸 B.碱石灰 C.无水硫酸铜
(2)下面是实验过程中的重要步骤,选出正确的操作顺序___________ 。
①用小试管收集气体,并检验其纯度
②停止加热,充分冷却后,关闭止水夹 和
和
③加热装有 的硬质玻璃管,使其逐渐熔化,反应一段时间
的硬质玻璃管,使其逐渐熔化,反应一段时间
④打开 和
和 ,滴加稀盐酸
,滴加稀盐酸
(3)在实验过程中观察到C中淡黄色固体逐渐变成白色,无水硫酸铜未变成蓝色,则 与
与 反应生成的产物为
反应生成的产物为___________ 。
Ⅱ.数据处理:
(4)实验结束以后,该小组的同学还想测定C装置内白色固体中未反应完的 含量。
含量。
操作流程如下:

①操作2的名称________________
②白色固体中 的质量分数为
的质量分数为________________ (用含 和
和 的式子表示)。
的式子表示)。
 具有强氧化性,
具有强氧化性, 具有还原性,某探究小组的同学学习氧化还原反应的知识后推测
具有还原性,某探究小组的同学学习氧化还原反应的知识后推测 与
与 可以发生反应。为了验证他们的猜想,设计了如图所示的实验进行验证。
可以发生反应。为了验证他们的猜想,设计了如图所示的实验进行验证。
Ⅰ.实验探究:
(1)装置A中盛装稀盐酸的仪器名称为
A浓硫酸 B.碱石灰 C.无水硫酸铜
(2)下面是实验过程中的重要步骤,选出正确的操作顺序
①用小试管收集气体,并检验其纯度
②停止加热,充分冷却后,关闭止水夹
 和
和
③加热装有
 的硬质玻璃管,使其逐渐熔化,反应一段时间
的硬质玻璃管,使其逐渐熔化,反应一段时间④打开
 和
和 ,滴加稀盐酸
,滴加稀盐酸(3)在实验过程中观察到C中淡黄色固体逐渐变成白色,无水硫酸铜未变成蓝色,则
 与
与 反应生成的产物为
反应生成的产物为Ⅱ.数据处理:
(4)实验结束以后,该小组的同学还想测定C装置内白色固体中未反应完的
 含量。
含量。操作流程如下:

①操作2的名称
②白色固体中
 的质量分数为
的质量分数为 和
和 的式子表示)。
的式子表示)。
您最近一年使用:0次
名校
解题方法
2 . 由硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、Al2O3和SiO2)得到绿矾(FeSO4•7H2O),然后制取透明氧化铁颜料的流程如图:
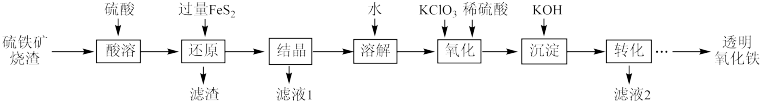
已知:
I.透明氧化铁又称纳米氧化铁,粒子直径很微小(10~90nm),包括氧化铁黄(FeOOH)和氧化铁红(Fe2O3),难溶于水,在碱性条件下非常稳定;
II.Fe3+能将FeS2中的硫元素氧化为+6价。
(1)FeS2的电子式是_____ 。
(2)“滤渣”中的主要成分是_____ (填名称)。
(3)流程中“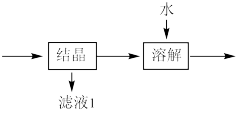 ”环节的目的是
”环节的目的是_____ 。
(4)“还原”过程中涉及的离子方程式为_____ 。
(5)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到均匀、色泽纯正的氢氧化铁,而且还可以_____ 。
(6)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁红的含量。已知Fe(SCN)3的吸光度A(对特定波长光的吸收程度)与Fe3+标准溶液浓度的关系如图所示。
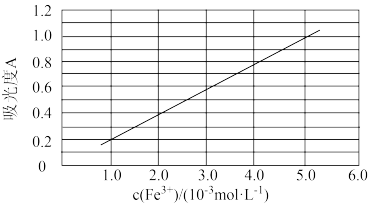
称取3.47g透明氧化铁,用稀硫酸溶解并定容至1L,准确移取该溶液10.00mL,加入足量KSCN溶液,再用蒸馏水定容至100mL,测得溶液吸光度A=0.8,则透明氧化铁中氧化铁黄的质量分数为_____ 。

已知:
I.透明氧化铁又称纳米氧化铁,粒子直径很微小(10~90nm),包括氧化铁黄(FeOOH)和氧化铁红(Fe2O3),难溶于水,在碱性条件下非常稳定;
II.Fe3+能将FeS2中的硫元素氧化为+6价。
(1)FeS2的电子式是
(2)“滤渣”中的主要成分是
(3)流程中“
 ”环节的目的是
”环节的目的是(4)“还原”过程中涉及的离子方程式为
(5)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到均匀、色泽纯正的氢氧化铁,而且还可以
(6)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁红的含量。已知Fe(SCN)3的吸光度A(对特定波长光的吸收程度)与Fe3+标准溶液浓度的关系如图所示。

称取3.47g透明氧化铁,用稀硫酸溶解并定容至1L,准确移取该溶液10.00mL,加入足量KSCN溶液,再用蒸馏水定容至100mL,测得溶液吸光度A=0.8,则透明氧化铁中氧化铁黄的质量分数为
您最近一年使用:0次
3 . 纯ClO2遇热易发生分解,工业上通常制成NaClO2固体以便运输和储存。制备NaClO2的实验装置如图所示(夹持装置省略),其中A装置制备ClO2,C装置用于制备NaClO2。回答下列问题:
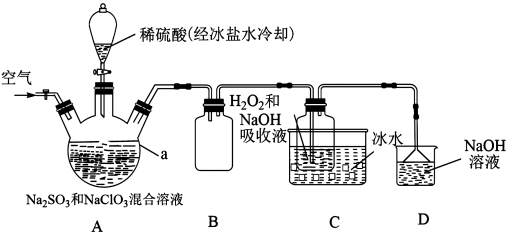
(1)仪器a的名称是_______ 。
(2)装置B的作用是_______ 。
(3)装置A中发生反应的离子方程式为_______ 。向装置A中通入空气的目的是_______ 。
(4)装置C中发生反应的化学方程式为_______ ,C装置采用“冰水浴”的目的是_______ 。
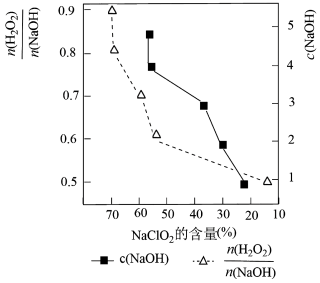
(5)研究测得C装置吸收液中的c(NaOH)与 对粗产品中NaClO2含量的影响如图所示。则最佳条件为c(NaOH)=
对粗产品中NaClO2含量的影响如图所示。则最佳条件为c(NaOH)=_______ mol·L-1, =
=_______ 。
(6)准确称取5.000 g所得粗产品NaClO2晶体溶于适量蒸馏水,加入过量的碘化钾溶液,在酸性条件下发生充分反应: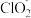 +4I-+4H+=2H2O+2I2+Cl-,将所得混合液稀释成250 mL待测溶液。移取25.00 mL待测溶液,用0.8000 mol·L-1的Na2S2O3标准溶液滴定至终点,重复2次,测得消耗Na2S2O3标准溶液的体积平均值为20.0 mL(已知:I2+2
+4I-+4H+=2H2O+2I2+Cl-,将所得混合液稀释成250 mL待测溶液。移取25.00 mL待测溶液,用0.8000 mol·L-1的Na2S2O3标准溶液滴定至终点,重复2次,测得消耗Na2S2O3标准溶液的体积平均值为20.0 mL(已知:I2+2 =2I-+
=2I-+ )。则该样品中NaClO2的质量分数为
)。则该样品中NaClO2的质量分数为_______ 。

(1)仪器a的名称是
(2)装置B的作用是
(3)装置A中发生反应的离子方程式为
(4)装置C中发生反应的化学方程式为
(5)研究测得C装置吸收液中的c(NaOH)与
 对粗产品中NaClO2含量的影响如图所示。则最佳条件为c(NaOH)=
对粗产品中NaClO2含量的影响如图所示。则最佳条件为c(NaOH)= =
=
(6)准确称取5.000 g所得粗产品NaClO2晶体溶于适量蒸馏水,加入过量的碘化钾溶液,在酸性条件下发生充分反应:
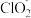 +4I-+4H+=2H2O+2I2+Cl-,将所得混合液稀释成250 mL待测溶液。移取25.00 mL待测溶液,用0.8000 mol·L-1的Na2S2O3标准溶液滴定至终点,重复2次,测得消耗Na2S2O3标准溶液的体积平均值为20.0 mL(已知:I2+2
+4I-+4H+=2H2O+2I2+Cl-,将所得混合液稀释成250 mL待测溶液。移取25.00 mL待测溶液,用0.8000 mol·L-1的Na2S2O3标准溶液滴定至终点,重复2次,测得消耗Na2S2O3标准溶液的体积平均值为20.0 mL(已知:I2+2 =2I-+
=2I-+ )。则该样品中NaClO2的质量分数为
)。则该样品中NaClO2的质量分数为
您最近一年使用:0次
2022-04-25更新
|
690次组卷
|
3卷引用:新疆维吾尔自治区乌鲁木齐市实验学校2023-2024学年高三上学期1月月考化学试题
新疆维吾尔自治区乌鲁木齐市实验学校2023-2024学年高三上学期1月月考化学试题安徽省“皖南八校”2022届高三下学期第三次联考理综化学试题(已下线)专项14 化学实验综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)
名校
解题方法
4 . 硫氰化钾(KSCN)是一种用途广泛的化学药品,常用于合成树脂、杀虫杀菌剂等。某化学小组用下图实验装置模拟工业制备硫氰化钾。

已知:①CS2为不溶于水且密度比水大的非极性试剂。
②NH4HS、(NH4)2S 在热水中易分解生成NH3和H2S。
③装置B中,滴液漏斗中装有一定体积5mol/L KOH溶液。
回答下列问题:
(1)制备NH4SCN溶液:
①三颈烧瓶内盛放有76g CS2、水和难溶于水的固体做催化剂。实验开始时,打开K1,水浴加热装置B,发生反应CS2+ 3NH3 NH4SCN + NH4HS, 则装置A中固体a的成分为
NH4SCN + NH4HS, 则装置A中固体a的成分为 _______ 。
②一段时间后,当观察到三颈烧瓶内_______ 时, 停止通入气体,反应完成。关闭K1和K2,将三颈烧瓶继续加热一段时间。
③装置C中用酸性KMnO4溶液吸收尾气后得澄清溶液,H2S所发生反应的离子方程式为_______ 。
(2)制备KSCN晶体:
打开K3,_______ , 干燥,得到硫氰化钾晶体。(须用的试剂:5mol/LKOH、蒸馏水、稀硫酸)
(3)测定产品中KSCN的含量:
称取0.85g样品,配成100mL溶液。量取25.00mL溶液锥形瓶中,加入适量稀硝酸,再加入几滴铁盐溶液作指示剂,用0.1000mol/LAgNO3标准溶液滴定,滴定时发生的反应:SCN—+Ag+=AgSCN↓(白色)。达到滴定终点,三次滴定平均消耗AgNO3标准溶液20.00mL。产品中KSCN的质量分数为_______ 。

已知:①CS2为不溶于水且密度比水大的非极性试剂。
②NH4HS、(NH4)2S 在热水中易分解生成NH3和H2S。
③装置B中,滴液漏斗中装有一定体积5mol/L KOH溶液。
回答下列问题:
(1)制备NH4SCN溶液:
①三颈烧瓶内盛放有76g CS2、水和难溶于水的固体做催化剂。实验开始时,打开K1,水浴加热装置B,发生反应CS2+ 3NH3
 NH4SCN + NH4HS, 则装置A中固体a的成分为
NH4SCN + NH4HS, 则装置A中固体a的成分为 ②一段时间后,当观察到三颈烧瓶内
③装置C中用酸性KMnO4溶液吸收尾气后得澄清溶液,H2S所发生反应的离子方程式为
(2)制备KSCN晶体:
打开K3,
(3)测定产品中KSCN的含量:
称取0.85g样品,配成100mL溶液。量取25.00mL溶液锥形瓶中,加入适量稀硝酸,再加入几滴铁盐溶液作指示剂,用0.1000mol/LAgNO3标准溶液滴定,滴定时发生的反应:SCN—+Ag+=AgSCN↓(白色)。达到滴定终点,三次滴定平均消耗AgNO3标准溶液20.00mL。产品中KSCN的质量分数为
您最近一年使用:0次
2022-04-20更新
|
460次组卷
|
4卷引用:新疆乌鲁木齐市第101中学2023-2024学年高三上学期8月月考化学试题
新疆乌鲁木齐市第101中学2023-2024学年高三上学期8月月考化学试题江苏省南通市海门区2022届高三下学期阶段检测化学试题(已下线)考点51 物质的制备-备战2023年高考化学一轮复习考点帮(全国通用)江西省重点校联盟2022-2023学年高三上学期10月联考化学试题
名校
5 . 大苏打 、苏打、小苏打被称为“苏氏三兄弟”。它们在生活、生产中有广泛应用。
、苏打、小苏打被称为“苏氏三兄弟”。它们在生活、生产中有广泛应用。
(1)工业上,将 和
和 以
以 的物质的量之比配成溶液。再通入
的物质的量之比配成溶液。再通入 可制取
可制取 ,同时放出
,同时放出 ,写出该反应的化学方程
,写出该反应的化学方程___________ 。 溶液在空气中久置,会生成浅黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的电子式为
溶液在空气中久置,会生成浅黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的电子式为___________ 。
(2) 标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高。用离子方程式表示其原因
标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高。用离子方程式表示其原因___________ 。
(3)下列关于苏打和小苏打的说法正确的是___________ (选填字母序号)。
A.纯碱是一种重要的化工原料,在玻璃、肥皂、造纸等工业中都有重要的应用
B.苏打和小苏打的相互转化属于可逆反应
C.苏打(含氯化钠杂质)可用滴定法测苏打的质量分数,使用石蕊溶液做指示剂更准确
D.牙膏中加入小苏打可以让小苏打颗粒直接摩擦牙齿,帮助清洁牙垢
(4)向 的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后再向溶液中逐滴滴入
的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后再向溶液中逐滴滴入 的稀盐酸,产生气体体积(标况)如图所示。
的稀盐酸,产生气体体积(标况)如图所示。

请回答下列问题
①通入二氧化碳后形成溶液的溶质成分是___________ (填写化学式)
②滴入 稀盐酸过程中,溶液导电性
稀盐酸过程中,溶液导电性___________ (填“增强”或“减弱”),试解释其原因___________ 。
③原 氢氧化钠溶液的浓度为
氢氧化钠溶液的浓度为___________ 。
 、苏打、小苏打被称为“苏氏三兄弟”。它们在生活、生产中有广泛应用。
、苏打、小苏打被称为“苏氏三兄弟”。它们在生活、生产中有广泛应用。(1)工业上,将
 和
和 以
以 的物质的量之比配成溶液。再通入
的物质的量之比配成溶液。再通入 可制取
可制取 ,同时放出
,同时放出 ,写出该反应的化学方程
,写出该反应的化学方程 溶液在空气中久置,会生成浅黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的电子式为
溶液在空气中久置,会生成浅黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的电子式为(2)
 标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高。用离子方程式表示其原因
标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高。用离子方程式表示其原因(3)下列关于苏打和小苏打的说法正确的是
A.纯碱是一种重要的化工原料,在玻璃、肥皂、造纸等工业中都有重要的应用
B.苏打和小苏打的相互转化属于可逆反应
C.苏打(含氯化钠杂质)可用滴定法测苏打的质量分数,使用石蕊溶液做指示剂更准确
D.牙膏中加入小苏打可以让小苏打颗粒直接摩擦牙齿,帮助清洁牙垢
(4)向
 的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后再向溶液中逐滴滴入
的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后再向溶液中逐滴滴入 的稀盐酸,产生气体体积(标况)如图所示。
的稀盐酸,产生气体体积(标况)如图所示。
请回答下列问题
①通入二氧化碳后形成溶液的溶质成分是
②滴入
 稀盐酸过程中,溶液导电性
稀盐酸过程中,溶液导电性③原
 氢氧化钠溶液的浓度为
氢氧化钠溶液的浓度为
您最近一年使用:0次
2021-02-09更新
|
1015次组卷
|
7卷引用:新疆维吾尔自治区伊犁哈萨克自治州新源县第二中学2021-2022学年上学期高三第一次月考化学试题
新疆维吾尔自治区伊犁哈萨克自治州新源县第二中学2021-2022学年上学期高三第一次月考化学试题河南省信阳市2021届高三上学期第二次教学质量检测化学试题(已下线)专题06 钠及其化合物(限时精练)-2022届高考化学一轮复习热点题型归纳与变式训练(已下线)第07讲 钠及其重要化合物(精练)-2022年高考化学一轮复习讲练测河北省武安市第一中学2021-2022学年高三上学期第五次调研考试化学试题(已下线)第07讲 钠及其重要化合物(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第1讲 钠及其重要化合物
名校
解题方法
6 . 硫酸肼(N2H4·H2SO4)又名硫酸联氨,在医药、染料、农业上用途广泛。回答下列问题:
已知:①Cl2与NaOH反应为放热反应,Cl2与热的NaOH溶液会生成NaClO3;
②利用尿素法生产水合肼的原理为CO(NH2)2+2NaOH+NaClO=N2H4·H2O+Na2CO3+NaCl;
③硫酸肼的制备原理为N2H4·H2O+H2SO4=N2H4·H2SO4+H2O。
I.制备NaClO溶液。实验制备装置如图1所示:

(1)图1装置试管内发生主要反应的化学方程式为_______ 。
II.尿素法生产水合肼的装置如图2所示:

(2)把I制得的NaClO溶液注入到图2装置的分液漏斗中,三颈烧瓶内装入一定量的尿素和NaOH溶液(物质的量之比1∶2.30),仪器a的名称为_______ ,采用低温(低于20℃)反应,降温的方式可采用_______ ,温度高时水合肼会被氧化成无色无味的气体,该气体在标准状况下的密度为1.25g·L−1,其反应化学方程式为_______ 。反应结束后,急速升温至108℃开始回流5min,收集108~114℃馏分。
(3)测定馏分中水合肼的含量。称取馏分6.0g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.30mol·L−1的碘标准溶液滴定(已知:N2H4·H2O+2I2=N2↑+4HI+H2O)。
①判断滴定终点的方法是_______ 。
②实验测得消耗碘标准溶液的平均值为20.00mL,馏分中水合肼(N2H4·H2O)的质量分数为_______ 。
III.硫酸肼的制备
(4)将水合肼转移到烧杯中,滴加一定质量98%的浓硫酸,滴加时间控制在1h左右,温度60℃以下。冷藏沉降2h,得硫酸肼沉淀。抽滤,用无水乙醇洗涤,干燥,得白色硫酸肼固体。用无水乙醇而不用水洗涤的原因是_______ 。
已知:①Cl2与NaOH反应为放热反应,Cl2与热的NaOH溶液会生成NaClO3;
②利用尿素法生产水合肼的原理为CO(NH2)2+2NaOH+NaClO=N2H4·H2O+Na2CO3+NaCl;
③硫酸肼的制备原理为N2H4·H2O+H2SO4=N2H4·H2SO4+H2O。
I.制备NaClO溶液。实验制备装置如图1所示:

(1)图1装置试管内发生主要反应的化学方程式为
II.尿素法生产水合肼的装置如图2所示:

(2)把I制得的NaClO溶液注入到图2装置的分液漏斗中,三颈烧瓶内装入一定量的尿素和NaOH溶液(物质的量之比1∶2.30),仪器a的名称为
(3)测定馏分中水合肼的含量。称取馏分6.0g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.30mol·L−1的碘标准溶液滴定(已知:N2H4·H2O+2I2=N2↑+4HI+H2O)。
①判断滴定终点的方法是
②实验测得消耗碘标准溶液的平均值为20.00mL,馏分中水合肼(N2H4·H2O)的质量分数为
III.硫酸肼的制备
(4)将水合肼转移到烧杯中,滴加一定质量98%的浓硫酸,滴加时间控制在1h左右,温度60℃以下。冷藏沉降2h,得硫酸肼沉淀。抽滤,用无水乙醇洗涤,干燥,得白色硫酸肼固体。用无水乙醇而不用水洗涤的原因是
您最近一年使用:0次
2021-05-14更新
|
158次组卷
|
4卷引用:新疆和田地区第二中学2022-2023学年高二上学期11月期中考试化学试题
新疆和田地区第二中学2022-2023学年高二上学期11月期中考试化学试题(已下线)化学-学科网2021年高三5月大联考(新课标Ⅲ卷)云南省腾冲市第八中学2023--2024学年上学期高二第3次月考化学试卷湖南省宁乡市第一高级中学2021届高三第二次模拟考试化学试卷
7 . 过氧乙酸(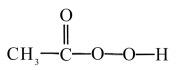 )可以有效地杀灭新冠肺炎等病毒,是一种广泛、高效、速效、廉价的消毒剂,应用广泛。回答下列回题。
)可以有效地杀灭新冠肺炎等病毒,是一种广泛、高效、速效、廉价的消毒剂,应用广泛。回答下列回题。
(1)过氧乙酸极不稳定,110℃时遇空气发生爆炸,此时发生反应的化学方程式是__________ ,所以过氧乙酸需要___________ 保存。
(2)过氧乙酸具有强氧化性,这与它的( )
)________ (填序号)键有关,向硫酸酸化的过氧乙酸溶液中加入少量KI溶液,溶液变黄,发生反应的离子方程式是_________ ,如有 过氧乙酸被还原,转移电子的物质的量是
过氧乙酸被还原,转移电子的物质的量是___________ mol。
(3)过氧乙酸可由 与
与 ,在浓硫酸催化作用下制得,反应方程式是
,在浓硫酸催化作用下制得,反应方程式是_________ ,其中浓硫酸用量(浓硫酸占反应液的体积百分数)对过氧乙酸的含量的影响如图:
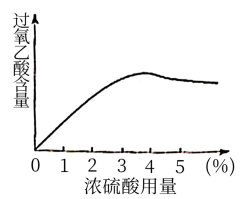
根据图表分析,浓硫酸的合适用量为___________ %(填整数)。
(4)过氧乙酸也可以用乙醛氧化法制得,反应原理为:
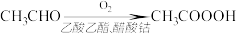
反应中乙醛的转化率为85%,生产质量分数10%的过氧乙酸溶液100kg,需要乙醛的质量为________ kg。
 )可以有效地杀灭新冠肺炎等病毒,是一种广泛、高效、速效、廉价的消毒剂,应用广泛。回答下列回题。
)可以有效地杀灭新冠肺炎等病毒,是一种广泛、高效、速效、廉价的消毒剂,应用广泛。回答下列回题。(1)过氧乙酸极不稳定,110℃时遇空气发生爆炸,此时发生反应的化学方程式是
(2)过氧乙酸具有强氧化性,这与它的(
 )
) 过氧乙酸被还原,转移电子的物质的量是
过氧乙酸被还原,转移电子的物质的量是(3)过氧乙酸可由
 与
与 ,在浓硫酸催化作用下制得,反应方程式是
,在浓硫酸催化作用下制得,反应方程式是
根据图表分析,浓硫酸的合适用量为
(4)过氧乙酸也可以用乙醛氧化法制得,反应原理为:
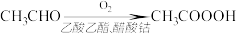
反应中乙醛的转化率为85%,生产质量分数10%的过氧乙酸溶液100kg,需要乙醛的质量为
您最近一年使用:0次
8 . 以电解法生产金属锰产生的阳极泥中,其锰含量高达40%~50%,主要成分为MnO2的水合物,且含有显著量的Pb2+、Sn2+等重金属杂质.本工艺采用的木屑富含的纤维素在较浓硫酸的作用下膨胀、水解生成还原糖,酸性条件下,可与二氧化锰反应生成可溶性的硫酸锰。
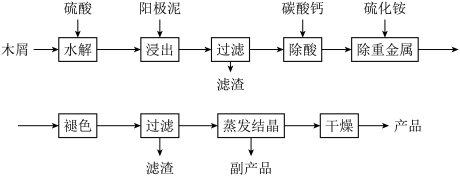
(1)工业上电解硫酸锰的水溶液生产金属锰,阳极的电极反应式为_____________ 。
(2)写出木屑水解反应的化学方程式:___________
配平浸出步骤反应方程式C6H12O6+MnO2+H2SO4→MnSO4+CO2+H2O_________________
(3)若取消除酸操作步骤,将会产生气体_____________ (填化学式)而污染环境;
(4)本工艺的一种副产品是重要的农业生产资料,写出其化学式____ ;
(5)取一定量的阳极泥进行实验分析,得到如图像。硫酸的最合适用量为________ mL,若再增加硫酸的用量,将会导致____________ (填化学式)的消耗量增大。

(6)某阳极泥中MnO2(相对分子质量为87)的质量分数为50.0%,将174g该阳极泥与320g36.5%的浓盐酸混合加热,则产生的氯气在标准状况下应少于_________ L。(假设阳极泥中的其它成分不参与反应)

(1)工业上电解硫酸锰的水溶液生产金属锰,阳极的电极反应式为
(2)写出木屑水解反应的化学方程式:
配平浸出步骤反应方程式C6H12O6+MnO2+H2SO4→MnSO4+CO2+H2O
(3)若取消除酸操作步骤,将会产生气体
(4)本工艺的一种副产品是重要的农业生产资料,写出其化学式
(5)取一定量的阳极泥进行实验分析,得到如图像。硫酸的最合适用量为

(6)某阳极泥中MnO2(相对分子质量为87)的质量分数为50.0%,将174g该阳极泥与320g36.5%的浓盐酸混合加热,则产生的氯气在标准状况下应少于
您最近一年使用:0次
名校
9 . 人的血液中的葡萄糖(简称血糖)的含量,以“mmol/L”表示时,正常值在3.61~6.11 mmol/L之间。这种表示血糖指标的物理量是
| A.质量分数 | B.物质的量浓度 | C.摩尔质量 | D.溶解度 |
您最近一年使用:0次
2018-03-13更新
|
409次组卷
|
5卷引用:新疆生产建设兵团第四师第一中学2020-2021学年高一上学期期中考试化学试题
名校
10 . 将28g CO2和CO的混合气体,通过装有足量过氧化钠的干燥管,反应后干燥管的总质量增加了5.6g,则原混合气体中CO2的质量分数为
| A.32 | B.44% | C.56% | D.88% |
您最近一年使用:0次
2024-03-01更新
|
57次组卷
|
2卷引用:新疆乌鲁木齐市第八中学2023-2024学年高一上学期1月期末化学试题



