解题方法
1 . 一种催化还原NO的机理如图所示,下列说法正确的是
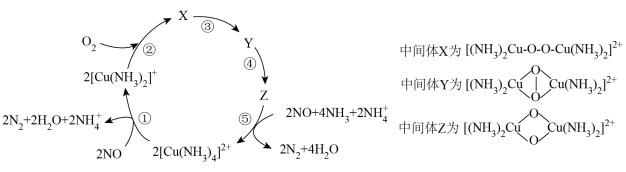

| A.中间体X和Z中O和Cu的化合价均不变 |
B.使用催化剂 ,可以提高NO的反应速率和平衡转化率 ,可以提高NO的反应速率和平衡转化率 |
| C.过程①中既有极性键的断裂,也有极性键的形成 |
D.该催化还原过程的总反应方程式为 |
您最近半年使用:0次
昨日更新
|
15次组卷
|
2卷引用:2024届新疆维吾尔自治区高三下学期三模考试理综试题-高中化学
解题方法
2 . 化学是现代生产、生活与科技的中心学科之一,下列说法正确的是
| A.中国天眼FAST用到的碳化硅及制作宇航服常用的聚四氟乙烯都属于有机高分子材料 |
| B.“蛟龙”号载人潜水器最关键的部件—耐压球壳是用稀土金属钛(第ⅣB族)制造而成 |
| C.2023年诺贝尔化学奖授予了“发现和合成量子点(纳米级粒子)”的三位科学家,量子点形成分散系后可能具有丁达尔效应 |
| D.超分子内部分子之间通过共价键结合 |
您最近半年使用:0次
昨日更新
|
32次组卷
|
2卷引用:2024届新疆维吾尔自治区高三下学期三模考试理综试题-高中化学
3 . 用氧化锌烟尘(主要成分为ZnO,还含有少量PbO、CuO、Fe2O3、FeO等)生产ZnSO4∙7H2O的流程如下(已知PbO不溶于稀硫酸酸):
(1)“酸浸”时用的稀酸是_______ (写名称)。
(2)加入NaClO的目的是_______ ,加入ZnO除杂时pH控制范围是_______ ~5.0。
(3)写出ZnO除杂得到滤渣2的离子反应方程式_______ 。
(4)滤渣3是_______ (写化学式) 。
(5)由滤液得到ZnSO4∙7H2O的操作是 蒸发浓缩、_______ 、 过滤、洗涤、干燥。
(6)已知Fe3+沉淀完全的标准为1.0×10-6mol。L-1,根据题目条件求常温下Fe(OH)3的Ksp=_______ 。

| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Cu2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 | 4.7 |
| 沉淀完全的pH | 3.0 | 8.3 | 8.2 | 6.7 |
(1)“酸浸”时用的稀酸是
(2)加入NaClO的目的是
(3)写出ZnO除杂得到滤渣2的离子反应方程式
(4)滤渣3是
(5)由滤液得到ZnSO4∙7H2O的操作是 蒸发浓缩、
(6)已知Fe3+沉淀完全的标准为1.0×10-6mol。L-1,根据题目条件求常温下Fe(OH)3的Ksp=
您最近半年使用:0次
解题方法
4 . 常温下,向0.1mol∙L-1二元弱酸H2A溶液中逐滴加入NaOH溶液,H2A、HA-、A2-的物质的量分数[已知 ]。随pH的变化如图所示。下列叙述正确的是
]。随pH的变化如图所示。下列叙述正确的是
 ]。随pH的变化如图所示。下列叙述正确的是
]。随pH的变化如图所示。下列叙述正确的是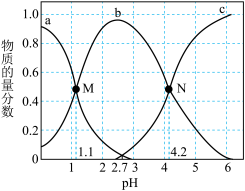
| A.a曲线代表A2-的物质的量分数随pH的变化 |
| B.溶液pH=1时的导电能力强于pH=6时的导电能力 |
| C.H2A第二步电离常数Ka2=10-4.2 |
| D.N点pH=4.2时,c(A2-)=c(HA-),溶液中不存在H2A分子 |
您最近半年使用:0次
解题方法
5 . 元素在周期表中的位置,反映了元素的原子结构和元素的性质,下图是元素周期表的一部分。______ (金属或非金属)元素;元素b在元素周期表中的位置为______ 。
(2)元素c的原子结构示意图_______ ;元素f的元素符号为______ ;元素c和f的原子半径大小关系为c____ f(>或<)
(3)元素d和元素g形成的盐的电子式为_______ 。
(4)第一电离能a___ d(>或<),非金属性c___ f(>或<)。
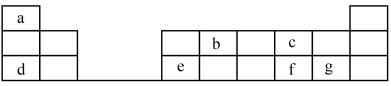
(2)元素c的原子结构示意图
(3)元素d和元素g形成的盐的电子式为
(4)第一电离能a
您最近半年使用:0次
解题方法
6 . 计算题本题要求写计算过程。
(1)计算出 的物质的量为
的物质的量为___________ 。
(2)配置 溶液,需要NaOH是多少?
溶液,需要NaOH是多少?___________
(1)计算出
 的物质的量为
的物质的量为(2)配置
 溶液,需要NaOH是多少?
溶液,需要NaOH是多少?
您最近半年使用:0次
7 . 化学是一门实用性很强的学科,请根据要求完成下列问题。
(1)钠有多种化合物,其中俗称“纯碱”的是___________ (填“ ”或“
”或“ ”)。
”)。
(2)铁有多种氧化物,其中为黑色且具有磁性的是___________ (填“ ”或“
”或“ ”)。
”)。
(3)日常生活中,活泼的铝在空气中能稳定存在的原因是表层的铝在空气中反应生成了___________ [填“ ”或“
”或“ ”],保护内层金属。
”],保护内层金属。
(4)铝与氢氧化钠溶液反应的离子方程式为___________ 。
(5)铁与水蒸气反应的化学方程式为___________ 。
(6)简述检验 的实验操作
的实验操作___________ 。
(1)钠有多种化合物,其中俗称“纯碱”的是
 ”或“
”或“ ”)。
”)。(2)铁有多种氧化物,其中为黑色且具有磁性的是
 ”或“
”或“ ”)。
”)。(3)日常生活中,活泼的铝在空气中能稳定存在的原因是表层的铝在空气中反应生成了
 ”或“
”或“ ”],保护内层金属。
”],保护内层金属。(4)铝与氢氧化钠溶液反应的离子方程式为
(5)铁与水蒸气反应的化学方程式为
(6)简述检验
 的实验操作
的实验操作
您最近半年使用:0次
解题方法
8 . 回答下列问题。
(1)氢氧化亚铁与氧气、水的反应方程式为:___________ 。
(2)钠通常保存在___________ 中,加热时,钠可以在空气中燃烧发出___________ 火焰,生成___________ 色固体。
(3)写出氯气和水反应的化学方程式:___________ 。
(4)电离:电解质溶于水或受热熔化时,形成___________ 的过程。
(5) 、
、 、
、 、
、 、
、 、
、 中,
中,___________ 和___________ 互为同位素,___________ 和___________ 的中子数相等,但质子数不等,所以不是同一种元素。
(6)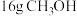 的物质的量是
的物质的量是___________ ,含H原子的数目为___________ 。
(1)氢氧化亚铁与氧气、水的反应方程式为:
(2)钠通常保存在
(3)写出氯气和水反应的化学方程式:
(4)电离:电解质溶于水或受热熔化时,形成
(5)
 、
、 、
、 、
、 、
、 、
、 中,
中,(6)
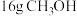 的物质的量是
的物质的量是
您最近半年使用:0次
解题方法
9 . 雷雨天 转化为
转化为 的流程为:
的流程为: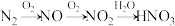
(1) 转化为NO的化学方程式是“
转化为NO的化学方程式是“_____ 。”
(2)NO转化为 的化学方程式是“
的化学方程式是“_____ 。”
(3) 转化为
转化为 的化学方程式是“
的化学方程式是“_____ 。”
 转化为
转化为 的流程为:
的流程为: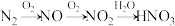
(1)
 转化为NO的化学方程式是“
转化为NO的化学方程式是“(2)NO转化为
 的化学方程式是“
的化学方程式是“(3)
 转化为
转化为 的化学方程式是“
的化学方程式是“
您最近半年使用:0次
解题方法
10 . 锌电解阳极泥(主要成分为 和
和 ,还有少量锰铅氧化物
,还有少量锰铅氧化物 和
和 )是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题:
)是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题: 易溶于水,不溶于乙醇
易溶于水,不溶于乙醇
②在较高温度及酸性催化条件下,葡萄糖能发生如图反应: 时
时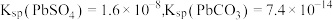
(1)已知 中
中 为
为 价,
价, 为
为 价和
价和 价,该氧化物中
价,该氧化物中 价和
价和 价
价 的物质的量之比为
的物质的量之比为_______ 。
(2)“还原酸浸”过程中主要反应的离子方程式为_______ ,该过程中实际葡萄糖加入量远大于理论需要量,其原因是_______ 。
(3)整个流程中可循环利用的物质是_______ (填名称)。获得 晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是
晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是_______ 。
(4)书写相关反应的离子方程式,并通过计算说明 时,可用
时,可用 溶液将“滤渣1”中的
溶液将“滤渣1”中的 完全转化为
完全转化为 的原因
的原因_______ 。
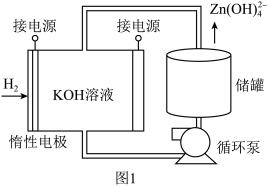
(5)通过氢电极增压法可制得单质锌,装置如图1所示。电解池工作时总反应的离子方程式为_______ 。 和
和 作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。
作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。
① 和
和 中
中 与
与 之间、
之间、 与
与 之间的离子键成分的百分数大小比较及解释
之间的离子键成分的百分数大小比较及解释_______ 。
② 晶胞结构如图2所示,其中
晶胞结构如图2所示,其中 代表
代表 。当
。当 位于晶胞的体心时,
位于晶胞的体心时, 于晶胞的
于晶胞的_______ 位置(填“顶点”“面心”“棱心”或“晶胞内”)。
 和
和 ,还有少量锰铅氧化物
,还有少量锰铅氧化物 和
和 )是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题:
)是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题: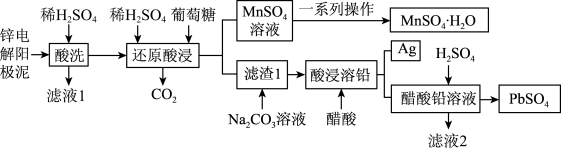
 易溶于水,不溶于乙醇
易溶于水,不溶于乙醇②在较高温度及酸性催化条件下,葡萄糖能发生如图反应:
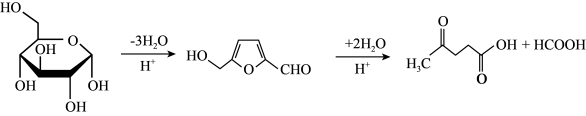
 时
时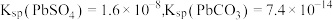
(1)已知
 中
中 为
为 价,
价, 为
为 价和
价和 价,该氧化物中
价,该氧化物中 价和
价和 价
价 的物质的量之比为
的物质的量之比为(2)“还原酸浸”过程中主要反应的离子方程式为
(3)整个流程中可循环利用的物质是
 晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是
晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是(4)书写相关反应的离子方程式,并通过计算说明
 时,可用
时,可用 溶液将“滤渣1”中的
溶液将“滤渣1”中的 完全转化为
完全转化为 的原因
的原因(5)通过氢电极增压法可制得单质锌,装置如图1所示。电解池工作时总反应的离子方程式为
 和
和 作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。
作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。①
 和
和 中
中 与
与 之间、
之间、 与
与 之间的离子键成分的百分数大小比较及解释
之间的离子键成分的百分数大小比较及解释②
 晶胞结构如图2所示,其中
晶胞结构如图2所示,其中 代表
代表 。当
。当 位于晶胞的体心时,
位于晶胞的体心时, 于晶胞的
于晶胞的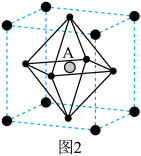
您最近半年使用:0次



