1 . 2024年3月初,中国新一代载人登月飞船命名为“梦舟”,月面着陆器命名为“揽月”,下列有关说法正确的是
| A.发射“梦舟”航天飞船的火箭发动机喷管套筒使用的T800碳纤维属于有机高分子材料 |
| B.“揽月”柔性太阳能板使用了国产新型高纯度二氧化硅,其性质稳定,是优良的光电材料 |
| C.新一代载人登月火箭应用液氧煤油发动机,煤油是烃及其含氧衍生物的混合物 |
| D.“梦舟”上用于电气管路隔热层的纳米二氧化硅不是胶体 |
您最近半年使用:0次
昨日更新
|
165次组卷
|
2卷引用:安徽师范大学附属中学2024届高三下学期5月测试化学试卷
名校
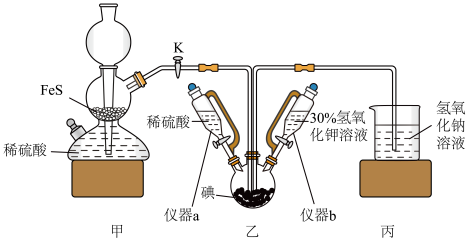
2 . 碘化钾用作制有机化合物及制药原料,医疗上用于防治甲状腺肿和甲状腺机能亢进的手术前准备,也可用作祛痰药。某实验室通过碘酸钾和硫化氢反应制备碘化钾。实验装置如图所示(夹持及加热装置已省略)回答下列问题:___________ ,实验中先关闭K,打开仪器___________ (填“a”、“b”或“ab”)制备碘酸钾,其反应的离子方程式为___________ 。某同学认为可以将甲装置中的 更换为粉末状
更换为粉末状 固体,你认为是否合理?
固体,你认为是否合理?___________ (填“合理”、“不合理”或“无法判断”)。
(2)乙装置中加入稀 的主要作用是
的主要作用是___________ 。
(3)如果乙装置最终生成 黄色沉淀,理论上可制得碘化钾的质量为
黄色沉淀,理论上可制得碘化钾的质量为___________ g。
(4)本实验尾气中的硫化氢可以用 溶液吸收,也可以用
溶液吸收,也可以用 溶液吸收。向
溶液吸收。向 溶液中通尾气直至饱和(
溶液中通尾气直至饱和( )时,溶液中刚好有
)时,溶液中刚好有 沉淀生成,此时溶液中
沉淀生成,此时溶液中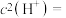
___________  (结果保留四位有效数字)。(已知
(结果保留四位有效数字)。(已知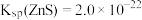 ,
, 的
的 ,
,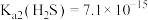 。)
。)
 更换为粉末状
更换为粉末状 固体,你认为是否合理?
固体,你认为是否合理?(2)乙装置中加入稀
 的主要作用是
的主要作用是(3)如果乙装置最终生成
 黄色沉淀,理论上可制得碘化钾的质量为
黄色沉淀,理论上可制得碘化钾的质量为(4)本实验尾气中的硫化氢可以用
 溶液吸收,也可以用
溶液吸收,也可以用 溶液吸收。向
溶液吸收。向 溶液中通尾气直至饱和(
溶液中通尾气直至饱和( )时,溶液中刚好有
)时,溶液中刚好有 沉淀生成,此时溶液中
沉淀生成,此时溶液中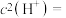
 (结果保留四位有效数字)。(已知
(结果保留四位有效数字)。(已知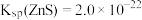 ,
, 的
的 ,
,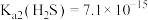 。)
。)
您最近半年使用:0次
名校
解题方法
3 . 我国最新型055型万吨驱逐舰上使用了最新一代国产有源相控阵雷达,采用了最先进的氮化镓( )半导体技术。某工厂利用铝土矿(主要成分为
)半导体技术。某工厂利用铝土矿(主要成分为 、
、 、
、 )为原料制备
)为原料制备 的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应,
的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应, 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 )半导体技术。某工厂利用铝土矿(主要成分为
)半导体技术。某工厂利用铝土矿(主要成分为 、
、 、
、 )为原料制备
)为原料制备 的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应,
的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应, 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是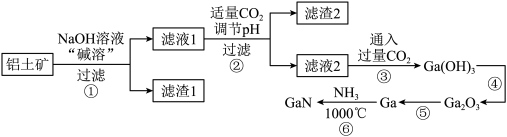
| A.可以通过粉碎铝土矿、搅拌等方法提高“碱溶”效率 |
B.由过程②、③可知, 的酸性比 的酸性比 强 强 |
C.已知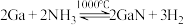 , , 与足量 与足量 反应,转移电子数为 反应,转移电子数为 |
D.滤渣1是 ,生成滤渣2的离子方程式可能为 ,生成滤渣2的离子方程式可能为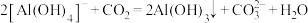 |
您最近半年使用:0次
4 . 锆是一种浅灰色金属,主要存在于海滨砂矿的矿床中,被用于核反应堆芯材料的制备,因此具有战略价值。某工厂以锆英砂(主要成分 ,同时含有
,同时含有 、
、 、
、 等元素)为原料生产金属锆工艺流程如下:
等元素)为原料生产金属锆工艺流程如下: 、
、 、
、 、
、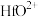 ;
;
②常温下弱碱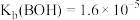 ,
,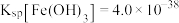 ;
;
③利用不同物质接近沸点时升华速度快的特点可以进行物质分离。
各物质沸点如下:
(1)“酸溶”步骤所得的溶液中 元素的化合价为
元素的化合价为___________ 。
(2)“萃取”步骤中含锆离子与萃取剂发生络合反应得到 ,写出反应的离子方程式:
,写出反应的离子方程式:___________ ;加入碱液 后,滤液中
后,滤液中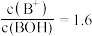 ,则滤液中
,则滤液中
___________  。
。
(3)“沸腾氯化”时金属元素转化为氯化物,同时得到一种还原性气体,写出 转化为
转化为 的化学方程式:
的化学方程式:___________ 。
(4) 沸点远高于
沸点远高于 的原因可能是
的原因可能是___________ ;“还原”的主要目的是___________ 。
(5)已知氧化锆和氧化钙形成某种亮紫色晶体,其晶胞如图所示,其中 位于面心位置。
位于面心位置。 周围最近的
周围最近的 原子个数为
原子个数为___________ 。
②该晶胞为立方晶胞,晶胞中 和
和 最小距离为
最小距离为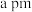 ,设
,设 为阿伏加德罗常数的值,
为阿伏加德罗常数的值, 的相对原子质量为M,该晶体密度是
的相对原子质量为M,该晶体密度是___________  (列出计算式即可)。
(列出计算式即可)。
 ,同时含有
,同时含有 、
、 、
、 等元素)为原料生产金属锆工艺流程如下:
等元素)为原料生产金属锆工艺流程如下: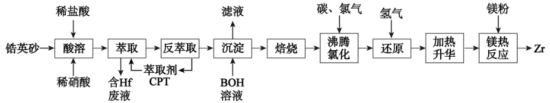
 、
、 、
、 、
、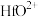 ;
;②常温下弱碱
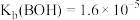 ,
,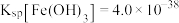 ;
;③利用不同物质接近沸点时升华速度快的特点可以进行物质分离。
各物质沸点如下:
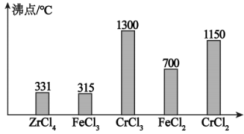
(1)“酸溶”步骤所得的溶液中
 元素的化合价为
元素的化合价为(2)“萃取”步骤中含锆离子与萃取剂发生络合反应得到
 ,写出反应的离子方程式:
,写出反应的离子方程式: 后,滤液中
后,滤液中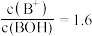 ,则滤液中
,则滤液中
 。
。(3)“沸腾氯化”时金属元素转化为氯化物,同时得到一种还原性气体,写出
 转化为
转化为 的化学方程式:
的化学方程式:(4)
 沸点远高于
沸点远高于 的原因可能是
的原因可能是(5)已知氧化锆和氧化钙形成某种亮紫色晶体,其晶胞如图所示,其中
 位于面心位置。
位于面心位置。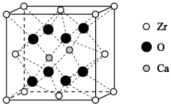
 周围最近的
周围最近的 原子个数为
原子个数为②该晶胞为立方晶胞,晶胞中
 和
和 最小距离为
最小距离为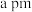 ,设
,设 为阿伏加德罗常数的值,
为阿伏加德罗常数的值, 的相对原子质量为M,该晶体密度是
的相对原子质量为M,该晶体密度是 (列出计算式即可)。
(列出计算式即可)。
您最近半年使用:0次
名校
5 . 已知 为阿伏伽德罗常数的值,下列说法正确的是
为阿伏伽德罗常数的值,下列说法正确的是
 为阿伏伽德罗常数的值,下列说法正确的是
为阿伏伽德罗常数的值,下列说法正确的是A. 环氧乙烷( 环氧乙烷(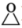 )中含有共价键数目约为 )中含有共价键数目约为 |
B.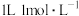 亚硫酸钠溶液中阴离子数目大于 亚硫酸钠溶液中阴离子数目大于 |
C.常温下, 乙二酸溶液的 乙二酸溶液的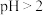 ,则含 ,则含 的数目大于 的数目大于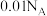 |
D.某样品中含有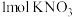 和少量 和少量 杂质,加水溶解后蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到的固体中离子数为 杂质,加水溶解后蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到的固体中离子数为 |
您最近半年使用:0次
名校
6 . 下列关于氨气的应用及性质说法正确的是
A.氨燃料动力集装箱船中氨气燃烧的化学方程式: |
B.足量的氨气和氯气反应,氧化剂和还原剂的物质的量之比为 |
C.氨气的中心原子采取 杂化,且氮原子提供空轨道与 杂化,且氮原子提供空轨道与 形成配位键 形成配位键 |
D.氨气可用于制备高能分子磷酰三叠氮,结构简式为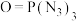 ,其分解产物 ,其分解产物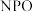 的电子式为 的电子式为 |
您最近半年使用:0次
名校
7 . 在473K、12159kPa下处理白磷(结构如图所示)得到斜方黑磷,继续增大压力,斜方黑磷还能转化为菱形黑磷(每层由曲折的磷原子链组成),设 为阿伏加德罗常数的值。下列说法中错误的是
为阿伏加德罗常数的值。下列说法中错误的是
 为阿伏加德罗常数的值。下列说法中错误的是
为阿伏加德罗常数的值。下列说法中错误的是
| A.白磷与黑磷属于磷元素的同素异形体 |
B. 中含有的中子数为 中含有的中子数为 |
C.12.4g白磷与0.6 mol H2在密闭容器中充分反应,生成的PH3分子数为 |
D.0.11mol白磷发生反应: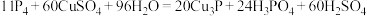 ,转移的电子数为 ,转移的电子数为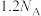 |
您最近半年使用:0次
名校
解题方法
8 . 下列化学用语表述正确的是
A. 的球棍模型: 的球棍模型: | B.NaClO的电子式为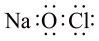 |
C.丁二烯的键线式: | D.基态Cr原子的价层电子轨道式: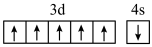 |
您最近半年使用:0次
名校
解题方法
9 . 实验室中利用固体 进行如图所示实验,下列说法错误的是
进行如图所示实验,下列说法错误的是
 进行如图所示实验,下列说法错误的是
进行如图所示实验,下列说法错误的是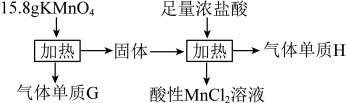
| A.气体G与气体H均为氧化产物 | B.实验中 既是氧化剂,又是还原剂 既是氧化剂,又是还原剂 |
| C.Mn元素至少参与了3个氧化还原反应 | D.G与H在标准状况下的总体积可能为5.6 L |
您最近半年使用:0次
名校
解题方法
10 . “宏观辨识与微观探析”是学科核心素养之一,下列离子方程式正确且符合题意的是
A.“84消毒液”具有漂白作用: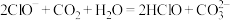 |
B.用铜片作电极,电解饱和食盐水: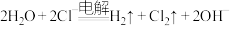 |
C.赤血盐溶液滴入FeSO4溶液中: |
D.向过量的NaHSO3溶液中滴加少量溴水: |
您最近半年使用:0次



