1 . 亚硝酸钠 是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是
是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是
 是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是
是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是A.滴定前滴定管尖嘴处有气泡,滴定后无气泡会使测得的 含量偏高 含量偏高 |
B.亚硝酸根( )空间结构为V形 )空间结构为V形 |
| C.酸性高锰酸钾溶液可以鉴别食盐和亚硝酸钠 |
D.滴定过程离子反应为: |
您最近一年使用:0次
2 . Romanenko利用微生物电池将 针催化还原的工作原理如图所示,下列说法正确的是
针催化还原的工作原理如图所示,下列说法正确的是
 针催化还原的工作原理如图所示,下列说法正确的是
针催化还原的工作原理如图所示,下列说法正确的是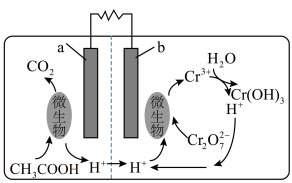
| A.b极电势比a极电势低 |
B.a极反应式: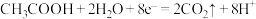 |
C.每处理1mol ,至少消耗 ,至少消耗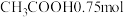 |
D.每生成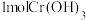 ,左池 ,左池 增加4mol 增加4mol |
您最近一年使用:0次
3 . 下列化学用语或表述正确的是
A. 的VSEPR模型为 的VSEPR模型为 |
B.Sc的原子结构示意图为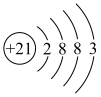 |
C.硼酸 的结构简式为 的结构简式为 |
D.等物质的量的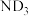 与 与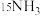 含有中子数前者多 含有中子数前者多 |
您最近一年使用:0次
4 . 课外实验可以帮助我们更好地学习化学知识。金属活动性强弱的探究过程如下,其中不正确的是(已知:白醋的水溶液显酸性,与稀盐酸的化学性质相似)
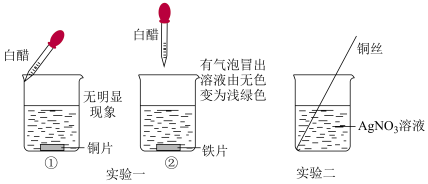
| A.实验一证明铁的金属活动性比铜强 |
| B.实验二的现象是铜丝不断减少,表面有银白色固体析出,无色溶液变为黄色 |
| C.实验一烧杯②中发生的是置换反应 |
| D.实验过程中存在不规范操作 |
您最近一年使用:0次
5 . 我国是铜业大国,氨法浸取工艺是铜矿提炼中常用方法,可实现废弃物“铜包钢”的有效分离,同时生产的CuCl可用于催化、医药、冶金等多种领域。工艺流程如下:
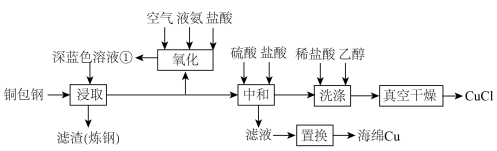
回答下列问题:
(1)首次浸取时所用深蓝色溶液①由细铜丝、足量液氨、空气和盐酸反应得到,其主要成分为___________ (填化学式),其配体的空间构型为___________ 。
(2)浸取工序的产物为 ,该工序发生反应的离子方程式为
,该工序发生反应的离子方程式为___________ 。
(3)浸取工序不宜超过40℃,其原因是___________ 。
(4)中和工序中主反应的离子方程式
___________ 。
(5)洗涤步骤中使用乙醇的优点有___________ 。
(6)选用真空干燥的原因___________ 。

回答下列问题:
(1)首次浸取时所用深蓝色溶液①由细铜丝、足量液氨、空气和盐酸反应得到,其主要成分为
(2)浸取工序的产物为
 ,该工序发生反应的离子方程式为
,该工序发生反应的离子方程式为(3)浸取工序不宜超过40℃,其原因是
(4)中和工序中主反应的离子方程式

(5)洗涤步骤中使用乙醇的优点有
(6)选用真空干燥的原因
您最近一年使用:0次
6 . 某课题组为探究0.1 的
的 与
与 溶液反应,进行了如下三个实验:
溶液反应,进行了如下三个实验:
实验一:
实验二: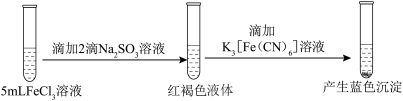
实验三: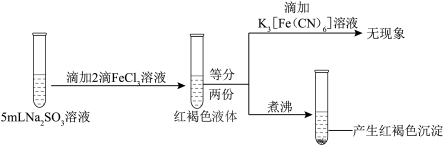
分析实验现象,下列说法中不合理的是
 的
的 与
与 溶液反应,进行了如下三个实验:
溶液反应,进行了如下三个实验:实验一:

实验二:

实验三:

分析实验现象,下列说法中不合理的是
| A.实验一的红褐色液体可产生丁达尔效应 |
B.实验二说明 既发生了水解反应也被 既发生了水解反应也被 还原 还原 |
C.实验三说明 发生了水解反应但未被还原 发生了水解反应但未被还原 |
D.以上三个实验说明 对 对 的水解无影响 的水解无影响 |
您最近一年使用:0次
7 . 已知:
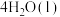
 ,设NA为阿伏伽德罗常数的数值。下列说法正确的是
,设NA为阿伏伽德罗常数的数值。下列说法正确的是

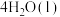
 ,设NA为阿伏伽德罗常数的数值。下列说法正确的是
,设NA为阿伏伽德罗常数的数值。下列说法正确的是A.0.1  溶液中含有NA个K+ 溶液中含有NA个K+ |
B.1mol  参与反应断裂的π键数目为NA 参与反应断裂的π键数目为NA |
C.反应每放出m kJ的热量,生成NA个 分子 分子 |
| D.每转移10NA个电子,产生CO2的体积标况下约为44.8L |
您最近一年使用:0次
8 . 向8 gCuO粉末中加入100 g稀H2SO4恰好完全反应。
(1)生成CuSO4的质量___________ 。
(2)稀H2SO4中溶质的质量分数___________ 。
(1)生成CuSO4的质量
(2)稀H2SO4中溶质的质量分数
您最近一年使用:0次
9 . 甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是

| A.t2℃时,甲、乙两物质的溶解度相等 |
| B.乙物质的溶解度大于甲物质的溶解度 |
| C.t2℃时,乙的饱和溶液降温至t1℃,乙溶液变为不饱和溶液 |
| D.t2C时,甲物质的饱和溶液降温至t1℃,溶液中溶质质量一定减小 |
您最近一年使用:0次
10 . 2022年北京冬奥会采用人工造雪,即先将水制成细小的冰片,储存于冷库;当需要雪花时,高压风机将冰片粉碎、吹出,就形成了晶莹剔透的雪花。下列有关说法正确的是

| A.水变成冰的过程中,水分子的大小改变了 |
| B.水制成冰片后,其中的水分子停止运动 |
| C.水和冰是由同种分子构成的,化学性质相同 |
| D.高压风机将冰片吹成雪花时,水分子分解了 |
您最近一年使用:0次



