1 . 下表是元素周期表的一部分,a~k分别代表10种元素,请按照要求回答:
(1)元素a~k中,其简单氢化物最稳定的是_______ (填元素名称)。
(2)b的简单氢化物的电子式_______ 。
(3)元素h、i的最高价氧化物对应水化物中酸性较强的是_______ (填化学式)。
(4)g的单质与e的最高价氧化物对应的水化物反应的化学方程式是_______ 。
(5)下列说法能证明金属性k强于f的是_______ (填序号)。
A.k的简单阳离子的氧化性更弱
B.k的氢氧化物水溶液的导电性更强
C.k的单质与水反应更剧烈
| a | ||||||||
| b | c | d | ||||||
| e | f | g | h | i | ||||
| k | …… | |||||||
(2)b的简单氢化物的电子式
(3)元素h、i的最高价氧化物对应水化物中酸性较强的是
(4)g的单质与e的最高价氧化物对应的水化物反应的化学方程式是
(5)下列说法能证明金属性k强于f的是
A.k的简单阳离子的氧化性更弱
B.k的氢氧化物水溶液的导电性更强
C.k的单质与水反应更剧烈
您最近一年使用:0次
2 . 现有A、B、X、Y、Z五种短周期主族元素,原子序数逐渐增大。它们的性质或原子结构如下表:
请回答:
(1)写出X在元素周期表中的位置_______ 。
(2)比较X、Y的离子半径:X的离子半径_______ Y的离子半径(填“>”“<”“=”)。
(3)检验BA3的方法和现象_______ 。
(4)用电子式表示化合物YZ的形成过程_______ 。
(5)W元素的核电荷数是B、X的核电荷数的和,则W与B的气态氢化物稳定性为_______ (填化学式)。
| 元素 | 性质或原子结构 |
| A | 原子核内只有一个质子 |
| B | 单质是空气中含量最多的气体 |
| X | 原子的最外层电子数是次外层电子数的3倍 |
| Y | 短周期元素中原子半径最大的元素 |
| Z | 最高正化合价与最低负化合价的代数和为6 |
(1)写出X在元素周期表中的位置
(2)比较X、Y的离子半径:X的离子半径
(3)检验BA3的方法和现象
(4)用电子式表示化合物YZ的形成过程
(5)W元素的核电荷数是B、X的核电荷数的和,则W与B的气态氢化物稳定性为
您最近一年使用:0次
3 . 氧化钙、氢氧化钙和碳酸钙是烟气脱硫理想的吸收剂,因而获得广泛应用。下列说法错误的是
| A.氧化钙是碱性氧化物 |
B.碱性: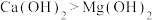 |
| C.碱石灰是烧碱、氧化钙的固体混合物,常用于干燥SO2 |
| D.燃煤中加入碳酸钙可以减少酸雨的形成 |
您最近一年使用:0次
4 . 中国古代文献和诗句中涉及许多化学知识。下列说法不正确 的是
| A.《天工开物》“凡石灰,经火焚炼为用”里的“石灰”是指碳酸钙 |
| B.“臣心一片磁针石,不指南方不肯休”中的磁针石主要成分是Fe3O4 |
| C.“爆竹声中一岁除,春风送暖入屠苏”中爆竹爆炸发生了化学反应 |
| D.“青蒿一握,以水二升渍,绞取法”,屠呦呦对青蒿素的提取属于化学变化 |
您最近一年使用:0次
5 . 化学是一门以实验为基础的自然科学。根据题意回答下列问题:
(1)在 溶液中逐滴滴入
溶液中逐滴滴入 溶液,观察到
溶液,观察到___________ (填“蓝色”或“红色”)的沉淀。
(2)铜和浓硫酸在加热时反应,产生无色刺激性气味的气体___________ (填化学式),能漂白___________ (填“蓝色”或“红色”)品红溶液。
(3)铜和浓硝酸反应剧烈,产生红棕色气体,离子方程式为___________ ;铜和稀硝酸反应缓慢,化学方程式为___________ ;对比现象可以说明浓硝酸的氧化性比稀硝酸___________ (填“强”或“弱”)。
(1)在
 溶液中逐滴滴入
溶液中逐滴滴入 溶液,观察到
溶液,观察到(2)铜和浓硫酸在加热时反应,产生无色刺激性气味的气体
(3)铜和浓硝酸反应剧烈,产生红棕色气体,离子方程式为
您最近一年使用:0次
6 . 下列各组离子能大量共存的是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
7 . 对于下列实验,能正确描述的离子方程式是
A.铁和足量的稀硝酸反应: |
B.向 溶液中滴加稀盐酸: 溶液中滴加稀盐酸: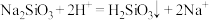 |
C.硅酸钠溶液与醋酸溶液混合: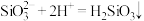 |
D. 溶液与 溶液与 溶液混合: 溶液混合: |
您最近一年使用:0次
8 . 设 为阿伏加德罗常数的值,下列判断正确的是
为阿伏加德罗常数的值,下列判断正确的是
 为阿伏加德罗常数的值,下列判断正确的是
为阿伏加德罗常数的值,下列判断正确的是A. 个NO分子的体积为 个NO分子的体积为 |
B.标准状况下,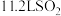 所含的原子数为 所含的原子数为 |
C. 与足量硝酸充分反应转移的电子数为 与足量硝酸充分反应转移的电子数为 |
D.含 个 个 分子的浓硫酸与足量铜反应可制得 分子的浓硫酸与足量铜反应可制得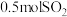 |
您最近一年使用:0次
名校
解题方法
9 . 立德粉(主要成分为BaSO4 ZnS)常用作颜料。以粗氧化锌(主要成分为ZnO,还含少量CuO、Fe3O4等杂质)和BaS为原料制备立德粉的流程如图所示:
ZnS)常用作颜料。以粗氧化锌(主要成分为ZnO,还含少量CuO、Fe3O4等杂质)和BaS为原料制备立德粉的流程如图所示:___________ 。
(2)加入H2O2发生反应的离子方程式为___________ 。
(3)分离出Fe(OH)3的实验操作名称为___________ 。
(4)“除杂Ⅱ”中加入过量的锌粉主要除去___________ (填离子符号),该反应的反应类型为___________ 。
(5)“滤渣”的成分是___________ 。
(6)8.34 g绿矾(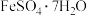 )晶体样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示:
)晶体样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示: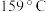 时固体N的化学式为
时固体N的化学式为___________ ,取适量  时所得的样品P,隔绝空气加热至
时所得的样品P,隔绝空气加热至 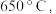 得到一种红棕色固体物质Q ,同时有两种无色气体生成,请写出该反应的化学方程式
得到一种红棕色固体物质Q ,同时有两种无色气体生成,请写出该反应的化学方程式___________ 。
 ZnS)常用作颜料。以粗氧化锌(主要成分为ZnO,还含少量CuO、Fe3O4等杂质)和BaS为原料制备立德粉的流程如图所示:
ZnS)常用作颜料。以粗氧化锌(主要成分为ZnO,还含少量CuO、Fe3O4等杂质)和BaS为原料制备立德粉的流程如图所示: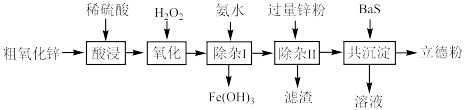
(2)加入H2O2发生反应的离子方程式为
(3)分离出Fe(OH)3的实验操作名称为
(4)“除杂Ⅱ”中加入过量的锌粉主要除去
(5)“滤渣”的成分是
(6)8.34 g绿矾(
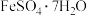 )晶体样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示:
)晶体样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示: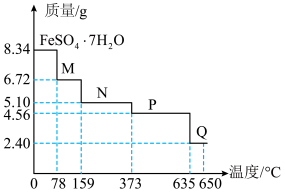
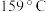 时固体N的化学式为
时固体N的化学式为 时所得的样品P,隔绝空气加热至
时所得的样品P,隔绝空气加热至 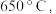 得到一种红棕色固体物质Q ,同时有两种无色气体生成,请写出该反应的化学方程式
得到一种红棕色固体物质Q ,同时有两种无色气体生成,请写出该反应的化学方程式
您最近一年使用:0次
2024-05-22更新
|
220次组卷
|
2卷引用:安徽省淮北市龙兴中学2023-2024学年高一上学期期末化学试卷
名校
10 . 为测定Cu和Cu2O混合粉末中Cu的含量。某同学将44.8g Cu和Cu2O混合粉末加入500mL 4.5mol/L的稀硝酸中,得到6.72LNO(标准状况下),忽略溶液体积的变化。下列说法正确的是
| A.反应后有固体剩余 | B.混合粉末中Cu的质量分数约为37% |
| C.反应后的溶液中c(Cu2+)=1.2mol/L | D.在反应后的溶液中加入足量铁粉,可置换出41.6g Cu |
您最近一年使用:0次



