1 . 下列指定反应的离子方程式书写正确的是
A.向氯化钡溶液中通入 气体: 气体: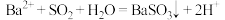 |
B.食醋去除水垢中的 |
C. 使溴水褪色: 使溴水褪色: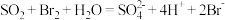 |
D.向 溶液中加入过量 溶液中加入过量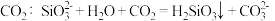 |
您最近一年使用:0次
解题方法
2 . 计算题本题要求写计算过程。
(1)计算出 的物质的量为
的物质的量为___________ 。
(2)配置 溶液,需要NaOH是多少?
溶液,需要NaOH是多少?___________
(1)计算出
 的物质的量为
的物质的量为(2)配置
 溶液,需要NaOH是多少?
溶液,需要NaOH是多少?
您最近一年使用:0次
3 . 化学是一门实用性很强的学科,请根据要求完成下列问题。
(1)钠有多种化合物,其中俗称“纯碱”的是___________ (填“ ”或“
”或“ ”)。
”)。
(2)铁有多种氧化物,其中为黑色且具有磁性的是___________ (填“ ”或“
”或“ ”)。
”)。
(3)日常生活中,活泼的铝在空气中能稳定存在的原因是表层的铝在空气中反应生成了___________ [填“ ”或“
”或“ ”],保护内层金属。
”],保护内层金属。
(4)铝与氢氧化钠溶液反应的离子方程式为___________ 。
(5)铁与水蒸气反应的化学方程式为___________ 。
(6)简述检验 的实验操作
的实验操作___________ 。
(1)钠有多种化合物,其中俗称“纯碱”的是
 ”或“
”或“ ”)。
”)。(2)铁有多种氧化物,其中为黑色且具有磁性的是
 ”或“
”或“ ”)。
”)。(3)日常生活中,活泼的铝在空气中能稳定存在的原因是表层的铝在空气中反应生成了
 ”或“
”或“ ”],保护内层金属。
”],保护内层金属。(4)铝与氢氧化钠溶液反应的离子方程式为
(5)铁与水蒸气反应的化学方程式为
(6)简述检验
 的实验操作
的实验操作
您最近一年使用:0次
解题方法
4 . 回答下列问题。
(1)氢氧化亚铁与氧气、水的反应方程式为:___________ 。
(2)钠通常保存在___________ 中,加热时,钠可以在空气中燃烧发出___________ 火焰,生成___________ 色固体。
(3)写出氯气和水反应的化学方程式:___________ 。
(4)电离:电解质溶于水或受热熔化时,形成___________ 的过程。
(5) 、
、 、
、 、
、 、
、 、
、 中,
中,___________ 和___________ 互为同位素,___________ 和___________ 的中子数相等,但质子数不等,所以不是同一种元素。
(6)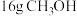 的物质的量是
的物质的量是___________ ,含H原子的数目为___________ 。
(1)氢氧化亚铁与氧气、水的反应方程式为:
(2)钠通常保存在
(3)写出氯气和水反应的化学方程式:
(4)电离:电解质溶于水或受热熔化时,形成
(5)
 、
、 、
、 、
、 、
、 、
、 中,
中,(6)
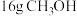 的物质的量是
的物质的量是
您最近一年使用:0次
解题方法
5 . 雷雨天 转化为
转化为 的流程为:
的流程为: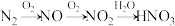
(1) 转化为NO的化学方程式是“
转化为NO的化学方程式是“_____ 。”
(2)NO转化为 的化学方程式是“
的化学方程式是“_____ 。”
(3) 转化为
转化为 的化学方程式是“
的化学方程式是“_____ 。”
 转化为
转化为 的流程为:
的流程为: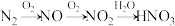
(1)
 转化为NO的化学方程式是“
转化为NO的化学方程式是“(2)NO转化为
 的化学方程式是“
的化学方程式是“(3)
 转化为
转化为 的化学方程式是“
的化学方程式是“
您最近一年使用:0次
6 . 写成电离方程式。
(1) =
=___________ 。
(2)HNO3=___________ 。
(1)
 =
=(2)HNO3=
您最近一年使用:0次
名校
解题方法
7 . 实验小组同学欲探究 的性质并测定空气中
的性质并测定空气中 的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。
的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。_______ 。
(2)装置E的作用是_______ 。(用离子方程式表示)
(3)装置D用于验证 的
的_______ 性,发生的化学方程式为_______ 。
(4)装置C中的现象是_______ ;若将C中的溴水改为酸性高锰酸钾溶液,现象为_______ ,发生的离子方程式为_______ 。
(5)如果用硫酸溶液和 固体反应制取
固体反应制取 装置如图所示。其中a导管的作用是
装置如图所示。其中a导管的作用是_______ 。 含量(假设空气中无其他还原性气体)。
含量(假设空气中无其他还原性气体)。

实验中若通过空气的体积为 (标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是
(标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是_______ 。(结果精确到0.001%)
 的性质并测定空气中
的性质并测定空气中 的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。
的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。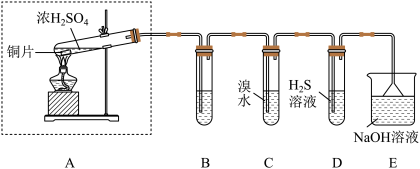
(2)装置E的作用是
(3)装置D用于验证
 的
的(4)装置C中的现象是
(5)如果用硫酸溶液和
 固体反应制取
固体反应制取 装置如图所示。其中a导管的作用是
装置如图所示。其中a导管的作用是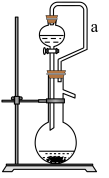
 含量(假设空气中无其他还原性气体)。
含量(假设空气中无其他还原性气体)。
实验中若通过空气的体积为
 (标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是
(标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是
您最近一年使用:0次
名校
8 . 依据如图中氮元素及其化合物的转化关系,回答问题:_______ 。
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为:_______ 。
②下列试剂用于干燥NH3的是_______ (填字母)。
A.浓硫酸 B.碱石灰 C.氯化钙固体
③氨气是重要的化工原料,可用于工业制硝酸,写出氨气催化氧化的化学方程式:_______ 。
(3)回答下列关于NO、NO2的问题:
①汽车尾气中的CO、NOx在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO2被CO还原的化学方程式:_______ 。
②用氨可将氮氧化物转化为无毒气体。如 ,该反应中,被氧化的物质是
,该反应中,被氧化的物质是_______ (填化学式),若反应中生成1molN2,则转移电子_______ mol。
(4)工业生产中利用氨水吸收SO2和NO2,原理如图所示:_______ 。
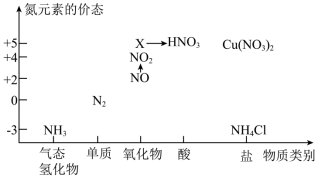
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为:
②下列试剂用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.氯化钙固体
③氨气是重要的化工原料,可用于工业制硝酸,写出氨气催化氧化的化学方程式:
(3)回答下列关于NO、NO2的问题:
①汽车尾气中的CO、NOx在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO2被CO还原的化学方程式:
②用氨可将氮氧化物转化为无毒气体。如
 ,该反应中,被氧化的物质是
,该反应中,被氧化的物质是(4)工业生产中利用氨水吸收SO2和NO2,原理如图所示:
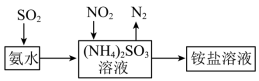
您最近一年使用:0次
9 . 针对表中10种元素及由这些元素形成的单质和化合物,用元素符号或者化学式填写以下空格。
(1)最活泼的金属元素是___________ ,最活泼的非金属元素是___________ ,最不活泼的元素是___________ 。
(2)碱性最强的最高价氧化物对应水化物是___________ ,酸性最强的最高价氧化物对应水化物是___________ ,最稳定的气态氢化物是___________ 。
(3)在④与⑤中,还原性较强的是___________ ,在⑧与⑨的单质中,氧化性较强的是___________ 。
(4)④的最高价氧化物对应的水化物和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:___________ ;用电子式表示④和⑧形成的化合物的形成过程___________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
(2)碱性最强的最高价氧化物对应水化物是
(3)在④与⑤中,还原性较强的是
(4)④的最高价氧化物对应的水化物和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:
您最近一年使用:0次
10 . a.有下列物质:①氢氧化钡 ②KHSO4 ③液态HCl ④稀硫酸 ⑤二氧化碳 ⑥铜 ⑦碳酸钠 ⑧蔗糖
请回答下列问题:
(1)属于电解质的有___________ (填序号)
(2)属于非电解质的有___________ (填序号)
b.某同学用如下实验探究 、
、 的性质。请回答下列问题:
的性质。请回答下列问题:
(3)在FeCl3溶液中需加入少量铁屑,发生反应的化学方程式为___________ 。FeCl3溶液,加入1滴___________ 溶液,溶液变___________ 。
(4)FeCl2溶液与氯水反应的化学方程式为___________ 。
(5)某同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程___________ 。
c.请回答下列问题:
(6)0.5 mol H2O含有H的物质的量___________ mol。含有O数目___________ 。
(7)100 mL 0.2 mol/L Na2SO4溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
(8)标准状况下11.2 L的CO2的物质的量是___________ mol。
请回答下列问题:
(1)属于电解质的有
(2)属于非电解质的有
b.某同学用如下实验探究
 、
、 的性质。请回答下列问题:
的性质。请回答下列问题:(3)在FeCl3溶液中需加入少量铁屑,发生反应的化学方程式为
(4)FeCl2溶液与氯水反应的化学方程式为
(5)某同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程
c.请回答下列问题:
(6)0.5 mol H2O含有H的物质的量
(7)100 mL 0.2 mol/L Na2SO4溶液中
 的物质的量浓度为
的物质的量浓度为(8)标准状况下11.2 L的CO2的物质的量是
您最近一年使用:0次



