名校
1 . 能源是现代社会物质文明的原动力,与我们每个人息息相关。
 .人们常利用化学反应中的能量变化为人类服务。
.人们常利用化学反应中的能量变化为人类服务。
(1)化石燃料是人类利用最多的能源,为促进社会可持续发展,人类不断地寻找更多新能源,例如:___________ 、___________ (任意书写两种新能源)。
 .已知31g白磷变为31g红磷释放能量。
.已知31g白磷变为31g红磷释放能量。
(2)上述变化属于___________ (填“物理”或“化学”)变化。
(3)常温常压下,白磷与红磷更稳定的是___________ 。
 .人们常利用化学反应中的能量变化为人类服务。
.人们常利用化学反应中的能量变化为人类服务。(1)化石燃料是人类利用最多的能源,为促进社会可持续发展,人类不断地寻找更多新能源,例如:
 .已知31g白磷变为31g红磷释放能量。
.已知31g白磷变为31g红磷释放能量。(2)上述变化属于
(3)常温常压下,白磷与红磷更稳定的是
您最近一年使用:0次
名校
2 . 氧化还原反应原理在研究物质性质及物质转化等方面具有重要的价值。回答下列问题:
(1)按照不同的分类方法将下列化学反应进行分类。
a. ;b.
;b. ;c.
;c.
d. ;e.
;e.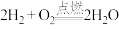 。
。
其中属于氧化还原反应,但不属于四大基本反应类型的是______ (填字母)。
(2)亚硝酸钠( )具有致癌作用,许多腌制食品中含
)具有致癌作用,许多腌制食品中含 。酸性
。酸性 溶液与
溶液与 反应的化学方程式为
反应的化学方程式为 ,将它改写为离子方程式并用双线桥表示电子转移的方向和数目:
,将它改写为离子方程式并用双线桥表示电子转移的方向和数目:______ 。
(3)新储氢材料—碳纳米管可利用电弧法合成,合成过程中会伴随大量的碳纳米颗粒杂质,这种碳纳米颗粒杂质可用氧化气化法提纯,反应方程式为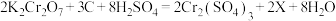

①该反应中,生成物X的化学式为______ 。
②该反应中,氧化剂为______ (填化学式),被氧化的元素为______ (填元素符号)。
③该反应中, 表现出
表现出______ (填字母)
A.酸性 B.还原性 C.氧化性
④该反应中,每生成3mol ,转移
,转移______ mol电子。
(1)按照不同的分类方法将下列化学反应进行分类。
a.
 ;b.
;b. ;c.
;c.
d.
 ;e.
;e.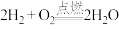 。
。其中属于氧化还原反应,但不属于四大基本反应类型的是
(2)亚硝酸钠(
 )具有致癌作用,许多腌制食品中含
)具有致癌作用,许多腌制食品中含 。酸性
。酸性 溶液与
溶液与 反应的化学方程式为
反应的化学方程式为 ,将它改写为离子方程式并用双线桥表示电子转移的方向和数目:
,将它改写为离子方程式并用双线桥表示电子转移的方向和数目:(3)新储氢材料—碳纳米管可利用电弧法合成,合成过程中会伴随大量的碳纳米颗粒杂质,这种碳纳米颗粒杂质可用氧化气化法提纯,反应方程式为
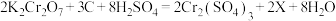

①该反应中,生成物X的化学式为
②该反应中,氧化剂为
③该反应中,
 表现出
表现出A.酸性 B.还原性 C.氧化性
④该反应中,每生成3mol
 ,转移
,转移
您最近一年使用:0次
名校
解题方法
3 . 下表列出了①~⑩十种元素在周期表中的位置:
请按要求回答下列问题:
(1)上述元素中,金属性最强的是______ (填元素名称),最高价氧化物对应水化物酸性最强的是______ (填化学式)
(2)由元素③形成的单质的结构式为______ ,由元素⑥和⑨形成化合物乙,请用电子式表示物质乙的形成过程______ 。
(3)由元素①、③、④、⑧形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为______ 。
(4)可以比较⑤、⑥两元素金属性强弱的实验是______。
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
4 | ⑩ |
(1)上述元素中,金属性最强的是
(2)由元素③形成的单质的结构式为
(3)由元素①、③、④、⑧形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为
(4)可以比较⑤、⑥两元素金属性强弱的实验是______。
| A.比较这两种元素最高价氧化物对应的水化物的碱性 |
| B.将⑤的单质投入到⑥的盐溶液中 |
| C.将这两种元素的单质分别放入冷水中 |
| D.比较这两种元素的单质与酸反应时失电子的数目 |
您最近一年使用:0次
名校
解题方法
4 . 重铬酸钾是一种重要的化工原料,可由铬铁矿(主要成分为 ,还含有硅、铝的氧化物等杂质)制备,流程如图所示:
,还含有硅、铝的氧化物等杂质)制备,流程如图所示: 主要以
主要以 形式存在,加入酸会转为
形式存在,加入酸会转为 。
。
Ⅱ.有关物质的溶解度如图所示:______ (任写一条)。
(2)步骤①中主要反应为: ,上述反应配平后
,上述反应配平后 与
与 的系数比为
的系数比为______ 。
(3)滤渣1中含量最多的金属元素是______ ,滤渣2的主要成分是Y及含硅杂质。向滤液1通入过量 得到Y的离子方程式为
得到Y的离子方程式为______ 。
(4)步骤④将滤液2的pH调小的原因是______ (结合离子方程式和文字表述说明)。
(5)向“滤液3”中加入适量KCl,经过操作X后得到 固体。操作X为:
固体。操作X为:______ ,过滤、洗涤、干燥。
(6)某工厂用448kg铬铁矿粉( 的含量为80%)制备
的含量为80%)制备 ,最终得到产品182.4kg,则
,最终得到产品182.4kg,则 的产率为
的产率为______ %。
 ,还含有硅、铝的氧化物等杂质)制备,流程如图所示:
,还含有硅、铝的氧化物等杂质)制备,流程如图所示:
 主要以
主要以 形式存在,加入酸会转为
形式存在,加入酸会转为 。
。Ⅱ.有关物质的溶解度如图所示:

(2)步骤①中主要反应为:
 ,上述反应配平后
,上述反应配平后 与
与 的系数比为
的系数比为(3)滤渣1中含量最多的金属元素是
 得到Y的离子方程式为
得到Y的离子方程式为(4)步骤④将滤液2的pH调小的原因是
(5)向“滤液3”中加入适量KCl,经过操作X后得到
 固体。操作X为:
固体。操作X为:(6)某工厂用448kg铬铁矿粉(
 的含量为80%)制备
的含量为80%)制备 ,最终得到产品182.4kg,则
,最终得到产品182.4kg,则 的产率为
的产率为
您最近一年使用:0次
名校
5 . 下列各组离子在相应的条件下可能大量共存的是
A.透明溶液中: 、 、 、 、 、 、 |
B.能使酚酞变红的溶液中: 、 、 、 、 、 、 |
C.在 盐酸中: 盐酸中: 、 、 、 、 、 、 |
D.能与Al反应放出 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
6 . 含硫化合物的反应具有多样性。下列反应的离子方程式书写正确的是
A.硫化钠溶液和硝酸反应: |
B.将 通入 通入 溶液: 溶液: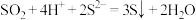 |
C.用 溶液吸收少量 溶液吸收少量 : : |
D.将等物质的量浓度的 和 和 溶液以体积比1∶2混合: 溶液以体积比1∶2混合: |
您最近一年使用:0次
名校
7 .  为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.0.1mol 含有电子数为 含有电子数为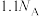 |
B.6.4gCu与0.1molS充分反应,转移电子数为 |
C.常温下,2.7g铝粉与足量浓硝酸反应,转移电子数为 |
D.1L 氨水中含有 氨水中含有 和 和 的数目之和为 的数目之和为 |
您最近一年使用:0次
8 . 用 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是
 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是A.18g重水( )中含有的质子数为10 )中含有的质子数为10 |
B.6.4g Cu在硫蒸气中完全反应,转移电子数为0.1 |
C.3mol  与水完全反应,转移电子数为4 与水完全反应,转移电子数为4 |
D.1mol  与0.5mol 与0.5mol  充分反应,生成 充分反应,生成 分子数为 分子数为 |
您最近一年使用:0次
解题方法
9 . 下列离子方程式书写正确的是
A.将Fe溶于足量稀硝酸: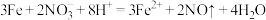 |
B.向 溶液中通入 溶液中通入 气体: 气体: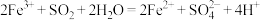 |
C.水玻璃溶液中通入过量 : : |
D. 溶液中加入足量的氨水: 溶液中加入足量的氨水: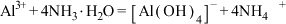 |
您最近一年使用:0次
10 . 在无色透明溶液中,下列各组离子能大量共存的是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次



