1 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.22.4LCH4分子中含有10NA个电子 |
| B.16gCH4分子中含有4NA个C-H |
| C.等体积的CH4和NH3所含氢原子数之比为4∶3 |
| D.等质量的CH4和HF所含共价键数目之比为4∶1 |
您最近一年使用:0次
2 . 下列离子方程式书写正确的是
A.稀硫酸和 溶液反应: 溶液反应: |
B.过量的 通入 通入 溶液中: 溶液中: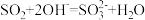 |
C.铜片在加热条件下与浓硫酸反应: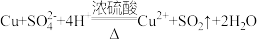 |
D. 使溴水褪色: 使溴水褪色: |
您最近一年使用:0次
3 . 能正确表示下列反应的离子方程式是
A.向澄清的石灰水中通入少量 气体 气体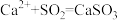 |
B.过量 气体通入氢氧化钠溶液中 气体通入氢氧化钠溶液中 |
C. 气体通入溴水中 气体通入溴水中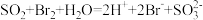 |
D.氢硫酸中通入氯气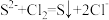 |
您最近一年使用:0次
4 . 下列实验结论与实验现象相符合的一组是
选项 | 实验 | 现象 | 结论 |
A | 向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液 | 先变橙色,后变蓝色 | 氧化性: |
B | 向品红溶液中通入某气体 | 品红褪色 | 气体一定是 |
C | 向蔗糖中滴加浓硫酸 | 蔗糖变黑 | 浓硫酸具有吸水性 |
D | 向某盐溶液中加入浓NaOH溶液,加热 | 产生的气体能使湿润的红色石蕊试纸变蓝 | 原溶液中一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
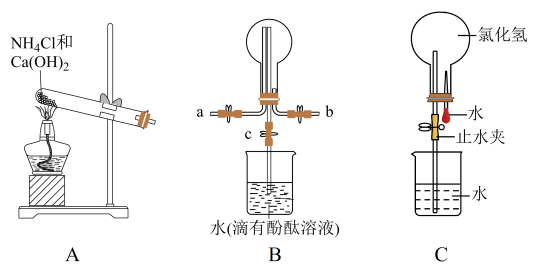
5 . 某化学实验小组同学利用如图所示装置制备氨气,并探究氨气的性质(部分仪器已略去)。_______ 。
(2)干燥氨气常用的干燥剂是_______ 。
a. b.浓硫酸 c.
b.浓硫酸 c. d.碱石灰
d.碱石灰
(3)收集氨气时,请你选择氨气的进气口_______ (填“a”或“b”)。
(4)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是_______ 。
(5)用图C装置进行喷泉实验,上部烧瓶已装满氯化氢,引发水上喷的操作是_______ 。
(6)下列装置用于 尾气处理较合适的是
尾气处理较合适的是_______ 。 等氮氧化物的尾气排出,为消除它们对环境的破坏作用,目前应用最广泛的烟气氮氧化物脱除技术是
等氮氧化物的尾气排出,为消除它们对环境的破坏作用,目前应用最广泛的烟气氮氧化物脱除技术是 催化还原氮氧化物技术。反应原理如图所示。当
催化还原氮氧化物技术。反应原理如图所示。当 与NO的物质的量之比为1:1时,与足量氨气在一定条件下发生反应。当有18mol电子发生转移时,将有
与NO的物质的量之比为1:1时,与足量氨气在一定条件下发生反应。当有18mol电子发生转移时,将有_______ 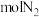 生成。
生成。
(2)干燥氨气常用的干燥剂是
a.
 b.浓硫酸 c.
b.浓硫酸 c. d.碱石灰
d.碱石灰(3)收集氨气时,请你选择氨气的进气口
(4)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是
(5)用图C装置进行喷泉实验,上部烧瓶已装满氯化氢,引发水上喷的操作是
(6)下列装置用于
 尾气处理较合适的是
尾气处理较合适的是
 等氮氧化物的尾气排出,为消除它们对环境的破坏作用,目前应用最广泛的烟气氮氧化物脱除技术是
等氮氧化物的尾气排出,为消除它们对环境的破坏作用,目前应用最广泛的烟气氮氧化物脱除技术是 催化还原氮氧化物技术。反应原理如图所示。当
催化还原氮氧化物技术。反应原理如图所示。当 与NO的物质的量之比为1:1时,与足量氨气在一定条件下发生反应。当有18mol电子发生转移时,将有
与NO的物质的量之比为1:1时,与足量氨气在一定条件下发生反应。当有18mol电子发生转移时,将有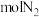 生成。
生成。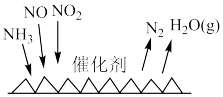
您最近一年使用:0次
名校
6 . “以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为 )吸收烟气中的
)吸收烟气中的 ,得到亚硫酸钠
,得到亚硫酸钠 粗品。其流程如下。
粗品。其流程如下。 的溶解,可采取的措施是
的溶解,可采取的措施是_______ (写出一种即可)。
(2)过程①进行的操作是_______ 。
(3)上述流程中;通入“含 的烟气”,发生反应的化学方程式为
的烟气”,发生反应的化学方程式为_______ 。
(4)上述流程中,加入NaOH后,发生反应的离子方程式为_______ 。
(5)设计实验证明亚硫酸钠粗品含有少量 的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,
的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,_______ ,出现白色沉淀,则证明含有 。
。
(6) 可用于处理酸性废水中的
可用于处理酸性废水中的 (转化为
(转化为 ),发生反应的离子方程式为
),发生反应的离子方程式为_______ 。
(7)某化工厂用如图所示工艺流程吸收烟气中的 。在标准状况下,当除去
。在标准状况下,当除去 时,消耗
时,消耗 的物质的量为
的物质的量为_______ mol。
 )吸收烟气中的
)吸收烟气中的 ,得到亚硫酸钠
,得到亚硫酸钠 粗品。其流程如下。
粗品。其流程如下。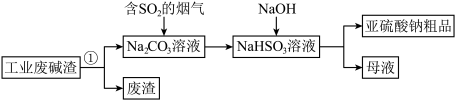
 的溶解,可采取的措施是
的溶解,可采取的措施是(2)过程①进行的操作是
(3)上述流程中;通入“含
 的烟气”,发生反应的化学方程式为
的烟气”,发生反应的化学方程式为(4)上述流程中,加入NaOH后,发生反应的离子方程式为
(5)设计实验证明亚硫酸钠粗品含有少量
 的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,
的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解, 。
。(6)
 可用于处理酸性废水中的
可用于处理酸性废水中的 (转化为
(转化为 ),发生反应的离子方程式为
),发生反应的离子方程式为(7)某化工厂用如图所示工艺流程吸收烟气中的
 。在标准状况下,当除去
。在标准状况下,当除去 时,消耗
时,消耗 的物质的量为
的物质的量为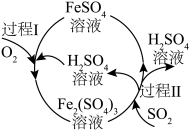
您最近一年使用:0次
名校
7 . 取纯净的 固体3.44g进行加热,测得固体质量随温度的变化情况如图所示。D~E阶段反应生成的气体能使品红溶液褪色,是形成酸雨的主要物质之一、下列说法错误的是
固体3.44g进行加热,测得固体质量随温度的变化情况如图所示。D~E阶段反应生成的气体能使品红溶液褪色,是形成酸雨的主要物质之一、下列说法错误的是
 固体3.44g进行加热,测得固体质量随温度的变化情况如图所示。D~E阶段反应生成的气体能使品红溶液褪色,是形成酸雨的主要物质之一、下列说法错误的是
固体3.44g进行加热,测得固体质量随温度的变化情况如图所示。D~E阶段反应生成的气体能使品红溶液褪色,是形成酸雨的主要物质之一、下列说法错误的是
A.C点固体的化学式是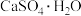 | B.D~E阶段还生成了 |
| C.E点固体物质为CaO | D. 随温度的升高,分三个阶段失去结晶水 随温度的升高,分三个阶段失去结晶水 |
您最近一年使用:0次
名校
8 . 下表列出了①~⑧所分别代表的八种元素在周期表中的位置,按要求填写下列问题:
(1)①~⑧八种元素中金属性最强的元素是_______ (填元素符号)。
(2)元素②与①组成的某化合物,其分子为18电子体,分子中两种元素原子个数的最简比为1:2,则该分子的电子式为_______ 。
(3)元素⑧的原子结构示意图为_______ 。
(4)Mg和元素⑤的单质作电极材料,氢氧化钠溶液作电解质溶液,能设计成原电池,则该电池负极反应式为_______ 。
(5)写出碳单质与元素②最高价氧化物对应水化物的浓溶液反应的化学方程式_______ 。
(6)第118号元素与⑥为同族元素,它位于元素周期表第_______ 周期。
周期 族 | IA | 0 | ||||||
1 | ① | lIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ② | ③ | ||||||
3 | ④ | ⑤ | ⑥ | |||||
4 | ⑦ | ⑧ |
(2)元素②与①组成的某化合物,其分子为18电子体,分子中两种元素原子个数的最简比为1:2,则该分子的电子式为
(3)元素⑧的原子结构示意图为
(4)Mg和元素⑤的单质作电极材料,氢氧化钠溶液作电解质溶液,能设计成原电池,则该电池负极反应式为
(5)写出碳单质与元素②最高价氧化物对应水化物的浓溶液反应的化学方程式
(6)第118号元素与⑥为同族元素,它位于元素周期表第
您最近一年使用:0次
名校
9 . 下列离于反应方程式正确的是
A.铜与浓硫酸反应制取 : : |
B. 与稀硝酸反应制取 与稀硝酸反应制取 : : |
C.向 溶液中通入等物质的量的 溶液中通入等物质的量的 : :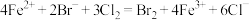 |
D. 与稀硫酸混合后溶液变浑浊: 与稀硫酸混合后溶液变浑浊: |
您最近一年使用:0次
名校
10 . 下列各组离子在指定溶液中一定能大量共存的是
A.加入Al粉能产生 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B. (酸性)的溶液中: (酸性)的溶液中: 、 、 、 、 、 、 |
C.滴加硫氰化钾变为血红色的溶液中: 、 、 、 、 、 、 |
D.能使蓝色石蕊试纸变红的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次



