1 . 锆( )是一种重要的战略金属。一种以氧氯化锆(主要含
)是一种重要的战略金属。一种以氧氯化锆(主要含 ,还含有少量
,还含有少量 、
、 等元素)为原料生产金属锆的工艺流程如下:
等元素)为原料生产金属锆的工艺流程如下: 、
、 、
、 ;
;
② 时,
时, ,
, ;
;
③“还原”前后相关物质沸点如下:
回答下列问题:
(1) 是
是 的同族相邻元素,基态
的同族相邻元素,基态 原子的价电子排布式是
原子的价电子排布式是___________ 。
(2) 通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的
通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的 ,再以盐酸酸化得到
,再以盐酸酸化得到 ,写出酸化过程的离子方程式
,写出酸化过程的离子方程式___________ 。
(3)“沉淀”后,废液中 ,则废液中
,则废液中 为
为___________  。
。
(4)“沸腾氯化”时, 转化为
转化为 ,同时生成一种还原性气体,该反应的化学方程式为
,同时生成一种还原性气体,该反应的化学方程式为___________ 。
(5)①气态 通常以二聚体
通常以二聚体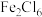 的形式存在,分子结构为
的形式存在,分子结构为 ,二聚体中
,二聚体中 的杂化轨道类型为
的杂化轨道类型为___________ 。 易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为
易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为___________ 。
②“还原”的主要目的是___________ 。
(6)下列金属冶炼方法与本工艺流程中加入 冶炼
冶炼 的方法相似的是___________
的方法相似的是___________
(7)实验室可以用络合滴定法快速测定“酸浸”溶液中锆的含量,步骤如下:___________ ,继续摇动锥形瓶,观察溶液颜色变化。
②已知 与EDTA发生
与EDTA发生 络合反应,则酸浸液中含量(以
络合反应,则酸浸液中含量(以 计)为
计)为___________  。
。
 )是一种重要的战略金属。一种以氧氯化锆(主要含
)是一种重要的战略金属。一种以氧氯化锆(主要含 ,还含有少量
,还含有少量 、
、 等元素)为原料生产金属锆的工艺流程如下:
等元素)为原料生产金属锆的工艺流程如下: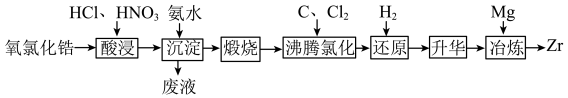
 、
、 、
、 ;
;②
 时,
时, ,
, ;
;③“还原”前后相关物质沸点如下:
| 物质 |  |  |  |  |  |
| 沸点 | 331 | 315 | 1300 | 700 | 1150 |
(1)
 是
是 的同族相邻元素,基态
的同族相邻元素,基态 原子的价电子排布式是
原子的价电子排布式是(2)
 通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的
通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的 ,再以盐酸酸化得到
,再以盐酸酸化得到 ,写出酸化过程的离子方程式
,写出酸化过程的离子方程式(3)“沉淀”后,废液中
 ,则废液中
,则废液中 为
为 。
。(4)“沸腾氯化”时,
 转化为
转化为 ,同时生成一种还原性气体,该反应的化学方程式为
,同时生成一种还原性气体,该反应的化学方程式为(5)①气态
 通常以二聚体
通常以二聚体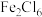 的形式存在,分子结构为
的形式存在,分子结构为 ,二聚体中
,二聚体中 的杂化轨道类型为
的杂化轨道类型为 易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为
易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为②“还原”的主要目的是
(6)下列金属冶炼方法与本工艺流程中加入
 冶炼
冶炼 的方法相似的是___________
的方法相似的是___________| A.高炉炼铁 | B.电解熔融氯化钠制钠 |
| C.铝热反应制锰 | D.氧化汞分解制汞 |
(7)实验室可以用络合滴定法快速测定“酸浸”溶液中锆的含量,步骤如下:

②已知
 与EDTA发生
与EDTA发生 络合反应,则酸浸液中含量(以
络合反应,则酸浸液中含量(以 计)为
计)为 。
。
您最近半年使用:0次
2 . 连二亚硫酸钠 俗称保险粉,是印染工业中常用的漂白剂。实验室制备流程如下:
俗称保险粉,是印染工业中常用的漂白剂。实验室制备流程如下:
 俗称保险粉,是印染工业中常用的漂白剂。实验室制备流程如下:
俗称保险粉,是印染工业中常用的漂白剂。实验室制备流程如下: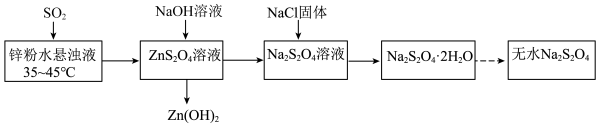
| A.将锌粉溶于水形成悬浊液可以提高反应速率 |
B.生成 的反应中氧化剂和还原剂物质的量之比为 的反应中氧化剂和还原剂物质的量之比为 |
C.温度超过 会导致 会导致 溶解度降低 溶解度降低 |
D.加入 有利于 有利于 析出,提高产率 析出,提高产率 |
您最近半年使用:0次
解题方法
3 . 下列离子方程式书写错误的是
A.向银氨溶液中滴入乙醛: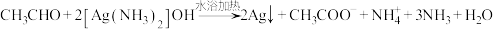 |
B.向硫代硫酸钠溶液中加入稀硫酸: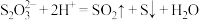 |
C.向漂白粉溶液中通入少量 : :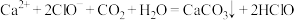 |
D.向加有 的 的 溶液中通入 溶液中通入 : :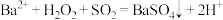 |
您最近半年使用:0次
4 . 用 与
与 制备纳米零价铁的反应为。设
制备纳米零价铁的反应为。设 为阿伏伽德罗常数的值,下列说法正确的是
为阿伏伽德罗常数的值,下列说法正确的是
 与
与 制备纳米零价铁的反应为。设
制备纳米零价铁的反应为。设 为阿伏伽德罗常数的值,下列说法正确的是
为阿伏伽德罗常数的值,下列说法正确的是A. 溶液中 溶液中 数为 数为 |
B.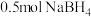 固体中 固体中 键数为 键数为 |
C.每生成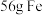 ,转移的电子数为 ,转移的电子数为 |
D. 中采取 中采取 杂化的原子数为 杂化的原子数为 |
您最近半年使用:0次
5 . 氯化亚铜(CuCl)广泛应用于有机合成,难溶于水和乙醇,在潮湿空气中易氧化和水解。某学习小组探究CuCl的制备并测定纯度。回答下列问题:
已知:①
②某些含铜化合物和离子在水中的颜色和状态如下表:
Ⅰ.组装仪器,检查装置气密性,添加药品;
Ⅱ.水浴加热三颈烧瓶,打开K1、K2;
Ⅲ.待三颈烧瓶中溶液由黄绿色变为无色,关闭K1、K2;
Ⅳ.通过注射器向三颈烧瓶中加入水,生成白色沉淀,一段时间后部分沉淀变为棕红色。
(1)仪器a的名称为___________ ;B的作用为___________ (答出一点即可)。
(2)步骤Ⅲ反应的离子方程式为___________ 。
(3)步骤Ⅳ中,沉淀由白色转化为棕红色的原因___________ 。
(4)为防止生成棕红色固体,还需在原步骤Ⅰ中通过注射器往三颈烧瓶中加入一定量___________ (药品名称),再按上述步骤进行实验即可。
(5)产品先快速水洗后再醇洗,醇洗的目的为___________ 。
(6)测定CuCl产品纯度:将10.00 g产品溶于硝酸,配成250 mL溶液,取25.00 mL,加20.00 mL 0.5000 mol/L AgNO3溶液,充分反应后,加少量硝基苯覆盖沉淀。NH4Fe(SO4)2溶液作指示剂,用0.1000mol/L NH4SCN标准溶液滴定过量的AgNO3溶液,平行实验三次,平均消耗NH4SCN溶液10.00 mL。产品的纯度为___________ ,若未加入硝基苯会导致测定结果___________ (填“偏高”或“偏低”或“无影响”)。
[已知: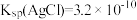 ,
,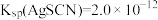 ]。
]。
已知:①

②某些含铜化合物和离子在水中的颜色和状态如下表:
| 化合物或离子 | CuCl | [CuCl4]2- | [CuCl3]2- | CuOH | Cu2O |
| 颜色和状态 | 白色沉淀 | 黄绿色溶液 | 无色溶液 | 黄色沉淀 | 棕红色沉淀 |
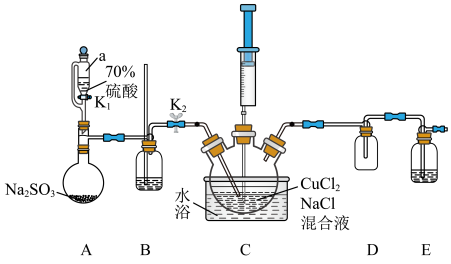
Ⅰ.组装仪器,检查装置气密性,添加药品;
Ⅱ.水浴加热三颈烧瓶,打开K1、K2;
Ⅲ.待三颈烧瓶中溶液由黄绿色变为无色,关闭K1、K2;
Ⅳ.通过注射器向三颈烧瓶中加入水,生成白色沉淀,一段时间后部分沉淀变为棕红色。
(1)仪器a的名称为
(2)步骤Ⅲ反应的离子方程式为
(3)步骤Ⅳ中,沉淀由白色转化为棕红色的原因
(4)为防止生成棕红色固体,还需在原步骤Ⅰ中通过注射器往三颈烧瓶中加入一定量
(5)产品先快速水洗后再醇洗,醇洗的目的为
(6)测定CuCl产品纯度:将10.00 g产品溶于硝酸,配成250 mL溶液,取25.00 mL,加20.00 mL 0.5000 mol/L AgNO3溶液,充分反应后,加少量硝基苯覆盖沉淀。NH4Fe(SO4)2溶液作指示剂,用0.1000mol/L NH4SCN标准溶液滴定过量的AgNO3溶液,平行实验三次,平均消耗NH4SCN溶液10.00 mL。产品的纯度为
[已知:
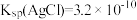 ,
,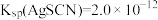 ]。
]。
您最近半年使用:0次
6 . 以某四氯化钛精制厂的尾渣(主要含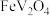 、
、 、NaCl及少量的
、NaCl及少量的 、
、 等)为原料制备
等)为原料制备 的工艺流程如下:
的工艺流程如下: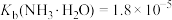 ;
; ;
;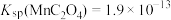
(1)“水洗”的目的为___________ 。“水洗”和“酸浸”后均采用减压过滤,与常压过滤相比,其优点为___________ 。
(2)“焙烧”的目的是将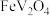 转化为
转化为 和可溶于水的
和可溶于水的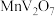 ,以利于“酸浸”时钒浸出。
,以利于“酸浸”时钒浸出。
①该反应的化学方程式为___________ 。
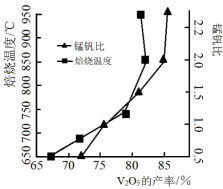
②钒浸出率与焙烧温度、锰钒比的关系如图所示。“焙烧”的最佳温度和锰钒比分别为___________ 、___________ 温度不宜过低的可能原因为___________ 。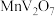 与
与 按物质的量比1:1进行反应的离子方程式为
按物质的量比1:1进行反应的离子方程式为___________
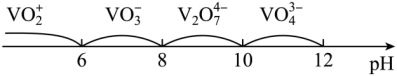
(4)“沉钒”时,在25℃下维持溶液pH=7,向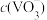 =0.2
=0.2 的酸浸液中加入等体积的
的酸浸液中加入等体积的 溶液进行反应(忽略溶液混合时体积的变化),反应后溶液中
溶液进行反应(忽略溶液混合时体积的变化),反应后溶液中 =0.005
=0.005 ,则沉钒率为
,则沉钒率为___________ %。
(5)“煅烧”所得 可制成铝钒合金(
可制成铝钒合金(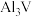 ),其晶胞结构如图所示。用原子的分数坐标可以表示晶胞中各原子的位置,如A点原子的分数坐标为
),其晶胞结构如图所示。用原子的分数坐标可以表示晶胞中各原子的位置,如A点原子的分数坐标为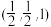 。
。___________ 。
②B点原子的分数坐标为(1, ,
,___________ )(用含b、c的代数式表示),V原子的配位数为___________ 。
 、
、 、NaCl及少量的
、NaCl及少量的 、
、 等)为原料制备
等)为原料制备 的工艺流程如下:
的工艺流程如下: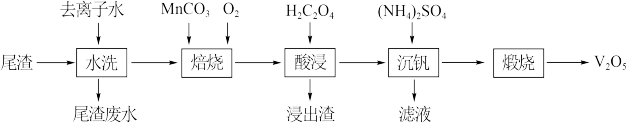
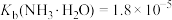 ;
; ;
;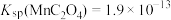
(1)“水洗”的目的为
(2)“焙烧”的目的是将
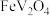 转化为
转化为 和可溶于水的
和可溶于水的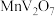 ,以利于“酸浸”时钒浸出。
,以利于“酸浸”时钒浸出。①该反应的化学方程式为
②钒浸出率与焙烧温度、锰钒比的关系如图所示。“焙烧”的最佳温度和锰钒比分别为
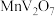 与
与 按物质的量比1:1进行反应的离子方程式为
按物质的量比1:1进行反应的离子方程式为(4)“沉钒”时,在25℃下维持溶液pH=7,向
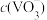 =0.2
=0.2 的酸浸液中加入等体积的
的酸浸液中加入等体积的 溶液进行反应(忽略溶液混合时体积的变化),反应后溶液中
溶液进行反应(忽略溶液混合时体积的变化),反应后溶液中 =0.005
=0.005 ,则沉钒率为
,则沉钒率为(5)“煅烧”所得
 可制成铝钒合金(
可制成铝钒合金(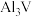 ),其晶胞结构如图所示。用原子的分数坐标可以表示晶胞中各原子的位置,如A点原子的分数坐标为
),其晶胞结构如图所示。用原子的分数坐标可以表示晶胞中各原子的位置,如A点原子的分数坐标为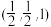 。
。
②B点原子的分数坐标为(1,
 ,
,
您最近半年使用:0次
7 . 某小组在实验室模拟侯氏制碱工艺制备 ,装置如图所示(夹持装置略去),下列离子方程式错误的是
,装置如图所示(夹持装置略去),下列离子方程式错误的是
 ,装置如图所示(夹持装置略去),下列离子方程式错误的是
,装置如图所示(夹持装置略去),下列离子方程式错误的是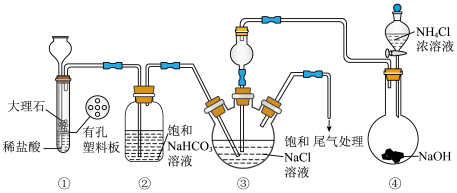
A.①中: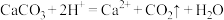 | B.②中: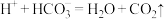 |
C.③中: | D.④中: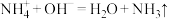 |
您最近半年使用:0次
8 . 硼氢化钠可作还原剂,与水反应的化学方程式为 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.3.8g 固体中含有的离子数为0.2 固体中含有的离子数为0.2 |
B.pH=7的纯水中含有的 数为 数为 |
C.0.1 mol 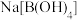 中含有的 中含有的 键数为0.4 键数为0.4 |
D.生成22.4L(已折算成标准状况)的 时,转移的电子数为2 时,转移的电子数为2 |
您最近半年使用:0次
2024·内蒙古呼和浩特·二模
名校
9 . 三氯三(四氢呋喃)合铬(Ⅲ) 可催化烯烃加聚,制备的方法加下。
可催化烯烃加聚,制备的方法加下。
已知:① 易潮解,易升华,高温下易被氧气氧化。
易潮解,易升华,高温下易被氧气氧化。
② 气体有毒,遇水发生水解产生两种酸性气体。
气体有毒,遇水发生水解产生两种酸性气体。
Ⅰ.制备无水 :
:
某化学小组用 (沸点76.8℃)和
(沸点76.8℃)和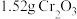 在高温下制备无水
在高温下制备无水 ,同时生成
,同时生成 气体,实验装置如图所示:
气体,实验装置如图所示: ,实验装置合理的连接顺序为A→G-→F→
,实验装置合理的连接顺序为A→G-→F→_______ →B(填装置字母标号,可重复使用)。
(2)装置乙名称为_______ ,装置D中粗导管的作用是_______ 。
(3)尾气处理时发生反应的离子方程式:_______ 。
Ⅱ.合成 :
: 原理为:
原理为:
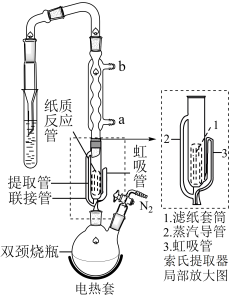
实验操作:按如图组装仪器,将步骤Ⅰ所得无水 和
和 锌粉放入滤纸套筒内,双颈烧瓶中加入
锌粉放入滤纸套筒内,双颈烧瓶中加入 无水四氢呋喃(THF),通
无水四氢呋喃(THF),通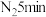 后关闭,接通冷却水,加热四氢呋喃至沸腾,在索氏提取器中发生反应,回流
后关闭,接通冷却水,加热四氢呋喃至沸腾,在索氏提取器中发生反应,回流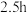 后再通入
后再通入 冷却至室温;取下双颈烧瓶,在通风橱中蒸发至有较多固体析出,冷却、抽滤、干燥后称量即得产品
冷却至室温;取下双颈烧瓶,在通风橱中蒸发至有较多固体析出,冷却、抽滤、干燥后称量即得产品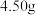 。
。_______ 。
(5)产品沿索氏提取器的管_______ (2或3)流回双颈烧瓶。
(6)已知Cr(Ⅱ)对该反应有催化作用,推断加入Zn粉发生反应的化学方程式为:_______ 。
(7)实验所用的四氢呋喃需进行无水处理,下列可以除去四氢呋喃中少量水分的试剂是_______ 。
A.金属钠 B.浓硫酸 C.具有吸水能力的分子筛
(8)产品产率为____ %(结果保留小数点后一位)[已知: 的摩尔质量为
的摩尔质量为 ;
; 的摩尔质量为
的摩尔质量为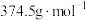 ]。
]。
 可催化烯烃加聚,制备的方法加下。
可催化烯烃加聚,制备的方法加下。已知:①
 易潮解,易升华,高温下易被氧气氧化。
易潮解,易升华,高温下易被氧气氧化。②
 气体有毒,遇水发生水解产生两种酸性气体。
气体有毒,遇水发生水解产生两种酸性气体。Ⅰ.制备无水
 :
:某化学小组用
 (沸点76.8℃)和
(沸点76.8℃)和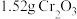 在高温下制备无水
在高温下制备无水 ,同时生成
,同时生成 气体,实验装置如图所示:
气体,实验装置如图所示: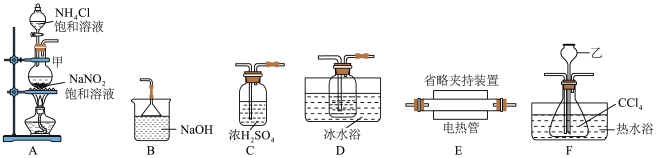
 ,实验装置合理的连接顺序为A→G-→F→
,实验装置合理的连接顺序为A→G-→F→(2)装置乙名称为
(3)尾气处理时发生反应的离子方程式:
Ⅱ.合成
 :
:①四氢呋喃(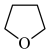 THF)为常见的有机溶剂,沸点66℃,易燃。
THF)为常见的有机溶剂,沸点66℃,易燃。
 原理为:
原理为:
实验操作:按如图组装仪器,将步骤Ⅰ所得无水
 和
和 锌粉放入滤纸套筒内,双颈烧瓶中加入
锌粉放入滤纸套筒内,双颈烧瓶中加入 无水四氢呋喃(THF),通
无水四氢呋喃(THF),通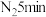 后关闭,接通冷却水,加热四氢呋喃至沸腾,在索氏提取器中发生反应,回流
后关闭,接通冷却水,加热四氢呋喃至沸腾,在索氏提取器中发生反应,回流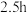 后再通入
后再通入 冷却至室温;取下双颈烧瓶,在通风橱中蒸发至有较多固体析出,冷却、抽滤、干燥后称量即得产品
冷却至室温;取下双颈烧瓶,在通风橱中蒸发至有较多固体析出,冷却、抽滤、干燥后称量即得产品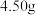 。
。
(5)产品沿索氏提取器的管
(6)已知Cr(Ⅱ)对该反应有催化作用,推断加入Zn粉发生反应的化学方程式为:
(7)实验所用的四氢呋喃需进行无水处理,下列可以除去四氢呋喃中少量水分的试剂是
A.金属钠 B.浓硫酸 C.具有吸水能力的分子筛
(8)产品产率为
 的摩尔质量为
的摩尔质量为 ;
; 的摩尔质量为
的摩尔质量为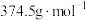 ]。
]。
您最近半年使用:0次
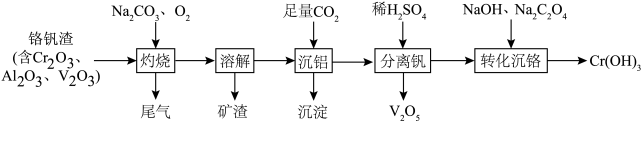
10 . 某科研团队从铬钒渣中分离钒并制备Cr(OH)3的流程如下:
②Cr的最高价含氧酸根离子在酸性介质中主要以 存在,在碱性介质中主要以
存在,在碱性介质中主要以 存在。
存在。
下列说法错误的是
②Cr的最高价含氧酸根离子在酸性介质中主要以
 存在,在碱性介质中主要以
存在,在碱性介质中主要以 存在。
存在。下列说法错误的是
| A.“灼烧”步骤的尾气中含CO2 |
B.“沉铝”步骤的离子方程式为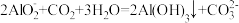 |
C.“分离钒”之后Cr元素的存在形式主要为 |
| D.“转化沉铬”步骤中氧化剂与还原剂的物质的量之比为1∶3 |
您最近半年使用:0次
7日内更新
|
256次组卷
|
2卷引用:福建省漳州市2024届高三下学期毕业班第三次质量检测三模化学试题



