名校
解题方法
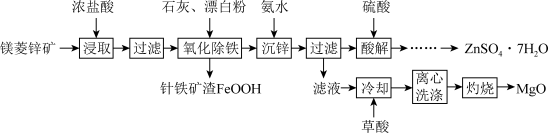
1 . 镁菱锌矿(主要成分为ZnCO3、MgCO3等,含有少量FeCO3、CaCO3等杂质)可用于生产媒染剂、防腐剂ZnSO4•7H2O以及耐火材料MgO。制备工艺流程如图:
回答下列有关问题:
(1)浓盐酸浸取矿石时,保持较大液固体积比(如3:1),目的是_______ 。
(2)“氧化除铁”在90℃,控制溶液pH在4.0~5.0,得到针铁矿渣的离子方程式为_______ 。
(3)“沉锌”时,加入氨水调节pH的范围是_______ 。
(4)“酸解”后获得ZnSO4•7H2O的操作依次经过蒸发浓缩、_______ 制得的ZnSO4•7H2O在烘干时需减压烘干的原因是_______ 。
(5)“滤液”中加入H2C2O4饱和溶液产生MgC2O4沉淀,若“灼烧”时产生两种气体,则该反应的化学方程式为:_______ 。
| 阳离子 | Fe3+ | Fe2+ | Zn2+ | Mg2+ | Ca2+ |
| 开始沉淀 | 2.7 | 7.6 | 6.2 | 9.4 | 13 |
| 完全沉淀 | 3.7 | 9.6 | 8.2 | 12.4 | _______ |
(1)浓盐酸浸取矿石时,保持较大液固体积比(如3:1),目的是
(2)“氧化除铁”在90℃,控制溶液pH在4.0~5.0,得到针铁矿渣的离子方程式为
(3)“沉锌”时,加入氨水调节pH的范围是
(4)“酸解”后获得ZnSO4•7H2O的操作依次经过蒸发浓缩、
(5)“滤液”中加入H2C2O4饱和溶液产生MgC2O4沉淀,若“灼烧”时产生两种气体,则该反应的化学方程式为:
您最近一年使用:0次
名校
解题方法
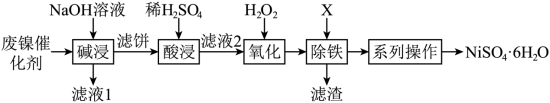
2 . 利用油脂厂废弃镍(Ni)催化剂(主要含有Ni,还含少量Al、Fe、NiO、Al2O3、Fe2O3)制备NiSO4·6H2O的工艺流程如下:
(1)为了加快“碱浸”的速率可以采取的措施是_______ (任写两条)。
(2)向滤液1中通入足量CO2可以将其中的金属元素沉淀,写出该反应的离子反应方程式____ 。
(3)“滤液2” 中含金属阳离子有_______ 。
(4)①“氧化”中反应的离子反应方程式是_______ 。
②“氧化”中可以代替H2O2的最佳物质是_______ (填标号)。
a.Cl2 b.O2 c.Fe
(5)根据除铁及系列操作,回答以下问题:
①已知溶液中存在Fe3++3H2O Fe(OH)3+3H+平衡,X物质可以为下列的
Fe(OH)3+3H+平衡,X物质可以为下列的_______ 。
a.H2SO4 b.NiO c.Ni(OH)2 d.CO2
②边搅拌边向滤液中加入X至pH=4,加热、过滤、洗涤,检验沉淀是否洗涤干净的方法_______ 。
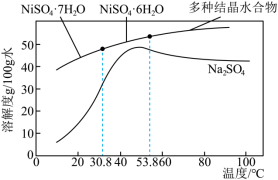
③结晶:将滤液蒸发、降温至稍高于_______ ℃结晶,过滤即获得产品,硫酸镍晶体溶解度曲线图如图所示。
(1)为了加快“碱浸”的速率可以采取的措施是
(2)向滤液1中通入足量CO2可以将其中的金属元素沉淀,写出该反应的离子反应方程式
(3)“滤液2” 中含金属阳离子有
(4)①“氧化”中反应的离子反应方程式是
②“氧化”中可以代替H2O2的最佳物质是
a.Cl2 b.O2 c.Fe
(5)根据除铁及系列操作,回答以下问题:
①已知溶液中存在Fe3++3H2O
 Fe(OH)3+3H+平衡,X物质可以为下列的
Fe(OH)3+3H+平衡,X物质可以为下列的a.H2SO4 b.NiO c.Ni(OH)2 d.CO2
②边搅拌边向滤液中加入X至pH=4,加热、过滤、洗涤,检验沉淀是否洗涤干净的方法
③结晶:将滤液蒸发、降温至稍高于
您最近一年使用:0次
3 . 利用物质的性质能帮助我们开展科学探究。
(1)判断化学变化。如图,在稀盐酸和氢氧化钠溶液中分别滴加几滴无色酚酞溶液,观察到能使无色酚酞变红的物质是___________ 。
实验结论:稀盐酸和氢氧化钠溶液反应的化学方程式为___________ 。
(1)判断化学变化。如图,在稀盐酸和氢氧化钠溶液中分别滴加几滴无色酚酞溶液,观察到能使无色酚酞变红的物质是

| 编号 | 实验操作 | 实验现象 | 实验分析 |
| 实验一 | 取一定量稀盐酸于小烧杯中,加入氢氧化钠溶液 | 无明显现象 | 稀盐酸与氢氧化钠溶液混合后有新物质生成 |
| 实验二 | 取实验一所得溶液少量于试管中,滴入几滴无色酚酞溶液 | 无明显现象 | |
| 实验三 | 取实验一所得溶液少量, |
您最近一年使用:0次
4 . 化学与生产生活密切相关,回答下列问题:
(1)在我市新农村建设中,许多家庭兴建了沼气池。沼气的主要成分是___________ 。
(2)6000L氧气在加压的情况下可装入容积为40L的钢瓶中,原因是___________ 。
(3)许多矿石中含有铁元素,菱铁矿的主要成分是FeCO3,其中铁元素的化合价是___________ 。
(4)大米的主要成分是淀粉,淀粉属于六大基本营养素中的___________ 。
(1)在我市新农村建设中,许多家庭兴建了沼气池。沼气的主要成分是
(2)6000L氧气在加压的情况下可装入容积为40L的钢瓶中,原因是
(3)许多矿石中含有铁元素,菱铁矿的主要成分是FeCO3,其中铁元素的化合价是
(4)大米的主要成分是淀粉,淀粉属于六大基本营养素中的
您最近一年使用:0次
5 . 甲、乙两种物质的溶解度曲线如图所示。下列说法错误的是

| A.80℃时,甲的饱和溶液中溶质与溶剂的质量比为4:5 |
| B.用蒸发结晶的方法可从乙的饱和溶液中获得大量的乙 |
| C.分别将60℃的甲、乙饱和溶液升温至80℃,此时甲溶液的溶质质量分数最大 |
| D.60℃时,向140g甲饱和溶液中先加50g水,再加20g甲,充分溶解后,溶液仍为饱和状态 |
您最近一年使用:0次
6 . 科学家研制出一种新型催化剂,可用于去除装修残留的甲醛(化学式为 CH2O),反应过程的微观示意图如下。下列说法正确的是

| A.物质甲为甲醛,其分子由碳原子和水分子构成 |
| B.物质乙中氧元素的化合价为-2 价 |
| C.该反应前后原子种类和数目均发生改变 |
| D.该反应消耗物质甲和生成物质丁的质量比为 5﹕3 |
您最近一年使用:0次
7 . 据西安电子科技大学芜湖研究所介绍,国内5G通信芯片用氮化镓材料制成。如图是氮元素在元素周期表中的信息以及镓原子的结构示意图。下列说法不正确的是
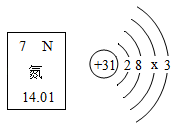
| A.氮原子核内质子数为7 | B.图中x=18 |
| C.镓原子核内中子数为31 | D.氮原子的相对原子质量为14.01 |
您最近一年使用:0次
名校
8 .  溶液具有漂白能力,已知
溶液具有漂白能力,已知 时,
时,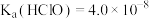 ,向含有
,向含有 的
的 溶液中逐滴滴入
溶液中逐滴滴入 溶液,滴加过程中溶液的
溶液,滴加过程中溶液的 随
随 溶液的体积的变化曲线及实验现象见下表。下列叙述不正确的是
溶液的体积的变化曲线及实验现象见下表。下列叙述不正确的是
 溶液具有漂白能力,已知
溶液具有漂白能力,已知 时,
时,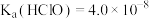 ,向含有
,向含有 的
的 溶液中逐滴滴入
溶液中逐滴滴入 溶液,滴加过程中溶液的
溶液,滴加过程中溶液的 随
随 溶液的体积的变化曲线及实验现象见下表。下列叙述不正确的是
溶液的体积的变化曲线及实验现象见下表。下列叙述不正确的是| 变化曲线 | 实验现象 |
| ⅰ. 产生红褐色沉淀 产生红褐色沉淀ⅱ.  红褐色沉淀的量增多 红褐色沉淀的量增多ⅲ.  红褐色沉淀的量增多 红褐色沉淀的量增多ⅳ.  点附近产生有刺激性气味的气体 点附近产生有刺激性气味的气体ⅴ.  红褐色沉淀的量略有增多 红褐色沉淀的量略有增多 |
A.NaClO的电子式是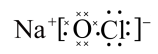 |
B.NaClO溶液中离子浓度大小顺序是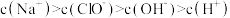 |
C.25℃,pH=7.0的NaClO和HClO的混合溶液中, |
D.C点附近生成红褐色沉淀的主要反应的离子方程式为 |
您最近一年使用:0次
名校
解题方法
9 . 下列离子方程式书写正确的是
A.用稀盐酸处理铜器表面的铜锈: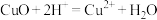 |
B. 与稀硝酸反应,当 与稀硝酸反应,当 时, 时,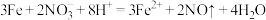 |
C.向 溶液中加入足量稀硝酸: 溶液中加入足量稀硝酸: |
D.向 悬浊液中加入 悬浊液中加入 溶液: 溶液: |
您最近一年使用:0次
名校
解题方法
10 . 下列表述不正确的是
A. 分子中 分子中 键的电子云轮廓图: 键的电子云轮廓图: |
B. 的分子模型:Ⅴ形 的分子模型:Ⅴ形 |
C.基态 原子的价层电子轨道表示式: 原子的价层电子轨道表示式: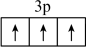 |
D. 的形成过程: 的形成过程: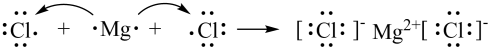 |
您最近一年使用:0次