名校
解题方法
1 . 立德粉(主要成分为BaSO4 ZnS)常用作颜料。以粗氧化锌(主要成分为ZnO,还含少量CuO、Fe3O4等杂质)和BaS为原料制备立德粉的流程如图所示:
ZnS)常用作颜料。以粗氧化锌(主要成分为ZnO,还含少量CuO、Fe3O4等杂质)和BaS为原料制备立德粉的流程如图所示:___________ 。
(2)加入H2O2发生反应的离子方程式为___________ 。
(3)分离出Fe(OH)3的实验操作名称为___________ 。
(4)“除杂Ⅱ”中加入过量的锌粉主要除去___________ (填离子符号),该反应的反应类型为___________ 。
(5)“滤渣”的成分是___________ 。
(6)8.34 g绿矾(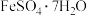 )晶体样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示:
)晶体样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示: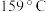 时固体N的化学式为
时固体N的化学式为___________ ,取适量  时所得的样品P,隔绝空气加热至
时所得的样品P,隔绝空气加热至 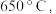 得到一种红棕色固体物质Q ,同时有两种无色气体生成,请写出该反应的化学方程式
得到一种红棕色固体物质Q ,同时有两种无色气体生成,请写出该反应的化学方程式___________ 。
 ZnS)常用作颜料。以粗氧化锌(主要成分为ZnO,还含少量CuO、Fe3O4等杂质)和BaS为原料制备立德粉的流程如图所示:
ZnS)常用作颜料。以粗氧化锌(主要成分为ZnO,还含少量CuO、Fe3O4等杂质)和BaS为原料制备立德粉的流程如图所示: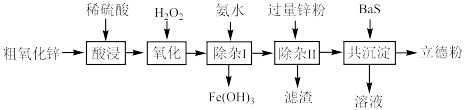
(2)加入H2O2发生反应的离子方程式为
(3)分离出Fe(OH)3的实验操作名称为
(4)“除杂Ⅱ”中加入过量的锌粉主要除去
(5)“滤渣”的成分是
(6)8.34 g绿矾(
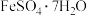 )晶体样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示:
)晶体样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示: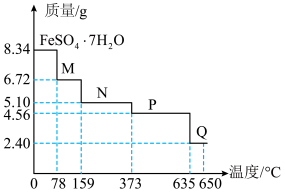
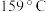 时固体N的化学式为
时固体N的化学式为 时所得的样品P,隔绝空气加热至
时所得的样品P,隔绝空气加热至 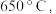 得到一种红棕色固体物质Q ,同时有两种无色气体生成,请写出该反应的化学方程式
得到一种红棕色固体物质Q ,同时有两种无色气体生成,请写出该反应的化学方程式
您最近一年使用:0次
2024-05-22更新
|
235次组卷
|
2卷引用:2024届重庆市乌江新高考协作体高三下学期模拟预测化学试题
解题方法
2 . 下列化学用语或图示表达正确的是
A.Mg(OH)2的电子式: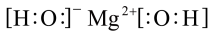 |
| B.第三周期所有元素中第一电离能比S大的元素只有Cl和Ar |
C.HCl的s-pσ键电子云图: |
D.Cu2+结构示意图: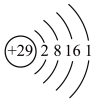 |
您最近一年使用:0次
解题方法
3 . 碳酸钛用作脱硫的催化剂,瓷釉、涂料和清漆的颜料,是合成二氧化锰和制造其他锰盐的原料。工业上制备高纯度碳酸锰的工艺流程如下:
②该工艺下,0.1mol/L的金属离子形成氢氧化物沉淀的pH如下:
③常温下,Ksp(CaF2)=1.60×10-10,Ksp(MgF2)=6.40×10-11.回答下列问题:
(1)基态Mn2+价电子的轨道表示式为___________ 。
(2)滤渣1的主要成份是:___________ ,其附着在矿粉颗粒表面会阻碍菱锰矿与酸的反应,若此时加入H2O2,利用其迅速分解产生的大量气泡可消除其不利影响,导致H2O2分解的因素是___________ 。
(3)在“浸出液”中加入“MnO2”所发生反应的离子方程式为___________ 。
(4)加入氨水调节溶液pH的范围___________ 。
(5)常温下,当溶液中Ca2+、Mg2+完全除去时,则c(F-)≥___________ mol/L。
(6)沉锰步骤发生主要反应的离子方程式为:___________ 。
(7)已知:5 +2Mn2++8H2O=16H++10
+2Mn2++8H2O=16H++10 +2
+2 ,实验室可利用Na2S2O8溶液来检验Mn2+是否反应完全。如何确定Mn2+已完全反应?
,实验室可利用Na2S2O8溶液来检验Mn2+是否反应完全。如何确定Mn2+已完全反应?___________ 。
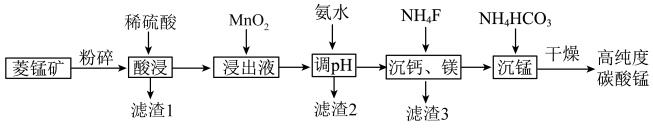
②该工艺下,0.1mol/L的金属离子形成氢氧化物沉淀的pH如下:
| 金属离子Mn+ | Fe3+ | Al3+ | Fe2+ | Mn2+ | Mg2+ |
| 开始沉淀的pH | 1.9 | 3.4 | 7.0 | 8.1 | 9.1 |
| 沉淀完全的pH[c(Mn2+)≤1.0×10-5mol/L] | 3.2 | 4.7 | 9.0 | 10.1 | 11.1 |
(1)基态Mn2+价电子的轨道表示式为
(2)滤渣1的主要成份是:
(3)在“浸出液”中加入“MnO2”所发生反应的离子方程式为
(4)加入氨水调节溶液pH的范围
(5)常温下,当溶液中Ca2+、Mg2+完全除去时,则c(F-)≥
(6)沉锰步骤发生主要反应的离子方程式为:
(7)已知:5
 +2Mn2++8H2O=16H++10
+2Mn2++8H2O=16H++10 +2
+2 ,实验室可利用Na2S2O8溶液来检验Mn2+是否反应完全。如何确定Mn2+已完全反应?
,实验室可利用Na2S2O8溶液来检验Mn2+是否反应完全。如何确定Mn2+已完全反应?
您最近一年使用:0次
解题方法
4 . 常温下,下列各组离子在相应条件下可能大量共存的是
A.水电离出来的c(H+)<10-7mol/L的溶液中:Cl-、K+、 、S2- 、S2- |
B.遇甲基橙变红色的溶液中: 、Na+、Cl-、 、Na+、Cl-、 |
C.含Al3+的溶液中:K+、Na+、Cl-、 |
D.透明中性溶液中:Fe3+、 、 、 、Cl- 、Cl- |
您最近一年使用:0次
解题方法
5 . 宏观辨识与微观探析是化学学科核心素养之一,下列方程式不能正确解释相应事实的是
A.SO2气体通入足量NaClO溶液中:SO2+H2O+3ClO-=Cl-+ +2HClO +2HClO |
B.亚硫酸氢钠水解方程式: +H2O +H2O H2SO3+OH- H2SO3+OH- |
C.向加碘食盐(含碘酸钾)中加入碘化钾溶液和稀硫酸: +5I-+6H+=3I2+3H2O +5I-+6H+=3I2+3H2O |
| D.常用稀H2SO4和Fe2+为原料处理废旧铅酸蓄电池中的PbO2:2Fe2++PbO2+4H+=2Fe3++Pb2++2H2O |
您最近一年使用:0次
6 . 已知反应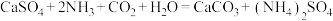 可以制取硫酸铵晶体,下列说法正确的是
可以制取硫酸铵晶体,下列说法正确的是
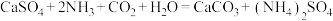 可以制取硫酸铵晶体,下列说法正确的是
可以制取硫酸铵晶体,下列说法正确的是A. 的电子式为 的电子式为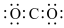 | B. 的VSEPR模型为三角锥形 的VSEPR模型为三角锥形 |
C.钙离子结构示意图为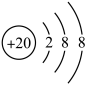 | D. 由非金属元素组成,仅含共价键 由非金属元素组成,仅含共价键 |
您最近一年使用:0次
7 . 已知反应: ,
, 为阿伏加德罗常数的值,若反应消耗了
为阿伏加德罗常数的值,若反应消耗了 粉(
粉( 足量)。下列说法正确的是
足量)。下列说法正确的是
 ,
, 为阿伏加德罗常数的值,若反应消耗了
为阿伏加德罗常数的值,若反应消耗了 粉(
粉( 足量)。下列说法正确的是
足量)。下列说法正确的是A.所得溶液中 数目为 数目为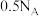 | B.收集到的 分子数为 分子数为 |
C.转移的电子数为 | D.生成的 含共价键数为 含共价键数为 |
您最近一年使用:0次
8 . “价类二维图”是学习元素及其化合物的重要模型和工具。如图为铁元素和氯元素的部分“价类二维图”,其中箭头表示部分物质间的转化关系。下列说法不正确的是

A. 与少量a反应可实现转化① 与少量a反应可实现转化① |
| B.从氯元素的化合价角度分析,b既有氧化性又有还原性 |
C.由图可预测:高铁酸盐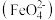 具有强氧化性,可用于杀菌消毒 具有强氧化性,可用于杀菌消毒 |
D.可存在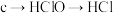 的转化 的转化 |
您最近一年使用:0次
9 . (I)铁是人类较早使用的金属之一。运用所学知识,回答下列问题。
(1)鉴别 胶体和
胶体和 溶液的方法是
溶液的方法是__________ 。
(2)不仅溶液中 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式
氧化,请写出反应的化学方程式__________ ,现象为__________ 。
(3)绿矾( )是治疗缺铁性贫血药品的主要成分,也是中学化学一种常见的化学试剂。亚铁盐在空气中容易被氧化而变质。
)是治疗缺铁性贫血药品的主要成分,也是中学化学一种常见的化学试剂。亚铁盐在空气中容易被氧化而变质。
①为防止 溶液变质,应在溶液中加入少量
溶液变质,应在溶液中加入少量___________ 。
②甲同学取 稀硫酸酸化
稀硫酸酸化 溶液,加入几滴双氧水后,再加入1滴
溶液,加入几滴双氧水后,再加入1滴 溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与双氧水反应的离子方程式为
溶液与双氧水反应的离子方程式为__________ 。乙同学认为甲同学的实验不够严谨,该组同学在 用稀
用稀 酸化的
酸化的 溶液中先加入
溶液中先加入 煤油,再于液面下依次加入几滴双氧水和1滴
煤油,再于液面下依次加入几滴双氧水和1滴 溶液,溶液变红,煤油的作用是
溶液,溶液变红,煤油的作用是__________ 。
(II)氯化铁溶液可用于腐蚀印刷电路板上的铜,某腐蚀后的废液中含有 和
和 ,且
,且 。
。
(4)从废液中可回收铜,并获得 溶液,设计如下方案:
溶液,设计如下方案:___________ (填物质名称)。
②物质X为___________ 。
A. B.酸性
B.酸性 溶液 C.
溶液 C.
(5)取该废液 并加入
并加入 铁粉,充分反应。
铁粉,充分反应。
①对反应后的溶液分析错误的是___________ 。
A.溶液中一定含有
B.若有固体剩余,则固体中一定含有铁
C.若溶液中有 ,则可能有固体析出
,则可能有固体析出
D.溶液若有 剩余,则一定没有固体析出
剩余,则一定没有固体析出
②若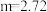 ,则充分反应后得到
,则充分反应后得到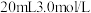 氯化亚铁溶液和
氯化亚铁溶液和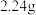 固体混合物。则原废液中
固体混合物。则原废液中 的物质的量浓度为
的物质的量浓度为___________ 。
(1)鉴别
 胶体和
胶体和 溶液的方法是
溶液的方法是(2)不仅溶液中
 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式
氧化,请写出反应的化学方程式(3)绿矾(
 )是治疗缺铁性贫血药品的主要成分,也是中学化学一种常见的化学试剂。亚铁盐在空气中容易被氧化而变质。
)是治疗缺铁性贫血药品的主要成分,也是中学化学一种常见的化学试剂。亚铁盐在空气中容易被氧化而变质。①为防止
 溶液变质,应在溶液中加入少量
溶液变质,应在溶液中加入少量②甲同学取
 稀硫酸酸化
稀硫酸酸化 溶液,加入几滴双氧水后,再加入1滴
溶液,加入几滴双氧水后,再加入1滴 溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与双氧水反应的离子方程式为
溶液与双氧水反应的离子方程式为 用稀
用稀 酸化的
酸化的 溶液中先加入
溶液中先加入 煤油,再于液面下依次加入几滴双氧水和1滴
煤油,再于液面下依次加入几滴双氧水和1滴 溶液,溶液变红,煤油的作用是
溶液,溶液变红,煤油的作用是(II)氯化铁溶液可用于腐蚀印刷电路板上的铜,某腐蚀后的废液中含有
 和
和 ,且
,且 。
。(4)从废液中可回收铜,并获得
 溶液,设计如下方案:
溶液,设计如下方案: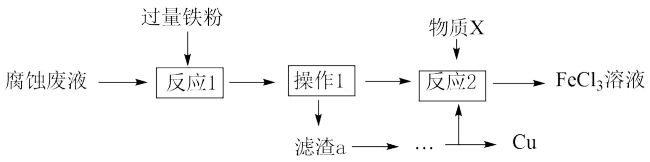
②物质X为
A.
 B.酸性
B.酸性 溶液 C.
溶液 C.
(5)取该废液
 并加入
并加入 铁粉,充分反应。
铁粉,充分反应。①对反应后的溶液分析错误的是
A.溶液中一定含有

B.若有固体剩余,则固体中一定含有铁
C.若溶液中有
 ,则可能有固体析出
,则可能有固体析出D.溶液若有
 剩余,则一定没有固体析出
剩余,则一定没有固体析出②若
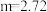 ,则充分反应后得到
,则充分反应后得到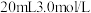 氯化亚铁溶液和
氯化亚铁溶液和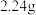 固体混合物。则原废液中
固体混合物。则原废液中 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
10 . 已知:① ;②
;② 。则下列判断正确的是
。则下列判断正确的是
 ;②
;② 。则下列判断正确的是
。则下列判断正确的是A.在反应②中 只表现出还原性 只表现出还原性 |
B.氧化性强弱: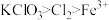 |
C. 只有氧化性, 只有氧化性, 只有还原性 只有还原性 |
D.用双线桥法表示反应②电子得失情况: |
您最近一年使用:0次



