名校
解题方法
1 . 下列反应的离子方程式正确的是
A.浓硝酸有时呈黄色: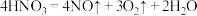 ,是分解生成的NO溶于硝酸的缘故 ,是分解生成的NO溶于硝酸的缘故 |
B.过量 通入苯酚钠溶液中: 通入苯酚钠溶液中: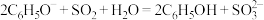 |
C.盐碱地(含较多NaCl, )不利于植物生长,通过施加适量石膏可以降低土壤的碱性,其原理为: )不利于植物生长,通过施加适量石膏可以降低土壤的碱性,其原理为: |
D.用 溶液检验 溶液检验 :Fe2++[Fe(CN)6]3- =Fe[Fe(CN)6]- :Fe2++[Fe(CN)6]3- =Fe[Fe(CN)6]- |
您最近一年使用:0次
名校
2 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.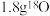 中含有的中子数为 中含有的中子数为 |
B.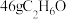 分子中含极性键数目一定是 分子中含极性键数目一定是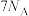 |
C. 过氧化钡 过氧化钡 固体中阴、阳离子总数为 固体中阴、阳离子总数为 |
D. 溶液中含有阳离子的数目大于 溶液中含有阳离子的数目大于 |
您最近一年使用:0次
3 . “龙行龘龘,欣欣家国”,美好生活与化学紧密相连。下列说法正确的是
| A.免洗洗手液有效成分中的活性银离子能使蛋白质变性 |
| B.维生素C可用做水果罐头的抗氧化剂是由于其难以被氧化 |
| C.重油在高温、高压和催化剂作用下通过水解反应转化为小分子烃 |
| D.“天目一号”气象星座卫星的光伏发电系统工作时可将化学能转化为电能 |
您最近一年使用:0次
名校
解题方法
4 . 下列生活情境中对应的离子方程式正确的是
A.泡沫灭火器灭火原理: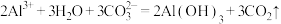 |
B.除水垢时,先用Na2CO3溶液浸泡: |
C.铅蓄电池放电时总反应: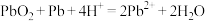 |
D.84消毒液与洁厕灵不能混合使用原理: |
您最近一年使用:0次
7日内更新
|
554次组卷
|
3卷引用:福建省厦门市国祺中学2023-2024学年高三下学期第二次模拟化学试题
名校
解题方法
5 . 锌电解阳极泥(主要成分为 和
和 ,还有少量锰铅氧化物
,还有少量锰铅氧化物 和
和 )是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题:
)是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题: 易溶于水,不溶于乙醇
易溶于水,不溶于乙醇
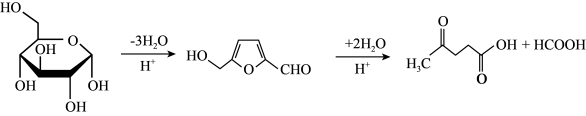
②在较高温度及酸性催化条件下,葡萄糖能发生如图反应: 时
时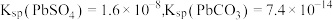
(1)已知 中
中 为
为 价,
价, 为
为 价和
价和 价,该氧化物中
价,该氧化物中 价和
价和 价
价 的物质的量之比为
的物质的量之比为_______ 。
(2)“还原酸浸”过程中主要反应的离子方程式为_______ ,该过程中实际葡萄糖加入量远大于理论需要量,其原因是_______ 。
(3)整个流程中可循环利用的物质是_______ (填名称)。获得 晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是
晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是_______ 。
(4)书写相关反应的离子方程式,并通过计算说明 时,可用
时,可用 溶液将“滤渣1”中的
溶液将“滤渣1”中的 完全转化为
完全转化为 的原因
的原因_______ 。
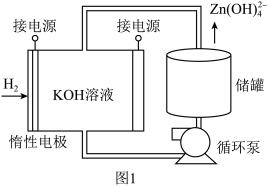
(5)通过氢电极增压法可制得单质锌,装置如图1所示。电解池工作时总反应的离子方程式为_______ 。 和
和 作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。
作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。
① 和
和 中
中 与
与 之间、
之间、 与
与 之间的离子键成分的百分数大小比较及解释
之间的离子键成分的百分数大小比较及解释_______ 。
② 晶胞结构如图2所示,其中
晶胞结构如图2所示,其中 代表
代表 。当
。当 位于晶胞的体心时,
位于晶胞的体心时, 于晶胞的
于晶胞的_______ 位置(填“顶点”“面心”“棱心”或“晶胞内”)。
 和
和 ,还有少量锰铅氧化物
,还有少量锰铅氧化物 和
和 )是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题:
)是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题: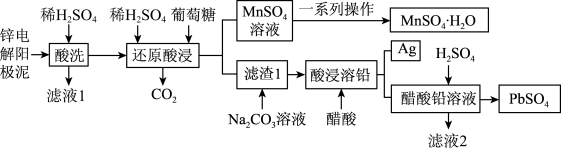
 易溶于水,不溶于乙醇
易溶于水,不溶于乙醇②在较高温度及酸性催化条件下,葡萄糖能发生如图反应:
 时
时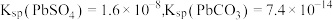
(1)已知
 中
中 为
为 价,
价, 为
为 价和
价和 价,该氧化物中
价,该氧化物中 价和
价和 价
价 的物质的量之比为
的物质的量之比为(2)“还原酸浸”过程中主要反应的离子方程式为
(3)整个流程中可循环利用的物质是
 晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是
晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是(4)书写相关反应的离子方程式,并通过计算说明
 时,可用
时,可用 溶液将“滤渣1”中的
溶液将“滤渣1”中的 完全转化为
完全转化为 的原因
的原因(5)通过氢电极增压法可制得单质锌,装置如图1所示。电解池工作时总反应的离子方程式为
 和
和 作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。
作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。①
 和
和 中
中 与
与 之间、
之间、 与
与 之间的离子键成分的百分数大小比较及解释
之间的离子键成分的百分数大小比较及解释②
 晶胞结构如图2所示,其中
晶胞结构如图2所示,其中 代表
代表 。当
。当 位于晶胞的体心时,
位于晶胞的体心时, 于晶胞的
于晶胞的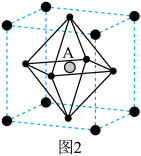
您最近一年使用:0次
7日内更新
|
94次组卷
|
2卷引用:福建省福州延安中学2024届高三下学期高考第一次模拟化学试题
名校
解题方法
6 . 从废旧镍钴锰三元锂电池正极材料[主要含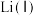 、
、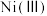 、
、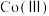 、
、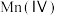 等金属的氧化物]中回收钴的一种流程如下:
等金属的氧化物]中回收钴的一种流程如下: 的形式存在。下列说法正确的是
的形式存在。下列说法正确的是
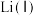 、
、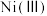 、
、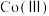 、
、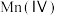 等金属的氧化物]中回收钴的一种流程如下:
等金属的氧化物]中回收钴的一种流程如下: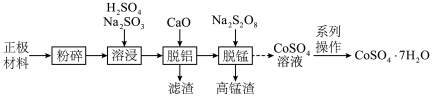
 的形式存在。下列说法正确的是
的形式存在。下列说法正确的是A.“溶浸”中 被还原 被还原 |
B.“脱铝”得到的滤渣成分是 |
C.“脱锰”的离子方程式为: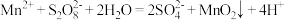 |
| D.“系列操作”含蒸发结晶、洗涤、干燥 |
您最近一年使用:0次
解题方法
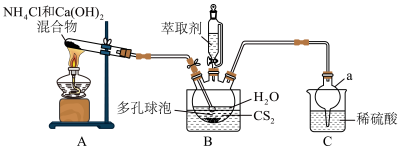
7 . 硫脲 为白色晶体,可溶于水,易溶于乙酸乙酯,可代替氰化物用于提炼金。合成硫脲的原理为
为白色晶体,可溶于水,易溶于乙酸乙酯,可代替氰化物用于提炼金。合成硫脲的原理为 。
。
(1)仪器a的名称为__________ 。
(2)从结构角度分析,硫脲可溶于水的原因是__________ 。
(3)多孔球泡的作用是__________ 。
(4)B中反应完全的标志是__________ 。
(5)分离提纯的方法为萃取,应选用的绿色萃取剂为__________ (填标号)。
a.苯 b.四氯化碳 c.乙酸乙酯 d.乙醇
(6)滴定原理:
取mg硫脲的粗产品溶于水,用c mol∙L-1的酸性重铬酸钾标准溶液滴定到终点,平行三次实验平均消耗VmL标准溶液,则样品中硫脲的纯度为__________ 。
(7)在酸性溶液中,硫脲在Fe3+存在下能溶解金形成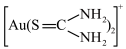 ,反应的离子方程式为
,反应的离子方程式为_______ 。溶解金的过程伴随着溶液变红的现象,原因可能为硫脲发生异构化生成__________ (填化学式)。
 为白色晶体,可溶于水,易溶于乙酸乙酯,可代替氰化物用于提炼金。合成硫脲的原理为
为白色晶体,可溶于水,易溶于乙酸乙酯,可代替氰化物用于提炼金。合成硫脲的原理为 。
。
(1)仪器a的名称为
(2)从结构角度分析,硫脲可溶于水的原因是
(3)多孔球泡的作用是
(4)B中反应完全的标志是
(5)分离提纯的方法为萃取,应选用的绿色萃取剂为
a.苯 b.四氯化碳 c.乙酸乙酯 d.乙醇
(6)滴定原理:

取mg硫脲的粗产品溶于水,用c mol∙L-1的酸性重铬酸钾标准溶液滴定到终点,平行三次实验平均消耗VmL标准溶液,则样品中硫脲的纯度为
(7)在酸性溶液中,硫脲在Fe3+存在下能溶解金形成
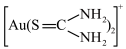 ,反应的离子方程式为
,反应的离子方程式为
您最近一年使用:0次
7日内更新
|
150次组卷
|
3卷引用:福建省厦门市国祺中学2023-2024学年高三下学期第二次模拟化学试题
解题方法
8 .  晶体为体心立方晶胞结构。
晶体为体心立方晶胞结构。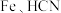 与
与 在一定条件下发生如下反应:
在一定条件下发生如下反应: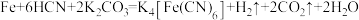 。
。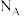 是阿伏加德罗常数的值。下列说法错误的是
是阿伏加德罗常数的值。下列说法错误的是
 晶体为体心立方晶胞结构。
晶体为体心立方晶胞结构。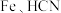 与
与 在一定条件下发生如下反应:
在一定条件下发生如下反应: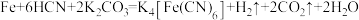 。
。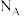 是阿伏加德罗常数的值。下列说法错误的是
是阿伏加德罗常数的值。下列说法错误的是A. 的 的 溶液中 溶液中 数目为 数目为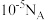 |
B.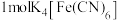 中配位键数为 中配位键数为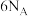 |
C.生成 (标准状况) (标准状况) ,转移电子数为 ,转移电子数为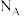 |
D.1个 晶胞质量为 晶胞质量为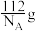 |
您最近一年使用:0次
名校
解题方法
9 . 某实验小组探究 的制取、性质及其应用。按要求回答下列问题。已知:①
的制取、性质及其应用。按要求回答下列问题。已知:① 是难溶于水的白色固体 ②
是难溶于水的白色固体 ② (无色)。
(无色)。
【实验i】探究 的制取(如下图所示装置,夹持装置略)
的制取(如下图所示装置,夹持装置略) 的
的 溶液
溶液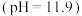 中通入
中通入 一段时间,至
一段时间,至 中溶液的
中溶液的 为7时向其中滴加一定量
为7时向其中滴加一定量 溶液,产生白色沉淀,过滤、洗涤、干燥,得到
溶液,产生白色沉淀,过滤、洗涤、干燥,得到 固体。
固体。
(1)试剂a是_______ 。
(2)向 溶液中通入
溶液中通入 的目的可能是
的目的可能是_______ 。
(3) 为7时滴加一定量
为7时滴加一定量 溶液产生白色沉淀的离子方程式为
溶液产生白色沉淀的离子方程式为_______ 。
(4)同学甲在 中出现白色沉淀之后继续通
中出现白色沉淀之后继续通 ,你认为同学甲的操作合理与否,并说明理由
,你认为同学甲的操作合理与否,并说明理由_______ 。
【实验ⅱ和实验ⅲ】探究 的性质
的性质_______ 。
(6)对比实验ⅱ和实验ⅲ,可以得出的实验结论为_______ 。
【实验ⅳ】探究的应用
(7)将 溶于乳酸
溶于乳酸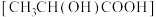 中制得可溶性的乳酸亚铁补血剂。同学乙用酸性
中制得可溶性的乳酸亚铁补血剂。同学乙用酸性 溶液测定该补血剂中亚铁含量,再计算乳酸亚铁的质量分数,发现乳酸亚铁的质量分数总是大于
溶液测定该补血剂中亚铁含量,再计算乳酸亚铁的质量分数,发现乳酸亚铁的质量分数总是大于 (操作误差略),其原因是
(操作误差略),其原因是_______ 。
 的制取、性质及其应用。按要求回答下列问题。已知:①
的制取、性质及其应用。按要求回答下列问题。已知:① 是难溶于水的白色固体 ②
是难溶于水的白色固体 ② (无色)。
(无色)。【实验i】探究
 的制取(如下图所示装置,夹持装置略)
的制取(如下图所示装置,夹持装置略)
 的
的 溶液
溶液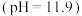 中通入
中通入 一段时间,至
一段时间,至 中溶液的
中溶液的 为7时向其中滴加一定量
为7时向其中滴加一定量 溶液,产生白色沉淀,过滤、洗涤、干燥,得到
溶液,产生白色沉淀,过滤、洗涤、干燥,得到 固体。
固体。(1)试剂a是
(2)向
 溶液中通入
溶液中通入 的目的可能是
的目的可能是(3)
 为7时滴加一定量
为7时滴加一定量 溶液产生白色沉淀的离子方程式为
溶液产生白色沉淀的离子方程式为(4)同学甲在
 中出现白色沉淀之后继续通
中出现白色沉淀之后继续通 ,你认为同学甲的操作合理与否,并说明理由
,你认为同学甲的操作合理与否,并说明理由【实验ⅱ和实验ⅲ】探究
 的性质
的性质
(6)对比实验ⅱ和实验ⅲ,可以得出的实验结论为
【实验ⅳ】探究的应用
(7)将
 溶于乳酸
溶于乳酸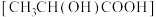 中制得可溶性的乳酸亚铁补血剂。同学乙用酸性
中制得可溶性的乳酸亚铁补血剂。同学乙用酸性 溶液测定该补血剂中亚铁含量,再计算乳酸亚铁的质量分数,发现乳酸亚铁的质量分数总是大于
溶液测定该补血剂中亚铁含量,再计算乳酸亚铁的质量分数,发现乳酸亚铁的质量分数总是大于 (操作误差略),其原因是
(操作误差略),其原因是
您最近一年使用:0次
名校
10 . 碳循环(如图所示)的研究有利于实现我国的碳达峰及碳中和目标。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
| A.可通过加聚反应使葡萄糖转化为淀粉 |
B.电催化 转化为乙酸时,转移 转化为乙酸时,转移 个电子 个电子 |
C. 、 、 分子中碳原子均不存在孤对电子 分子中碳原子均不存在孤对电子 |
D.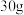 葡萄糖与乙酸的混合物中含有的氢原子数目为 葡萄糖与乙酸的混合物中含有的氢原子数目为 个 个 |
您最近一年使用:0次



