名校
解题方法
1 . 金昌市镍储量很丰富。草酸镍(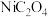 )是一种不溶于水的浅绿色粉末,常用于制镍催化剂和镍粉等。以铜镍合金废料(主要成分为镍和铜,含有一定量的铁和硅)为原料生产草酸镍的工艺流程如图:
)是一种不溶于水的浅绿色粉末,常用于制镍催化剂和镍粉等。以铜镍合金废料(主要成分为镍和铜,含有一定量的铁和硅)为原料生产草酸镍的工艺流程如图: 、
、 、
、 、
、 、
、 、
、 ;
;
②pH增大, 被氧化的速率加快,同时生成的
被氧化的速率加快,同时生成的 水解形成的胶体能吸附
水解形成的胶体能吸附 ;
;
③草酸的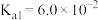 ,
,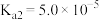 。
。
回答下列问题:
(1)Ni在元素周期表中的位置是___________ 。
(2)生产时为提高合金废料浸出率,下列措施可行的是___________ (填字母)。
A.适当延长浸出时间 B.高温浸出 C.分批加入混酸浸取并搅拌
(3)“萃取”步骤中萃取除去的主要金属阳离子是___________ 。
(4)“氧化”过程中,控制70℃、pH小于3的条件下进行。
①“氧化”过程的离子方程式为___________ ;
②若pH大于3镍的回收率降低的原因是___________ 。
(5)“过滤”后的滤液中加入 溶液反应得到草酸镍,过滤得到的草酸镍需要用蒸馏水洗涤,检验晶体是否洗涤干净的方法是
溶液反应得到草酸镍,过滤得到的草酸镍需要用蒸馏水洗涤,检验晶体是否洗涤干净的方法是___________ ;已知常温下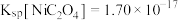 ,当溶液
,当溶液 时,
时, 沉淀完全[
沉淀完全[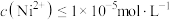 认为完全沉淀],则此时溶液中草酸的浓度
认为完全沉淀],则此时溶液中草酸的浓度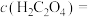
___________ (保留两位有效数字)。
(6)在空气中加热二水合草酸镍得到NiO,该反应的化学方程式为___________ 。
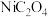 )是一种不溶于水的浅绿色粉末,常用于制镍催化剂和镍粉等。以铜镍合金废料(主要成分为镍和铜,含有一定量的铁和硅)为原料生产草酸镍的工艺流程如图:
)是一种不溶于水的浅绿色粉末,常用于制镍催化剂和镍粉等。以铜镍合金废料(主要成分为镍和铜,含有一定量的铁和硅)为原料生产草酸镍的工艺流程如图: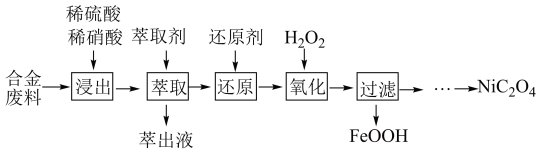
 、
、 、
、 、
、 、
、 、
、 ;
;②pH增大,
 被氧化的速率加快,同时生成的
被氧化的速率加快,同时生成的 水解形成的胶体能吸附
水解形成的胶体能吸附 ;
;③草酸的
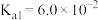 ,
,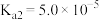 。
。回答下列问题:
(1)Ni在元素周期表中的位置是
(2)生产时为提高合金废料浸出率,下列措施可行的是
A.适当延长浸出时间 B.高温浸出 C.分批加入混酸浸取并搅拌
(3)“萃取”步骤中萃取除去的主要金属阳离子是
(4)“氧化”过程中,控制70℃、pH小于3的条件下进行。
①“氧化”过程的离子方程式为
②若pH大于3镍的回收率降低的原因是
(5)“过滤”后的滤液中加入
 溶液反应得到草酸镍,过滤得到的草酸镍需要用蒸馏水洗涤,检验晶体是否洗涤干净的方法是
溶液反应得到草酸镍,过滤得到的草酸镍需要用蒸馏水洗涤,检验晶体是否洗涤干净的方法是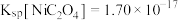 ,当溶液
,当溶液 时,
时, 沉淀完全[
沉淀完全[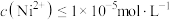 认为完全沉淀],则此时溶液中草酸的浓度
认为完全沉淀],则此时溶液中草酸的浓度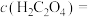
(6)在空气中加热二水合草酸镍得到NiO,该反应的化学方程式为
您最近半年使用:0次
名校
解题方法
2 .  (三氯化六氨合钴)是一种橙黄色的晶体,溶于热水和稀盐酸中,在冷水、乙醇、浓盐酸中溶解度较小,可用于制备其他三价钴配合物。实验室制备
(三氯化六氨合钴)是一种橙黄色的晶体,溶于热水和稀盐酸中,在冷水、乙醇、浓盐酸中溶解度较小,可用于制备其他三价钴配合物。实验室制备 的装置和步骤如下:
的装置和步骤如下: 、4.00g
、4.00g  和5mL高纯水,加热溶解后加入1.5g催化剂活性炭,7mL浓氨水,搅拌,得到
和5mL高纯水,加热溶解后加入1.5g催化剂活性炭,7mL浓氨水,搅拌,得到 (二氯化六氨合钴)溶液;
(二氯化六氨合钴)溶液;
②将得到的 溶液冷却至10℃,加入7mL 4%的
溶液冷却至10℃,加入7mL 4%的 ,恒温55℃,搅拌15min后冷却至2℃,抽滤,收集沉淀;
,恒温55℃,搅拌15min后冷却至2℃,抽滤,收集沉淀;
③将沉淀转移入100mL烧杯中,用20mL、80℃的高纯水进行冲洗,再加入1mL的浓盐酸,搅拌均匀,___________,将活性炭滤出弃去;
④在滤液中加入3.5mL试剂甲,搅拌后用冰水浴冷却至2℃析出沉淀,之后快速抽滤,弃去滤液,用试剂乙洗涤沉淀3次,低温烘干,得到产品2.14g。
回答下列问题:
(1)仪器a盛装的试剂是___________ 。
(2)常温下, ,从平衡角度解释,步骤①中先加
,从平衡角度解释,步骤①中先加 ,后加浓氨水的原因是
,后加浓氨水的原因是___________ 。
(3)步骤②中温度控制在55℃左右的原因是___________ 。
(4)步骤③中缺少的操作名称为___________ 。
(5)步骤④中:试剂甲和试剂乙选择合理的是___________ (填标号);
A.甲为浓盐酸,乙为水 B.甲为乙醇,乙为水 C.甲为浓盐酸,乙为乙醇
该反应的产率为___________ (已知: 的摩尔质量为267.5g/mol)。
的摩尔质量为267.5g/mol)。
(6)由 制备
制备 的化学方程式为
的化学方程式为___________ 。
 (三氯化六氨合钴)是一种橙黄色的晶体,溶于热水和稀盐酸中,在冷水、乙醇、浓盐酸中溶解度较小,可用于制备其他三价钴配合物。实验室制备
(三氯化六氨合钴)是一种橙黄色的晶体,溶于热水和稀盐酸中,在冷水、乙醇、浓盐酸中溶解度较小,可用于制备其他三价钴配合物。实验室制备 的装置和步骤如下:
的装置和步骤如下: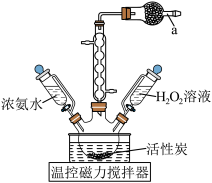
 、4.00g
、4.00g  和5mL高纯水,加热溶解后加入1.5g催化剂活性炭,7mL浓氨水,搅拌,得到
和5mL高纯水,加热溶解后加入1.5g催化剂活性炭,7mL浓氨水,搅拌,得到 (二氯化六氨合钴)溶液;
(二氯化六氨合钴)溶液;②将得到的
 溶液冷却至10℃,加入7mL 4%的
溶液冷却至10℃,加入7mL 4%的 ,恒温55℃,搅拌15min后冷却至2℃,抽滤,收集沉淀;
,恒温55℃,搅拌15min后冷却至2℃,抽滤,收集沉淀;③将沉淀转移入100mL烧杯中,用20mL、80℃的高纯水进行冲洗,再加入1mL的浓盐酸,搅拌均匀,___________,将活性炭滤出弃去;
④在滤液中加入3.5mL试剂甲,搅拌后用冰水浴冷却至2℃析出沉淀,之后快速抽滤,弃去滤液,用试剂乙洗涤沉淀3次,低温烘干,得到产品2.14g。
回答下列问题:
(1)仪器a盛装的试剂是
(2)常温下,
 ,从平衡角度解释,步骤①中先加
,从平衡角度解释,步骤①中先加 ,后加浓氨水的原因是
,后加浓氨水的原因是(3)步骤②中温度控制在55℃左右的原因是
(4)步骤③中缺少的操作名称为
(5)步骤④中:试剂甲和试剂乙选择合理的是
A.甲为浓盐酸,乙为水 B.甲为乙醇,乙为水 C.甲为浓盐酸,乙为乙醇
该反应的产率为
 的摩尔质量为267.5g/mol)。
的摩尔质量为267.5g/mol)。(6)由
 制备
制备 的化学方程式为
的化学方程式为
您最近半年使用:0次
名校
3 . 下列离子方程式错误的是
A.证明氧化性: |
B. 与 与 溶液混合呈中性: 溶液混合呈中性: |
C.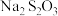 在酸性环境下不能稳定存在: 在酸性环境下不能稳定存在: |
D. 与烧碱溶液反应制水玻璃: 与烧碱溶液反应制水玻璃: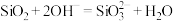 |
您最近半年使用:0次
名校
4 . 下列化学用语表示错误的是
A. 的空间填充模型: 的空间填充模型: |
B. 中,C原子与O原子之间形成 中,C原子与O原子之间形成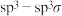 键 键 |
C.基态氧原子核外电子轨道表示式: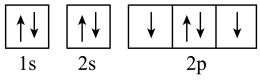 |
D.邻羟基苯甲醛分子内氢键示意图: |
您最近半年使用:0次
名校
5 . 甲酸甲酯常用作杀菌剂、熏蒸剂和烟草处理剂,可由甲酸和甲醇反应制得。 为阿伏加德罗常数的值。下列有关说法正确的是
为阿伏加德罗常数的值。下列有关说法正确的是
 为阿伏加德罗常数的值。下列有关说法正确的是
为阿伏加德罗常数的值。下列有关说法正确的是A.pH=3的甲酸溶液中氢离子数目为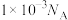 |
B.23g甲酸和8g甲醇中所含的氢原子数目均为 |
C.50g质量分数为64%的甲醇水溶液中含有σ键数目为 |
D.甲醇燃料电池中,每消耗22.4L(标准状况)甲醇,转移电子数目为 |
您最近半年使用:0次
6 . 草酸亚铁晶体( )是一种黄色难溶于水可溶于稀硫酸的固体,具有较强还原性,受热易分解,是生产电池、涂料以及感光材料的原材料。某化学活动小组分别设计了相应装置进行草酸亚铁的制备及其性质实验。回答下列问题:
)是一种黄色难溶于水可溶于稀硫酸的固体,具有较强还原性,受热易分解,是生产电池、涂料以及感光材料的原材料。某化学活动小组分别设计了相应装置进行草酸亚铁的制备及其性质实验。回答下列问题:
Ⅰ.制备草酸亚铁晶体(装置如图所示)___________ 、___________ 、过滤、洗涤、干燥。
(2)实验过程:先打开 和
和 ,待a中反应一段时间后,需要对开关进行的操作为
,待a中反应一段时间后,需要对开关进行的操作为___________ 。
Ⅱ.草酸亚铁晶体热分解产物的探究___________ 。
(4)装置C的作用为___________ 。
(5)从绿色化学考虑,该套装置存在的明显缺陷是___________ 。
(6)实验结束后,E中黑色固体变为红色,B、F中澄清石灰水变浑浊,a中无水硫酸铜变为蓝色,A中残留FeO,则A处反应管中发生反应的化学方程式为___________ 。
Ⅲ.运用热重分析法推测产物
称取54.0g草酸亚铁晶体( )加热分解,得到剩余固体质量随温度变化的曲线如图所示:
)加热分解,得到剩余固体质量随温度变化的曲线如图所示:___________ 。
 )是一种黄色难溶于水可溶于稀硫酸的固体,具有较强还原性,受热易分解,是生产电池、涂料以及感光材料的原材料。某化学活动小组分别设计了相应装置进行草酸亚铁的制备及其性质实验。回答下列问题:
)是一种黄色难溶于水可溶于稀硫酸的固体,具有较强还原性,受热易分解,是生产电池、涂料以及感光材料的原材料。某化学活动小组分别设计了相应装置进行草酸亚铁的制备及其性质实验。回答下列问题:Ⅰ.制备草酸亚铁晶体(装置如图所示)
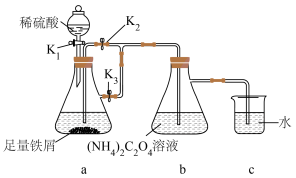
(2)实验过程:先打开
 和
和 ,待a中反应一段时间后,需要对开关进行的操作为
,待a中反应一段时间后,需要对开关进行的操作为Ⅱ.草酸亚铁晶体热分解产物的探究
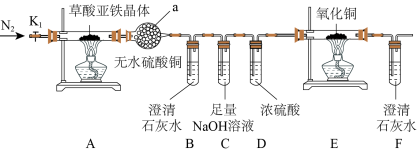
(4)装置C的作用为
(5)从绿色化学考虑,该套装置存在的明显缺陷是
(6)实验结束后,E中黑色固体变为红色,B、F中澄清石灰水变浑浊,a中无水硫酸铜变为蓝色,A中残留FeO,则A处反应管中发生反应的化学方程式为
Ⅲ.运用热重分析法推测产物
称取54.0g草酸亚铁晶体(
 )加热分解,得到剩余固体质量随温度变化的曲线如图所示:
)加热分解,得到剩余固体质量随温度变化的曲线如图所示: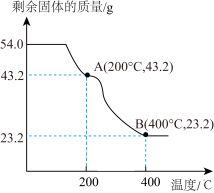
您最近半年使用:0次
7 . 下列反应的离子方程式书写正确的是
A.用醋酸处理水垢中的氢氧化镁: |
B.向次氯酸钙溶液通入足量二氧化碳: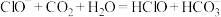 |
C.实验室电解饱和食盐水: |
D.向滴有酚酞的 溶液中加入 溶液中加入 溶液至溶液恰好变为无色: 溶液至溶液恰好变为无色: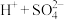  |
您最近半年使用:0次
解题方法
8 . 下列化学用语表达正确的是
A.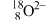 的结构示意图: 的结构示意图: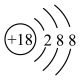 |
B.基态 的价电子排布图: 的价电子排布图: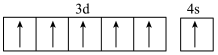 |
C.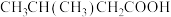 用系统命名法命名:3-甲基丁酸 用系统命名法命名:3-甲基丁酸 |
D. 的VSEPR模型: 的VSEPR模型: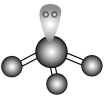 |
您最近半年使用:0次
解题方法
9 . 下列各组离子可能大量共存的是
A.在含大量 的溶液中: 的溶液中: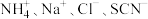 |
B.在含有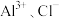 的溶液中: 的溶液中: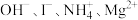 |
C.在含有大量 的溶液中: 的溶液中: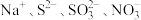 |
D.在溶质为 和 和 的溶液中: 的溶液中: |
您最近半年使用:0次
10 . 化学学习小组欲探究铁及其化合物的氧化性和还原性。请你协助他们完成实验报告。
实验目的:探究铁及其化合物的氧化性和还原性。
实验试剂及仪器:
试剂:氯化亚铁溶液、氯化铁溶液、氯水、 溶液、铁粉、锌片、铜片、稀硫酸。
溶液、铁粉、锌片、铜片、稀硫酸。
仪器:胶头滴管、试管、烧杯等。
(1)实验记录(仿照①实验作答,填写空白部分)。
(2)在实验②中,有部分同学在氯化亚铁溶液中滴入  溶液后,出现了红色,你认为是什么原因:
溶液后,出现了红色,你认为是什么原因:___________ ;你对实验员在配制氯化亚铁溶液时,提出的建议是___________ 。
实验目的:探究铁及其化合物的氧化性和还原性。
实验试剂及仪器:
试剂:氯化亚铁溶液、氯化铁溶液、氯水、
 溶液、铁粉、锌片、铜片、稀硫酸。
溶液、铁粉、锌片、铜片、稀硫酸。仪器:胶头滴管、试管、烧杯等。
(1)实验记录(仿照①实验作答,填写空白部分)。
| 序号 | 实验设计 | 实验现象 | 离子方程式 | 解释与结论 |
| ① | 在铁粉中滴入稀硫酸 | 铁粉溶解,溶液由无色变成浅绿色,生成无色无味气体 | 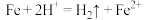 |  具有还原性 具有还原性 |
| ② |  溶液中滴入 溶液中滴入  溶液,再加氯水 溶液,再加氯水 | 滴入 溶液无明显变化,加入氯水立即变成红色 溶液无明显变化,加入氯水立即变成红色 | ||
| ③ |  溶液中加入锌片 溶液中加入锌片 |  | ||
| ④ |  |  具有氧化性 具有氧化性 |
 溶液后,出现了红色,你认为是什么原因:
溶液后,出现了红色,你认为是什么原因:
您最近半年使用:0次



