1 . 高效净水剂聚合氯化铝铁(PAFC)的组成可表示为 ,该物质广泛应用于日常生活用水和工业废水的处理。回答下列问题:
,该物质广泛应用于日常生活用水和工业废水的处理。回答下列问题:
(1)为检测PAFC中铝和铁元素的含量,采用如图所示流程进行。 中的A是
中的A是___________ 。
②步骤 中发生反应生成
中发生反应生成 中溶液离子方程式为
中溶液离子方程式为___________ 。
(2)某工厂欲以工业废料(铁、铁和铝的氧化物)为原料制取PAFC,设计如下流程:___________ , 的电子式为
的电子式为___________ 。
②所得酸性溶液中,一定大量存在的离子有___________ ;可能存在的离子有___________ ,证明该离子确实存在,可采用的操作(必须指明所采用的试剂及观察到的观象)是___________ 。
③步骤 中发生反应的离子方程式为
中发生反应的离子方程式为___________ 。
 ,该物质广泛应用于日常生活用水和工业废水的处理。回答下列问题:
,该物质广泛应用于日常生活用水和工业废水的处理。回答下列问题:(1)为检测PAFC中铝和铁元素的含量,采用如图所示流程进行。
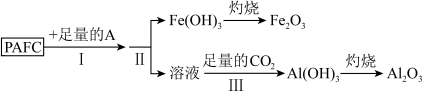
 中的A是
中的A是②步骤
 中发生反应生成
中发生反应生成 中溶液离子方程式为
中溶液离子方程式为(2)某工厂欲以工业废料(铁、铁和铝的氧化物)为原料制取PAFC,设计如下流程:

 的电子式为
的电子式为②所得酸性溶液中,一定大量存在的离子有
③步骤
 中发生反应的离子方程式为
中发生反应的离子方程式为
您最近半年使用:0次
2 . 若 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.标准状况下,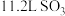 含有的分子数为 含有的分子数为 |
B.32g Cu在足量硫蒸气中完全反应失去的电子数为 |
C.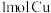 和含有 和含有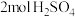 的浓硫酸反应,生成的 的浓硫酸反应,生成的 分子数目为 分子数目为 |
D.常温下,5.6g铁与硝酸反应,失去的电子数一定为 |
您最近半年使用:0次
3 . 用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.28gCO所含的分子数目为NA |
| B.lmol镁原子中含有的电子数为2NA |
| C.标准状况下,22.4LH2O含有的分子数目为NA |
| D.lmol/LNa2SO4溶液中含有的Na+的数目为2NA |
您最近半年使用:0次
解题方法
4 . 近年来我国航天航空事业飞速发展,下列有关叙述正确的是
| A.神舟十四号载人飞船发射过程中火箭点火产生动力的原理源于氧化还原反应 |
| B.返回舱降落过程中使用了芳纶纤维制作的降落伞绳,降落伞绳是高强度的合金钢 |
| C.太阳电池翼所使用的“碳纤维”(由聚丙烯腈经碳化而成)与金刚石互为同位素 |
| D.“天问一号”实验舱所使用的铝合金熔点高于其各组分金属 |
您最近半年使用:0次
名校
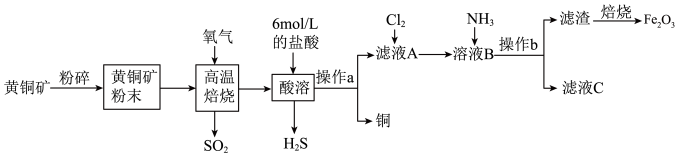
5 . Cu和Fe2O3在工农业生产中用途广泛,用黄铜矿(主要成分为CuFeS2,其中Cu为+2价,Fe为+2价)制取Cu和Fe2O3的工艺流程如图所示:__________ 。
(2)CuFeS2中S元素的化合价是______ ,高温焙烧时生成FeS及另外两种产物,则发生的化学反应方程式为____________ 。
(3)操作a为____________ 。
(4)向滤液A中通入Cl2的目的是__________ 。
(5)向溶液B中通入NH3发生反应的离子方程式为___________ 。
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
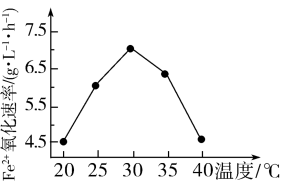
由下图可知,使用硫杆菌的最佳温度为______ ℃,若反应温度过高,反应速率下降,其原因是_______________ 。
(2)CuFeS2中S元素的化合价是
(3)操作a为
(4)向滤液A中通入Cl2的目的是
(5)向溶液B中通入NH3发生反应的离子方程式为
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4
 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O由下图可知,使用硫杆菌的最佳温度为
您最近半年使用:0次
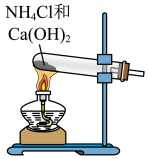
6 . 合成氨是人类科学技术发展史上的一项重大成就。实验室利用如右图所示装置及药品制取氨气:_____________ 。
(2)下列装置中,可用于收集氨的是_________ (填标号)。______________ 。
(4)在一定条件下,将2molN2和6molH2在体积恒为5L的密闭容器中混合,发生如下反应:N2(g)+3H2(g) 2NH3(g)。2min时测得容器内N2的物质的量为1.6mol,则:
2NH3(g)。2min时测得容器内N2的物质的量为1.6mol,则:
①2min内该反应的平均反应速率v(N2)=______ mol/(L·min)
②一段时间后反应达到平衡,密闭容器中混合气体的压强比反应前减少了25%,计算此时容器中NH3的浓度为____________ mol/L。
③能说明该反应已经达到平衡状态的是____________ 。
a.气体的密度保持不变 b.NH3的含量保持不变
c.N2和H2的物质的量之比为1:3 d.N2的转化率不再发生改变
(5)工业上通常用氨转化法处理含NO、NO2等氮氧化物的尾气:已知8 mol氨恰好能将含NO和NO2共7mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为_____ 。
(2)下列装置中,可用于收集氨的是
a. 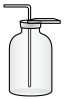 b.
b. 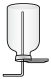 c.
c. 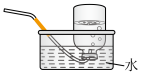
(4)在一定条件下,将2molN2和6molH2在体积恒为5L的密闭容器中混合,发生如下反应:N2(g)+3H2(g)
 2NH3(g)。2min时测得容器内N2的物质的量为1.6mol,则:
2NH3(g)。2min时测得容器内N2的物质的量为1.6mol,则:①2min内该反应的平均反应速率v(N2)=
②一段时间后反应达到平衡,密闭容器中混合气体的压强比反应前减少了25%,计算此时容器中NH3的浓度为
③能说明该反应已经达到平衡状态的是
a.气体的密度保持不变 b.NH3的含量保持不变
c.N2和H2的物质的量之比为1:3 d.N2的转化率不再发生改变
(5)工业上通常用氨转化法处理含NO、NO2等氮氧化物的尾气:已知8 mol氨恰好能将含NO和NO2共7mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为
您最近半年使用:0次
名校
解题方法
7 . 下列关于氮及其化合物的说法正确的是
| A.可用向上排空气法收集NO |
| B.NO在与水的反应中只做氧化剂 |
| C.将大气中游离态的氮转化为氮的化合物的过程叫氮的固定 |
| D.N2的化学性质稳定,任何情况下不与O2、H2等发生反应 |
您最近半年使用:0次
名校
8 . 下列过程中的化学反应,相应的离子方程式正确的是
| A.氢氧化钡与稀硫酸溶液混合:H++OH-=H2O |
| B.稀盐酸滴在铁片上:2Fe+6H+=2Fe3++3H2↑ |
| C.氯化亚铁溶液中通入Cl2:2Fe2++Cl2=2Fe3++2Cl- |
D.稀盐酸和碳酸钙反应制取CO2: +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
您最近半年使用:0次
名校
解题方法
9 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.含有7.8 g 的溶液中: 的溶液中: 的数目为 的数目为 |
B.1 L 1 mol⋅L 溴化铵水溶液中 溴化铵水溶液中 与 与 离子数之和大于 离子数之和大于 |
C.标准状况下,11.2 L  含有 含有 键的数目为 键的数目为 |
D.常温下,1 L  的 的 溶液中,由水电离出的 溶液中,由水电离出的 数目为 数目为 |
您最近半年使用:0次
2024-05-02更新
|
56次组卷
|
2卷引用:广西防城港市实验高级中学2023-2024学年高二下学期期中考试化学试题
名校
10 . 用可溶性 溶液生产纳米
溶液生产纳米 的一种工艺流程如下:
的一种工艺流程如下:
 溶液生产纳米
溶液生产纳米 的一种工艺流程如下:
的一种工艺流程如下: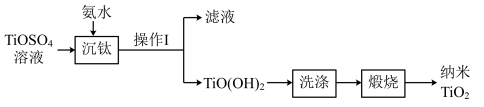
| A.实验室中进行“操作Ⅰ”时,需要的玻璃仪器有烧杯、玻璃棒、普通漏斗 |
B.“沉钛”时反应的离子方程式为: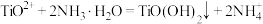 |
C.回收“滤液”中的 时,高温灼烧有利于提高其产率 时,高温灼烧有利于提高其产率 |
D.空气与纳米 所形成的分散系,可检测出有丁达尔效应 所形成的分散系,可检测出有丁达尔效应 |
您最近半年使用:0次



