1 . 用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.28gCO所含的分子数目为NA |
| B.lmol镁原子中含有的电子数为2NA |
| C.标准状况下,22.4LH2O含有的分子数目为NA |
| D.lmol/LNa2SO4溶液中含有的Na+的数目为2NA |
您最近一年使用:0次
名校
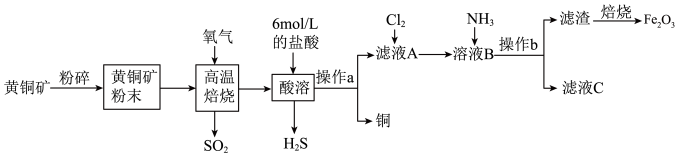
2 . Cu和Fe2O3在工农业生产中用途广泛,用黄铜矿(主要成分为CuFeS2,其中Cu为+2价,Fe为+2价)制取Cu和Fe2O3的工艺流程如图所示:__________ 。
(2)CuFeS2中S元素的化合价是______ ,高温焙烧时生成FeS及另外两种产物,则发生的化学反应方程式为____________ 。
(3)操作a为____________ 。
(4)向滤液A中通入Cl2的目的是__________ 。
(5)向溶液B中通入NH3发生反应的离子方程式为___________ 。
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
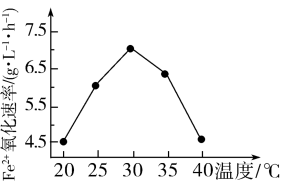
由下图可知,使用硫杆菌的最佳温度为______ ℃,若反应温度过高,反应速率下降,其原因是_______________ 。
(2)CuFeS2中S元素的化合价是
(3)操作a为
(4)向滤液A中通入Cl2的目的是
(5)向溶液B中通入NH3发生反应的离子方程式为
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4
 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O由下图可知,使用硫杆菌的最佳温度为
您最近一年使用:0次
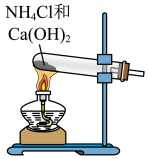
3 . 合成氨是人类科学技术发展史上的一项重大成就。实验室利用如右图所示装置及药品制取氨气:_____________ 。
(2)下列装置中,可用于收集氨的是_________ (填标号)。______________ 。
(4)在一定条件下,将2molN2和6molH2在体积恒为5L的密闭容器中混合,发生如下反应:N2(g)+3H2(g) 2NH3(g)。2min时测得容器内N2的物质的量为1.6mol,则:
2NH3(g)。2min时测得容器内N2的物质的量为1.6mol,则:
①2min内该反应的平均反应速率v(N2)=______ mol/(L·min)
②一段时间后反应达到平衡,密闭容器中混合气体的压强比反应前减少了25%,计算此时容器中NH3的浓度为____________ mol/L。
③能说明该反应已经达到平衡状态的是____________ 。
a.气体的密度保持不变 b.NH3的含量保持不变
c.N2和H2的物质的量之比为1:3 d.N2的转化率不再发生改变
(5)工业上通常用氨转化法处理含NO、NO2等氮氧化物的尾气:已知8 mol氨恰好能将含NO和NO2共7mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为_____ 。
(2)下列装置中,可用于收集氨的是
a. 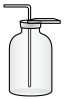 b.
b. 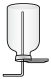 c.
c. 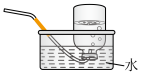
(4)在一定条件下,将2molN2和6molH2在体积恒为5L的密闭容器中混合,发生如下反应:N2(g)+3H2(g)
 2NH3(g)。2min时测得容器内N2的物质的量为1.6mol,则:
2NH3(g)。2min时测得容器内N2的物质的量为1.6mol,则:①2min内该反应的平均反应速率v(N2)=
②一段时间后反应达到平衡,密闭容器中混合气体的压强比反应前减少了25%,计算此时容器中NH3的浓度为
③能说明该反应已经达到平衡状态的是
a.气体的密度保持不变 b.NH3的含量保持不变
c.N2和H2的物质的量之比为1:3 d.N2的转化率不再发生改变
(5)工业上通常用氨转化法处理含NO、NO2等氮氧化物的尾气:已知8 mol氨恰好能将含NO和NO2共7mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为
您最近一年使用:0次
名校
解题方法
4 . 下列关于氮及其化合物的说法正确的是
| A.可用向上排空气法收集NO |
| B.NO在与水的反应中只做氧化剂 |
| C.将大气中游离态的氮转化为氮的化合物的过程叫氮的固定 |
| D.N2的化学性质稳定,任何情况下不与O2、H2等发生反应 |
您最近一年使用:0次
名校
5 . 下列过程中的化学反应,相应的离子方程式正确的是
| A.氢氧化钡与稀硫酸溶液混合:H++OH-=H2O |
| B.稀盐酸滴在铁片上:2Fe+6H+=2Fe3++3H2↑ |
| C.氯化亚铁溶液中通入Cl2:2Fe2++Cl2=2Fe3++2Cl- |
D.稀盐酸和碳酸钙反应制取CO2: +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
您最近一年使用:0次
解题方法
6 . 下表是元素周期表的一部分,针对表中的元素①~⑩,请用化学用语回答下列问题:
(1)在元素①~⑨中,原子半径最小的元素是___________ (填元素符号或化学式,下同),最高价氧化物对应水化物碱性最强的是___________ ;
(2)①③⑤⑨对应的简单离子中,离子半径最小的金属离子是___________ (填离子符号)。
(3)元素⑦、⑧对应的最简氢化物的稳定性由大到小顺序为___________ ;元素①做焰色试验时的颜色为___________ ;
(4)写出元素①的单质与元素⑧的单质在加热条件下反应生成的化合物的电子式:___________ 。
(5)元素⑤的最高价氧化物与元素①的最高价氧化物对应的水化物反应的离子方程式为___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ⑧ | |||||
| 3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
| 4 | ② | ④ |
(2)①③⑤⑨对应的简单离子中,离子半径最小的金属离子是
(3)元素⑦、⑧对应的最简氢化物的稳定性由大到小顺序为
(4)写出元素①的单质与元素⑧的单质在加热条件下反应生成的化合物的电子式:
(5)元素⑤的最高价氧化物与元素①的最高价氧化物对应的水化物反应的离子方程式为
您最近一年使用:0次
解题方法
7 . 我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。
联合制碱法的主要流程如下(部分物质已略去):___________ (填序号)。
(2)纯碱属于___________ (填“酸”“碱”或“盐”)。
(3)根据上述流程图,将化学方程式补充完整:___________ 。
 +___________+___________=___________↓+
+___________+___________=___________↓+
(4)向饱和食盐水中应先通___________ (填“ ”或“
”或“ ”)。
”)。
(5)煅烧 固体的化学方程式是
固体的化学方程式是___________ 。
(6)下列联合制碱法流程说法正确的是___________ (填字母)。
a.副产物 可用作肥料
可用作肥料
b.溶液B中一定含有 、
、 、
、
c.①中 析出是因为
析出是因为 不溶于水
不溶于水
(7)②这个步骤生成的产物可以循环使用的是___________ (填化学式)。
联合制碱法的主要流程如下(部分物质已略去):
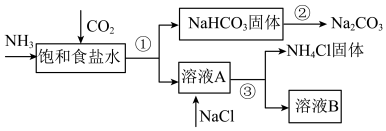
(2)纯碱属于
(3)根据上述流程图,将化学方程式补充完整:
 +___________+___________=___________↓+
+___________+___________=___________↓+
(4)向饱和食盐水中应先通
 ”或“
”或“ ”)。
”)。(5)煅烧
 固体的化学方程式是
固体的化学方程式是(6)下列联合制碱法流程说法正确的是
a.副产物
 可用作肥料
可用作肥料b.溶液B中一定含有
 、
、 、
、
c.①中
 析出是因为
析出是因为 不溶于水
不溶于水(7)②这个步骤生成的产物可以循环使用的是
您最近一年使用:0次
8 . 下列说法正确的是
A.胶体粒子的直径小于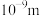 | B.白磷和红磷互为同素异形体 |
| C.胶体属于纯净物 | D. 和 和 互为同素异形体 互为同素异形体 |
您最近一年使用:0次
解题方法
9 . 下列离子方程式书写正确的是
A.碳酸钡与醋酸反应: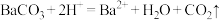 |
B.氯气与水反应: |
C.金属钠与水反应: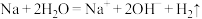 |
D.碳酸氢钙溶液中加入等物质的量的氢氧化钠溶液: |
您最近一年使用:0次
10 . 下列有关说法正确的是
A.中子数为8的碳原子: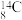 | B. 的比例模型: 的比例模型: |
C.Si原子的结构示意图: | D. 的电子式: 的电子式: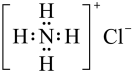 |
您最近一年使用:0次



