名校
解题方法
1 . 亚硝酸钙 可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应
可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应 利用如下装置制备亚硝酸钙(加热及夹持装置略)。
利用如下装置制备亚硝酸钙(加热及夹持装置略)。 溶液能将NO氧化为
溶液能将NO氧化为 。
。
回答下列问题:
(1)检查装置气密性,加入相应的试剂。先通 ,其目的是
,其目的是________ 。通 后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开
后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开 ,使稀硝酸滴入三颈烧瓶中;(iv)关闭
,使稀硝酸滴入三颈烧瓶中;(iv)关闭 ,打开
,打开 ,通入
,通入 。操作(ii)是
。操作(ii)是________ 。
(2)仪器a的名称为________ ,装置D中盛装的试剂是________ (填名称),装置E的作用是________ 。
(3)制备的产品 样品中含有杂质
样品中含有杂质 ,通过下列方法可测定产品的纯度:称量mg样品溶于水,加
,通过下列方法可测定产品的纯度:称量mg样品溶于水,加 固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作:
固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作: ;“还原
;“还原 ”时加入
”时加入 的
的 标准液,“滴定剩余
标准液,“滴定剩余 ”时消耗
”时消耗 的
的 标准溶液VmL。“滴定剩余
标准溶液VmL。“滴定剩余 ”过程中发生反应的离子方程式为
”过程中发生反应的离子方程式为________ ,样品中 的纯度为
的纯度为________ (用含m、V的式子表示)。
 可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应
可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应 利用如下装置制备亚硝酸钙(加热及夹持装置略)。
利用如下装置制备亚硝酸钙(加热及夹持装置略)。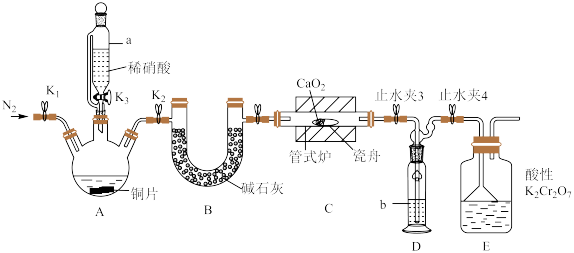
 溶液能将NO氧化为
溶液能将NO氧化为 。
。回答下列问题:
(1)检查装置气密性,加入相应的试剂。先通
 ,其目的是
,其目的是 后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开
后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开 ,使稀硝酸滴入三颈烧瓶中;(iv)关闭
,使稀硝酸滴入三颈烧瓶中;(iv)关闭 ,打开
,打开 ,通入
,通入 。操作(ii)是
。操作(ii)是(2)仪器a的名称为
(3)制备的产品
 样品中含有杂质
样品中含有杂质 ,通过下列方法可测定产品的纯度:称量mg样品溶于水,加
,通过下列方法可测定产品的纯度:称量mg样品溶于水,加 固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作:
固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作: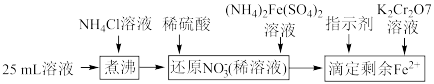
 ;“还原
;“还原 ”时加入
”时加入 的
的 标准液,“滴定剩余
标准液,“滴定剩余 ”时消耗
”时消耗 的
的 标准溶液VmL。“滴定剩余
标准溶液VmL。“滴定剩余 ”过程中发生反应的离子方程式为
”过程中发生反应的离子方程式为 的纯度为
的纯度为
您最近半年使用:0次
今日更新
|
2次组卷
|
2卷引用: 湖南省北师联盟2024届高三下学期模拟考试三模化学试题
2 . 二硼化钛(TiB2)是一种高熔点、高硬度、电阻小的导电陶瓷材料,在工业领域具有广泛的应用。利用废弃SCR催化剂(主要含TiO2、V2O5、Al2O3、SiO2等),制备TiB2并回收钒的工艺流程如图所示:
②B2O3高温下蒸气压大、易挥发;
③溶液酸性较强时,五价钒粒子主要以VO 的形式存在。
的形式存在。
回答下列问题:
(1)“酸浸”中生成TiO2+的离子方程式为_____ 。
(2)“滤渣①”的主要成分为_____ (填化学式)。
(3)“热水解”工艺中,经处理可循环利用的物质是_____ (填化学式)。
(4)“热还原”时生成一种可燃性气体,每制备1molTiB2,转移电子的物质的量为_____ mol。过程中B2O3的实际用量超过了理论用量,主要原因是_____ 。
(5)“沉钒”时,溶液pH过低或过高均不利于生成NH4VO3沉淀,原因是_____ 。
(6)含钛X晶体是一种高温超导母体,其晶胞结构如图甲所示(α=β=γ=90°),Ti原子与As原子构成的八面体如图乙所示,阿伏伽德罗常数的值为NA。回答下列问题:_____ 。
②X晶体的密度为_____ g·cm-3。
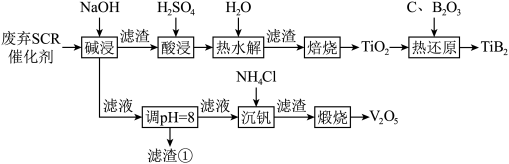
②B2O3高温下蒸气压大、易挥发;
③溶液酸性较强时,五价钒粒子主要以VO
 的形式存在。
的形式存在。回答下列问题:
(1)“酸浸”中生成TiO2+的离子方程式为
(2)“滤渣①”的主要成分为
(3)“热水解”工艺中,经处理可循环利用的物质是
(4)“热还原”时生成一种可燃性气体,每制备1molTiB2,转移电子的物质的量为
(5)“沉钒”时,溶液pH过低或过高均不利于生成NH4VO3沉淀,原因是
(6)含钛X晶体是一种高温超导母体,其晶胞结构如图甲所示(α=β=γ=90°),Ti原子与As原子构成的八面体如图乙所示,阿伏伽德罗常数的值为NA。回答下列问题:

②X晶体的密度为
您最近半年使用:0次
3 . 磷化氢(PH3)具有能量密度高、可再生优势,常用作新能源材料。一种工业上利用副产法制备PH3的流程如图所示:
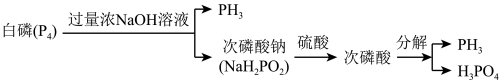
| A.白磷(P4)属于共价晶体 |
| B.次磷酸钠是酸式盐 |
| C.白磷与浓NaOH溶液反应,氧化剂与还原剂的物质的量之比为1:3 |
| D.流程中的每一步反应均属于氧化还原反应 |
您最近半年使用:0次
解题方法
4 . 能正确表示下列变化的离子方程式是
| A.甲醇碱性燃料电池负极方程式:CH3OH-6e-+H2O=CO2↑+6H+ |
B.铁粉与过量稀硝酸反应:Fe+NO +4H+=Fe3++NO↑+2H2O +4H+=Fe3++NO↑+2H2O |
C.亚硫酸氢钠的水解:HSO +H2O +H2O SO SO +H3O+ +H3O+ |
| D.硫酸铜溶液中通入硫化氢:Cu2++S2-=CuS↓ |
您最近半年使用:0次
解题方法
5 . 下列化学用语表述错误的是
A.碳化钙的电子式: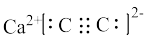 |
B.聚丙烯的结构简式: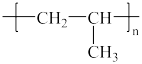 |
C.H2O2的分子结构示意图: |
D.邻羟基苯甲醛分子内氢键示意图: |
您最近半年使用:0次
名校
解题方法
6 . 高砷烟尘(主要成分有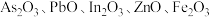 等)属于危险固体废弃物,对高砷烟尘进行综合处理回收
等)属于危险固体废弃物,对高砷烟尘进行综合处理回收 ,和金属铟的工业流程如下:
,和金属铟的工业流程如下: 在酸性溶液中以
在酸性溶液中以 或
或 形式存在,氧化性环境中主要存在
形式存在,氧化性环境中主要存在 ;
;
② 在
在 易分解为
易分解为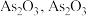 难溶于水;
难溶于水;
③ 。
。
回答下列问题:
(1)滤渣的主要成分为_______ (填化学式)。
(2)“高压酸浸”时, 的浸出率随硫酸浓度的增大而变化的曲线如图所示,硫酸浓度超过
的浸出率随硫酸浓度的增大而变化的曲线如图所示,硫酸浓度超过 时,
时, 的浸出率随硫酸浓度增大而略微减小的原因可能为
的浸出率随硫酸浓度增大而略微减小的原因可能为_______ 。 ,发生反应的离子方程式为
,发生反应的离子方程式为_______ 。已知 在水溶液中电离的总反应式为
在水溶液中电离的总反应式为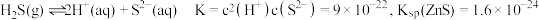 。当“硫化”操作后溶液中
。当“硫化”操作后溶液中 ,则此时溶液的
,则此时溶液的
_______ 。
(4)“还原”后溶液酸性增强,主要原因是_______ (用离子方程式表示)。
(5)“结晶”操作为_______ 、过滤、洗涤、干燥。
(6)“萃余液”中含有的金属阳离子为_______ (填离子符号),将 溶液电解得到金属铟,阴极的电极反应式为
溶液电解得到金属铟,阴极的电极反应式为_______ 。
(7)硫化铟铜是一种新型的纳米材料,具有优异的光电性能和光催化性能。一种由S、 三种元素组成的化合物的晶胞如图所示。采用
三种元素组成的化合物的晶胞如图所示。采用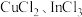 和
和 合成硫化铟铜薄膜,该反应的化学方程式是
合成硫化铟铜薄膜,该反应的化学方程式是_______ ,该晶胞的六个面均为矩形,上、下底面的晶胞参数为 ,高为
,高为 ,晶体密度为
,晶体密度为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为_______ (用含a、b、d的式子表示)。
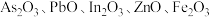 等)属于危险固体废弃物,对高砷烟尘进行综合处理回收
等)属于危险固体废弃物,对高砷烟尘进行综合处理回收 ,和金属铟的工业流程如下:
,和金属铟的工业流程如下: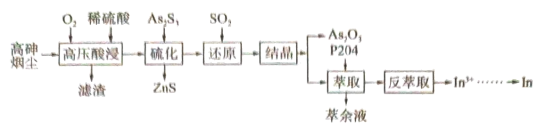
 在酸性溶液中以
在酸性溶液中以 或
或 形式存在,氧化性环境中主要存在
形式存在,氧化性环境中主要存在 ;
;②
 在
在 易分解为
易分解为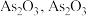 难溶于水;
难溶于水;③
 。
。回答下列问题:
(1)滤渣的主要成分为
(2)“高压酸浸”时,
 的浸出率随硫酸浓度的增大而变化的曲线如图所示,硫酸浓度超过
的浸出率随硫酸浓度的增大而变化的曲线如图所示,硫酸浓度超过 时,
时, 的浸出率随硫酸浓度增大而略微减小的原因可能为
的浸出率随硫酸浓度增大而略微减小的原因可能为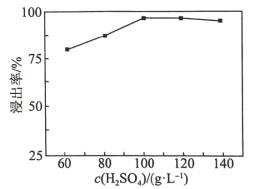
 ,发生反应的离子方程式为
,发生反应的离子方程式为 在水溶液中电离的总反应式为
在水溶液中电离的总反应式为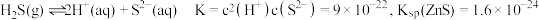 。当“硫化”操作后溶液中
。当“硫化”操作后溶液中 ,则此时溶液的
,则此时溶液的
(4)“还原”后溶液酸性增强,主要原因是
(5)“结晶”操作为
(6)“萃余液”中含有的金属阳离子为
 溶液电解得到金属铟,阴极的电极反应式为
溶液电解得到金属铟,阴极的电极反应式为(7)硫化铟铜是一种新型的纳米材料,具有优异的光电性能和光催化性能。一种由S、
 三种元素组成的化合物的晶胞如图所示。采用
三种元素组成的化合物的晶胞如图所示。采用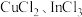 和
和 合成硫化铟铜薄膜,该反应的化学方程式是
合成硫化铟铜薄膜,该反应的化学方程式是 ,高为
,高为 ,晶体密度为
,晶体密度为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为
您最近半年使用:0次
名校
解题方法
7 . 下列陈述I和陈述II均正确,且有因果关系的是
| 选项 | 陈述I | 陈述II |
| A | 用 计测得等浓度的2-氯丙酸与2-氟丙酸溶液的 计测得等浓度的2-氯丙酸与2-氟丙酸溶液的 分别为 分别为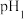 和 和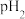 ,且 ,且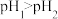 | 2-氯丙酸中 键的极性大于2-氟丙酸中 键的极性大于2-氟丙酸中 键的极性 键的极性 |
| B | 将氨气溶于水,进行导电性实验,灯泡亮 | 氨气是电解质 |
| C | 向 溶液中通入足量 溶液中通入足量 再滴加 再滴加 溶液,溶液不显红色 溶液,溶液不显红色 | 还原性: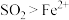 |
| D | 取少量涂改液,向其中加入足量硝酸银溶液,溶液出现白色沉淀 | 涂改液所含卤代烃中存在氯元素 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
8 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A. 时, 时, 的 的 溶液中 溶液中 的数目为 的数目为 |
B.标准状况下,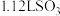 中所含分子数为 中所含分子数为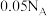 |
C.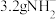 中含有的电子数和质子数均为 中含有的电子数和质子数均为 |
D. 中含有的 中含有的 键数为 键数为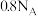 |
您最近半年使用:0次
名校
解题方法
9 . 建设美丽乡村,守护中华家园,衣食住行皆化学。下列与食品有关的叙述中没有涉及氧化还原反应的是
| A.用葡萄糖酸—δ—内酯做食品的凝固剂品 |
| B.用抗坏血酸做食品抗氧化剂 |
| C.将植物油氢化,以便运输和储存 |
| D.使用臭氧代替氯气进行自来水消毒 |
您最近半年使用:0次
10 . 科教兴国,我国科技发展在多个领域获得突破。下列说法错误的是
| A.新能源甲醇燃料电池汽车在行驶时其能量的转化形式:电能→化学能 |
| B.新一代航空发动机陶瓷基复合材料:具有耐高温、耐腐蚀特性 |
| C.X射线衍射实验:深度解析复杂晶体结构的晶胞参数 |
| D.火焰喷雾技术制备纳米材料:在高温火焰喷雾中形成的胶体属于气溶胶 |
您最近半年使用:0次



