名校
解题方法
1 . 氮的氧化物( )是大气污染物之一,含有氮氧化物的尾气需处理后才能排放。回答下列问题:
)是大气污染物之一,含有氮氧化物的尾气需处理后才能排放。回答下列问题:
(1)工业上在一定温度和催化剂条件下用 将
将 还原生成
还原生成 。
。
①如果选择图中A作为氨气的发生装置,对应反应的化学方程式为:_______ 。_______ :a→d→c→_______→_______→d→c→i。(按气流方向,用小写字母表示),F中倒置漏斗的作用是_______ 。
③若用通式 表示氮氧化物,则
表示氮氧化物,则_______ mol氨气(用含x表示)可将1mol的 转化为
转化为 。
。
(2)NO和 可用NaOH溶液吸收,主要反应:
可用NaOH溶液吸收,主要反应: ,
,
①下列措施能提高尾气中NO和 去除率的有
去除率的有_______ (填标号)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②将NO、 通入石灰乳中可制备重要的工业原料
通入石灰乳中可制备重要的工业原料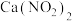 。该工艺需控制NO和
。该工艺需控制NO和 物质的量之比接近1:1,每生成
物质的量之比接近1:1,每生成 ,该反应转移的电子数为
,该反应转移的电子数为_______ (NA表示阿伏伽德罗常数)。若 ,则会导致
,则会导致_______ 。
 )是大气污染物之一,含有氮氧化物的尾气需处理后才能排放。回答下列问题:
)是大气污染物之一,含有氮氧化物的尾气需处理后才能排放。回答下列问题:(1)工业上在一定温度和催化剂条件下用
 将
将 还原生成
还原生成 。
。①如果选择图中A作为氨气的发生装置,对应反应的化学方程式为:

③若用通式
 表示氮氧化物,则
表示氮氧化物,则 转化为
转化为 。
。(2)NO和
 可用NaOH溶液吸收,主要反应:
可用NaOH溶液吸收,主要反应: ,
,
①下列措施能提高尾气中NO和
 去除率的有
去除率的有A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②将NO、
 通入石灰乳中可制备重要的工业原料
通入石灰乳中可制备重要的工业原料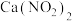 。该工艺需控制NO和
。该工艺需控制NO和 物质的量之比接近1:1,每生成
物质的量之比接近1:1,每生成 ,该反应转移的电子数为
,该反应转移的电子数为 ,则会导致
,则会导致
您最近一年使用:0次
名校
解题方法
2 . 下列离子方程式书写正确的是
A.红热的木炭与浓硝酸反应:C+4H++4 =CO2↑+4NO2↑+H2O =CO2↑+4NO2↑+H2O |
B.将二氧化硫通入酸性高锰酸钾溶液: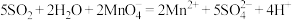 |
C.SO2使紫色石蕊溶液变红色:SO2+H2O= +2H+ +2H+ |
D.向NH4HSO3溶液中滴入过量的NaOH溶液: +H++2OH-=NH3·H2O+H2O +H++2OH-=NH3·H2O+H2O |
您最近一年使用:0次
名校
解题方法
3 . 研究人员拟设计黄铜矿(主要含 )制备硝酸铜和绿矾晶体的流程如下:
)制备硝酸铜和绿矾晶体的流程如下:
(1) 中铁元素的化合价为
中铁元素的化合价为_______ 价,已知“焙烧”生成 、CuO和
、CuO和 则其化学反应方程式为
则其化学反应方程式为_______ 。
(2)“置换”步骤中发生的所有反应的离子方程式有
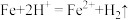 、
、_______ 。
(3)流程中“操作A”所需的玻璃仪器有烧杯、玻璃棒、_______ 。
(4)“浸洗”步骤中加入用于分离Cu、Fe的溶液A是_______ (填“稀 ”或“稀
”或“稀 ”)。
”)。
(5)“反应”步骤中,10% 为氧化剂,20%
为氧化剂,20% 提供
提供 ,可以避免污染性气体的产生,写出该“反应”的离子方程式:
,可以避免污染性气体的产生,写出该“反应”的离子方程式:_______ 。
(6)绿矾晶体( )在空气中极易变质;验证绿矾晶体已变质可选择的试剂为
)在空气中极易变质;验证绿矾晶体已变质可选择的试剂为_______ 。
 )制备硝酸铜和绿矾晶体的流程如下:
)制备硝酸铜和绿矾晶体的流程如下: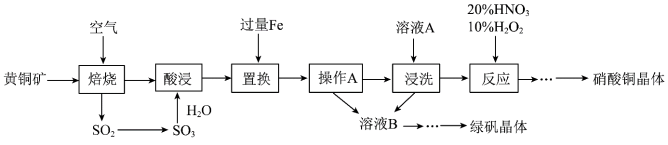
(1)
 中铁元素的化合价为
中铁元素的化合价为 、CuO和
、CuO和 则其化学反应方程式为
则其化学反应方程式为(2)“置换”步骤中发生的所有反应的离子方程式有

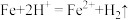 、
、(3)流程中“操作A”所需的玻璃仪器有烧杯、玻璃棒、
(4)“浸洗”步骤中加入用于分离Cu、Fe的溶液A是
 ”或“稀
”或“稀 ”)。
”)。(5)“反应”步骤中,10%
 为氧化剂,20%
为氧化剂,20% 提供
提供 ,可以避免污染性气体的产生,写出该“反应”的离子方程式:
,可以避免污染性气体的产生,写出该“反应”的离子方程式:(6)绿矾晶体(
 )在空气中极易变质;验证绿矾晶体已变质可选择的试剂为
)在空气中极易变质;验证绿矾晶体已变质可选择的试剂为
您最近一年使用:0次
名校
解题方法
4 . 研究实验发现硝酸的浓度越稀,硝酸发生氧化还原反应时,对应还原产物中氮元素的化合价越低。现有一定量的铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出,在反应结束后的溶液中逐滴加入5mol/LNaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量关系如图所示,下列说法不正确的是
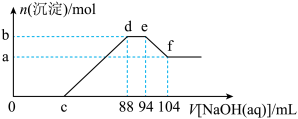
| A.该稀硝酸与铝粉、铁粉反应,其还原产物为硝酸铵 |
| B.c点对应NaOH溶液的体积为40mL |
| C.b点与a点的差值为0.03mol |
| D.样品中铝粉和铁粉的物质的量之比为5∶3 |
您最近一年使用:0次
名校
解题方法
5 . 在酸性溶液中,下列各组离子能在水溶液中大量共存的是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
6 . 设NA表示阿伏加德罗常数的值,下列叙述正确的是
A.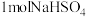 熔融态时含有NA个 熔融态时含有NA个 离子 离子 |
B. 气体中氧原子总数为3NA 气体中氧原子总数为3NA |
C.氧原子总数为0.2NA的 和 和 的混合气体,其体积为2.24L 的混合气体,其体积为2.24L |
D.1mol/L的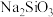 水溶液中含有的氧原子数为3 NA 水溶液中含有的氧原子数为3 NA |
您最近一年使用:0次
名校
解题方法
7 . 将 和空气的混合气体通入
和空气的混合气体通入 、
、 、
、 的混合溶液中反应回收
的混合溶液中反应回收 ,其物质转化如图所示。下列说法正确的是
,其物质转化如图所示。下列说法正确的是
 和空气的混合气体通入
和空气的混合气体通入 、
、 、
、 的混合溶液中反应回收
的混合溶液中反应回收 ,其物质转化如图所示。下列说法正确的是
,其物质转化如图所示。下列说法正确的是
| A.在图示的转化中,化合价不变的元素只有铜 |
B.根据图示可知 、 、 均能氧化 均能氧化 |
C.回收 的总反应为 的总反应为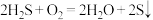 |
D.在图示的转化中发生的反应有 |
您最近一年使用:0次
名校
8 . 铊(Tl)广泛用于电子、军工、航天、化工、治金、通讯等方面,一种以红铊矿(主要成分是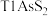 ,含少量
,含少量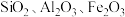 ,等杂质)为原料制备金属铊的流程如图所示。
,等杂质)为原料制备金属铊的流程如图所示。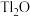 )膜,而失去金属光泽变得灰暗。
)膜,而失去金属光泽变得灰暗。
②TlCl难溶于水,而 溶于水。
溶于水。
③溶液中金属离子开始沉淀和完全沉淀的 如下表所示:
如下表所示:
回答下列问题:
(1) 中三元素的基态原子含有未成对电子数最多的元素是
中三元素的基态原子含有未成对电子数最多的元素是_______ 。(填元素符号)
(2)“焙烧1”中, 最终转化为
最终转化为 ﹔
﹔ 和
和 也转化为相应的硫酸盐。其中,
也转化为相应的硫酸盐。其中, 转化为
转化为 分如下两步完成。请写出第二步反应的化学方程式。
分如下两步完成。请写出第二步反应的化学方程式。
第一步( 与
与 反应):
反应):
第二步:_______ 。
(3)滤渣的成分 属于共价晶体,晶体中每个最小环含有
属于共价晶体,晶体中每个最小环含有_______ 个原子。
(4)“沉铊”步骤中,需要加入过量 ,其原因是
,其原因是_______ 。(用化学用语和简要的文字解释)
(5)向“沉铊”后的滤液中加入生石灰至 时才能外排,此时滤液中的
时才能外排,此时滤液中的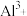 浓度为
浓度为_______  。(指数允许是小数)
。(指数允许是小数)
(6)“焙烧2”中发生的反应为 。则“置换”步骤中发生反应的离子方程式为
。则“置换”步骤中发生反应的离子方程式为_______ 。
(7)所得产品高纯铊应保存在_______ 中。
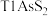 ,含少量
,含少量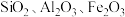 ,等杂质)为原料制备金属铊的流程如图所示。
,等杂质)为原料制备金属铊的流程如图所示。
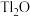 )膜,而失去金属光泽变得灰暗。
)膜,而失去金属光泽变得灰暗。②TlCl难溶于水,而
 溶于水。
溶于水。③溶液中金属离子开始沉淀和完全沉淀的
 如下表所示:
如下表所示:| 金属离子 |  |  |
开始沉淀的 | 2.2 | 3.5 |
沉淀完全( )的 )的 | 3.2 | 4.7 |
(1)
 中三元素的基态原子含有未成对电子数最多的元素是
中三元素的基态原子含有未成对电子数最多的元素是(2)“焙烧1”中,
 最终转化为
最终转化为 ﹔
﹔ 和
和 也转化为相应的硫酸盐。其中,
也转化为相应的硫酸盐。其中, 转化为
转化为 分如下两步完成。请写出第二步反应的化学方程式。
分如下两步完成。请写出第二步反应的化学方程式。第一步(
 与
与 反应):
反应):
第二步:
(3)滤渣的成分
 属于共价晶体,晶体中每个最小环含有
属于共价晶体,晶体中每个最小环含有(4)“沉铊”步骤中,需要加入过量
 ,其原因是
,其原因是(5)向“沉铊”后的滤液中加入生石灰至
 时才能外排,此时滤液中的
时才能外排,此时滤液中的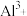 浓度为
浓度为 。(指数允许是小数)
。(指数允许是小数)(6)“焙烧2”中发生的反应为
 。则“置换”步骤中发生反应的离子方程式为
。则“置换”步骤中发生反应的离子方程式为(7)所得产品高纯铊应保存在
您最近一年使用:0次
名校
解题方法
9 . 下列化学用语正确的是
| A.聚丙烯的结构简式:﹣CH2﹣CH2﹣CH2﹣ |
B.丙烷分子的比例模型: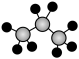 |
C.四氯化碳分子的电子式: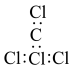 |
| D.溴乙烷的分子式:C2H5Br |
您最近一年使用:0次
名校
10 . 钒的用途十分广泛,有金属“维生素”之称。以含钒石煤(主要成分是V2O3、V2O4,含有的杂质有SiO2、FeS2及Mg、Al、Mn等的化合物)制备单质钒的工艺流程如图所示。
②Ksp(CaCO3)=2.8×10-9,Ksp(CaSiO3)=2.5×10-8,Ksp[Ca(VO3)2]远大于Ksp(CaCO3)。
回答下列问题:
(1)写出Cr3+的核外电子排布式为________ 。
(2)为了提高“焙烧”效率,可采取的措施有______ 。
(3)“焙烧”时,V2O3、V2O4都转化为Ca(VO3)2,写出V2O4转化为Ca(VO3)2的化学方程式:_____ 。
(4)“水浸”加入Na2CO3调节溶液的pH为8.5,可完全除去的金属离子有______ ;“水浸”加入过量Na2CO3不能使CaSiO3完全转化为CaCO3,原因是_______ 。(列式计算平衡常数分析该反应进行的趋势,一般认为,K>105时反应进行较完全,K<105时反应难以进行)
(5)“离子交换”与“洗脱”可表示为[RCl4]+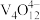
 [R-V4O12]+4Cl- ([RCl4]为强碱性阴离子交换树脂,
[R-V4O12]+4Cl- ([RCl4]为强碱性阴离子交换树脂,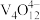 为
为 在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用
在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用_____ 。
(6)下列金属冶炼方法中,与本工艺流程中冶炼钒的方法相似的是____ (填字母)。
A.铝热反应制锰 B.电解熔融氯化钠制钠 C.氧化汞分解制汞

| 金属离子 | Fe3+ | Mg2+ | Al3+ | Mn2+ |
| 开始沉淀时的pH | 1.9 | 7.0 | 3.0 | 8.1 |
| 完全沉淀时的pH | 3.2 | 9.0 | 4.7 | 10.1 |
回答下列问题:
(1)写出Cr3+的核外电子排布式为
(2)为了提高“焙烧”效率,可采取的措施有
(3)“焙烧”时,V2O3、V2O4都转化为Ca(VO3)2,写出V2O4转化为Ca(VO3)2的化学方程式:
(4)“水浸”加入Na2CO3调节溶液的pH为8.5,可完全除去的金属离子有
(5)“离子交换”与“洗脱”可表示为[RCl4]+
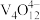
 [R-V4O12]+4Cl- ([RCl4]为强碱性阴离子交换树脂,
[R-V4O12]+4Cl- ([RCl4]为强碱性阴离子交换树脂,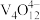 为
为 在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用
在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用(6)下列金属冶炼方法中,与本工艺流程中冶炼钒的方法相似的是
A.铝热反应制锰 B.电解熔融氯化钠制钠 C.氧化汞分解制汞
您最近一年使用:0次



