名校
1 . 下列解释事实的方程式不正确 的是
A.SO2通入澄清石灰水变浑浊: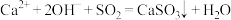 |
B.氯化钡溶液与稀硫酸反应: |
C.氨气溶于水溶液呈碱性: |
D.Cu与稀HNO3混合产生无色气体: |
您最近一年使用:0次
2 . 下列化学用语正确的是
A.CH4分子的球棍模型: | B.乙烯的结构简式:CH2CH2 |
| C.1,3―丁二烯的分子式:C4H8 | D.聚丙烯的结构简式: |
您最近一年使用:0次
3 . 工业上制备下列物质的生产流程不合理 的是
A.由铝土矿冶炼铝:铝土矿 |
B.由黄铁矿制硫酸:黄铁矿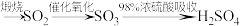 |
C.工业制硝酸: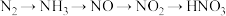 |
D.由石英砂制高纯硅:石英砂 粗硅 粗硅 纯硅 纯硅 |
您最近一年使用:0次
名校
解题方法
4 . 下列电子式书写正确的是
A.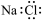 | B. | C. | D.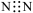 |
您最近一年使用:0次
名校
5 . 化学科学需要借助化学专用语言描述,下列有关化学用语不正确的是
A. 的电子式: 的电子式: |
B.质量数为14的碳原子: |
C.用电子式表示氯化钠的形成过程: |
D. 的结构示意图: 的结构示意图: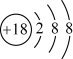 |
您最近一年使用:0次
名校
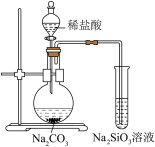
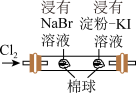
6 . 下列图中的实验方案,能达到实验目的的是
| 选项 | A | B |
| 方案 |
|
|
| 目的 | 证明非金属性:Cl>C>Si | 氧化性: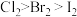 |
| 选项 | C | D |
| 方案 |
|
|
| 目的 | 反应开始后,U形管液面左高右低,证明是吸热反应 | 证明化学能转化为电能 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 高一年级小村同学最近通过学习了解到:“肼”(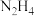 )是一种重要的化学物质,可用作喷气式发动机燃料、火箭燃料、显影剂、抗氧剂、还原剂等。请结合数据完成下面有关“肼”的化学问题。
)是一种重要的化学物质,可用作喷气式发动机燃料、火箭燃料、显影剂、抗氧剂、还原剂等。请结合数据完成下面有关“肼”的化学问题。
(1)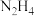 属于
属于_______ 化合物(填“离子化合物”或“共价化合物”),所含化学键类型有_______ (填“离子键”或“极性键”或“非极性键”)
(2)已知①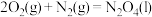
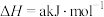
②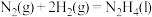
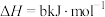
③
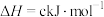
某型号火箭采用液态肼和液态 作推进剂,燃烧生成两种无污染气体。写出反应的热化学方程式
作推进剂,燃烧生成两种无污染气体。写出反应的热化学方程式________ 。
(3)液态肼可以除去水中的溶解氧,且生成物能参与大气循环。写出该反应的热化学方程式________ ,理论上每消耗64 g肼可除去标准状况下
________ L。
(4)科学家用肼作为燃料电池的燃料,电池结构如图所示,写出负极的电极反应式_________ 。
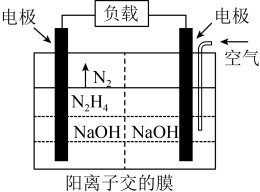
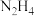 )是一种重要的化学物质,可用作喷气式发动机燃料、火箭燃料、显影剂、抗氧剂、还原剂等。请结合数据完成下面有关“肼”的化学问题。
)是一种重要的化学物质,可用作喷气式发动机燃料、火箭燃料、显影剂、抗氧剂、还原剂等。请结合数据完成下面有关“肼”的化学问题。(1)
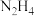 属于
属于(2)已知①
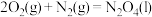
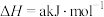
②
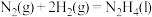
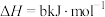
③

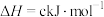
某型号火箭采用液态肼和液态
 作推进剂,燃烧生成两种无污染气体。写出反应的热化学方程式
作推进剂,燃烧生成两种无污染气体。写出反应的热化学方程式(3)液态肼可以除去水中的溶解氧,且生成物能参与大气循环。写出该反应的热化学方程式

(4)科学家用肼作为燃料电池的燃料,电池结构如图所示,写出负极的电极反应式

您最近一年使用:0次
名校
8 . SO2、NOx为常见的空气污染物,会引起酸雨、光化学烟雾等污染问题。研究者以多种方法进行“脱硫”“脱硝”。
(1)利用工业废碱渣(主要成分为Na2CO3)来吸收含SO2的烟气,同时得到Na2SO3粗品。其流程如图所示:___________ ;
②SO2被Na2CO3溶液吸收时,会释放出一种无色无味气体,该反应的离子方程式为___________ 。
(2)利用含有SO2的烟气制备NaClO2。其流程如图所示:___________ 。
②反应b中的氧化剂和还原剂的物质的量之比为___________ 。
(3)以NaClO溶液作为吸收剂进行一体化“脱硫”“脱硝”。控制溶液的pH=5.5,一定时间内,温度对SO2、NO脱除率的影响如图所示: 、NO
、NO 。
。
①NO在吸收过程中,反应的离子方程式是___________ 。
②50℃时,吸收液中烟气转化生成的Cl‒和NO 的物质的量之比为
的物质的量之比为___________ 。
③烟气中NOx含量的测定:将VL气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO ,加水稀释至100mL。量取25mL该溶液,加入V1mLc1mol·L‒1FeSO4溶液(过量),充分反应后,用c2mol·L‒1K2Cr2O7溶液和剩余的Fe2+恰好反应(该反应的还原产物为Cr3+),消耗V2mL。气样中NOx折合成NO的含量为
,加水稀释至100mL。量取25mL该溶液,加入V1mLc1mol·L‒1FeSO4溶液(过量),充分反应后,用c2mol·L‒1K2Cr2O7溶液和剩余的Fe2+恰好反应(该反应的还原产物为Cr3+),消耗V2mL。气样中NOx折合成NO的含量为___________ mg·L‒1。
(1)利用工业废碱渣(主要成分为Na2CO3)来吸收含SO2的烟气,同时得到Na2SO3粗品。其流程如图所示:
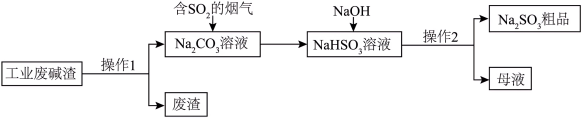
②SO2被Na2CO3溶液吸收时,会释放出一种无色无味气体,该反应的离子方程式为
(2)利用含有SO2的烟气制备NaClO2。其流程如图所示:
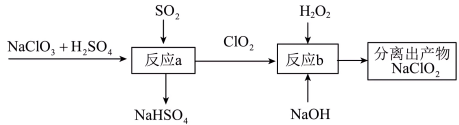
②反应b中的氧化剂和还原剂的物质的量之比为
(3)以NaClO溶液作为吸收剂进行一体化“脱硫”“脱硝”。控制溶液的pH=5.5,一定时间内,温度对SO2、NO脱除率的影响如图所示:
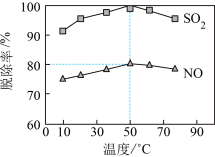
 、NO
、NO 。
。①NO在吸收过程中,反应的离子方程式是
②50℃时,吸收液中烟气转化生成的Cl‒和NO
 的物质的量之比为
的物质的量之比为③烟气中NOx含量的测定:将VL气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO
 ,加水稀释至100mL。量取25mL该溶液,加入V1mLc1mol·L‒1FeSO4溶液(过量),充分反应后,用c2mol·L‒1K2Cr2O7溶液和剩余的Fe2+恰好反应(该反应的还原产物为Cr3+),消耗V2mL。气样中NOx折合成NO的含量为
,加水稀释至100mL。量取25mL该溶液,加入V1mLc1mol·L‒1FeSO4溶液(过量),充分反应后,用c2mol·L‒1K2Cr2O7溶液和剩余的Fe2+恰好反应(该反应的还原产物为Cr3+),消耗V2mL。气样中NOx折合成NO的含量为
您最近一年使用:0次
7日内更新
|
182次组卷
|
2卷引用:北师大附属实验中学2023-2024学年度第二学期期中试卷
名校
9 . 硫化氢(H2S)是一种有毒气体,高于200℃分解,溶于水显弱酸性,脱除H2S的方法很多。
(1)Na2CO3吸收H2S。含H2S的气体与饱和Na2CO3溶液在吸收塔内逆流接触,生成两种酸式盐。该反应的离子方程式为___________ 。
(2)干法脱硫技术。
①铁系脱硫剂:活性氧化铁(Fe2O3•H2O)是经典而有效的脱硫剂,脱硫反应:Fe2O3•H2O+H2S→FeS+S+H2O,再生反应:FeS+H2O+O2→Fe2O3•H2O+S(脱硫反应和再生反应均未配平)。
a.Fe2O3•H2O在该反应中的作用可描述为___________ 。
b.若处理标况下4.48LH2S时,理论上消耗O2的物质的量为___________ 。
②锌系脱硫剂:550℃时,将H2S和还原性气体H2按一定比例混合,以一定的流速通过装有锌的复合金属脱硫剂(ZnFe2O4)的反应器,脱硫过程中,ZnFe2O4与H2S、H2反应生成了ZnS、FeS和H2O,其化学方程式为___________ 。
(3)生物脱硫技术。
天然气是一种重要的化工原料和燃料,常含有少量H2S。H2S与碱反应转化为HS‒,在脱氮硫杆菌参与下,HS‒被NO 氧化为SO
氧化为SO 、NO
、NO 被还原为N2。当33.6m3(标准状况)某燃气(H2S的体积分数为0.2%)脱硫时,消耗NO
被还原为N2。当33.6m3(标准状况)某燃气(H2S的体积分数为0.2%)脱硫时,消耗NO 的物质的量为
的物质的量为___________ mol。
(1)Na2CO3吸收H2S。含H2S的气体与饱和Na2CO3溶液在吸收塔内逆流接触,生成两种酸式盐。该反应的离子方程式为
(2)干法脱硫技术。
①铁系脱硫剂:活性氧化铁(Fe2O3•H2O)是经典而有效的脱硫剂,脱硫反应:Fe2O3•H2O+H2S→FeS+S+H2O,再生反应:FeS+H2O+O2→Fe2O3•H2O+S(脱硫反应和再生反应均未配平)。
a.Fe2O3•H2O在该反应中的作用可描述为
b.若处理标况下4.48LH2S时,理论上消耗O2的物质的量为
②锌系脱硫剂:550℃时,将H2S和还原性气体H2按一定比例混合,以一定的流速通过装有锌的复合金属脱硫剂(ZnFe2O4)的反应器,脱硫过程中,ZnFe2O4与H2S、H2反应生成了ZnS、FeS和H2O,其化学方程式为
(3)生物脱硫技术。
天然气是一种重要的化工原料和燃料,常含有少量H2S。H2S与碱反应转化为HS‒,在脱氮硫杆菌参与下,HS‒被NO
 氧化为SO
氧化为SO 、NO
、NO 被还原为N2。当33.6m3(标准状况)某燃气(H2S的体积分数为0.2%)脱硫时,消耗NO
被还原为N2。当33.6m3(标准状况)某燃气(H2S的体积分数为0.2%)脱硫时,消耗NO 的物质的量为
的物质的量为
您最近一年使用:0次
7日内更新
|
70次组卷
|
2卷引用:北师大附属实验中学2023-2024学年度第二学期期中试卷
名校
解题方法
10 . 下列离子方程式书写正确的是
A.酸化的FeSO4溶液长时间存放变黄:4H++2Fe2++SO =2Fe3++SO2↑+2H2O =2Fe3++SO2↑+2H2O |
B.向(NH4)2SO4溶液中滴加Ba(OH)2溶液:NH +SO +SO +Ba2++OH−=NH3·H2O+BaSO4↓ +Ba2++OH−=NH3·H2O+BaSO4↓ |
C.向FeCl3溶液中通入SO2,黄色溶液变为浅绿色:SO2+2Fe3++2H2O=SO +2Fe2++4H+ +2Fe2++4H+ |
D.过量铁粉与稀硝酸反应,产生无色气体:Fe+NO +4H+=Fe3++NO↑+2H2O +4H+=Fe3++NO↑+2H2O |
您最近一年使用:0次
7日内更新
|
154次组卷
|
2卷引用:北师大附属实验中学2023-2024学年度第二学期期中试卷