名校
1 . 下列离子方程式书写正确的是
A.向硫酸铝熔液中加入过量氨水: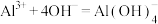 |
B.将 通入冷的石灰乳中制备漂白粉: 通入冷的石灰乳中制备漂白粉: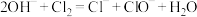 |
C.铁与过量稀硝酸反应: |
D.二氧化硫通入氯化钡溶液中: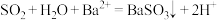 |
您最近半年使用:0次
2 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.将2mol NO和2mol  混合,充分反应后体系中原子总数为8 混合,充分反应后体系中原子总数为8 |
B.标准状况下,22.4L  中所含原子数为4 中所含原子数为4 |
C.1mol的铁与足量的硫粉发生反应,转移的电子数为3 |
D.100g质量分数为9.8%的 水溶液中所含氧原子数目为0.4 水溶液中所含氧原子数目为0.4 |
您最近半年使用:0次
名校
3 . 在酸性溶液中,下列离子能大量共存的是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近半年使用:0次
名校
4 . 下列反应既属于氧化还原反应,又属于吸热反应的是
A. 与 与 的反应 的反应 | B.液氮做冷却剂 |
C. | D.过氧化钠与水反应 |
您最近半年使用:0次
名校
解题方法
5 .  四种易溶于水的化合物只由表中的八种离子组成,且四种化合物中阴、阳离子各不相同。
四种易溶于水的化合物只由表中的八种离子组成,且四种化合物中阴、阳离子各不相同。
已知:A溶液呈强酸性,且A溶液与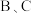 溶液混合均产生白色沉淀,
溶液混合均产生白色沉淀, 的焰色反应呈黄色。
的焰色反应呈黄色。
回答下列问题:
(1)写出C的化学式:_____________ , 的电子式:
的电子式:_____________ 。
(2)写出A溶液与 溶液反应的离子方程式:
溶液反应的离子方程式:_____________ 。
(3)A中阴离子的检验操作_____________________________________ 。
(4)请选出适合存放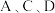 溶液的试剂瓶的序号:(每空1分)
溶液的试剂瓶的序号:(每空1分)
 四种易溶于水的化合物只由表中的八种离子组成,且四种化合物中阴、阳离子各不相同。
四种易溶于水的化合物只由表中的八种离子组成,且四种化合物中阴、阳离子各不相同。| 阴离子 | 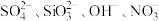 |
| 阳离子 | 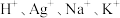 |
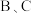 溶液混合均产生白色沉淀,
溶液混合均产生白色沉淀, 的焰色反应呈黄色。
的焰色反应呈黄色。回答下列问题:
(1)写出C的化学式:
 的电子式:
的电子式:(2)写出A溶液与
 溶液反应的离子方程式:
溶液反应的离子方程式:(3)A中阴离子的检验操作
(4)请选出适合存放
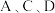 溶液的试剂瓶的序号:(每空1分)
溶液的试剂瓶的序号:(每空1分)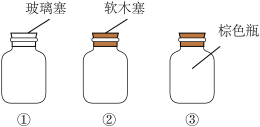
溶液 | A | C |
|
试剂瓶序号 |
您最近半年使用:0次
名校
解题方法
6 . 某溶液含有下列离子中的几种: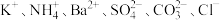 ,取该溶液进行如下实验
,取该溶液进行如下实验
(1)取该溶液与足量 溶液共热产生刺激性气体
溶液共热产生刺激性气体
(2)另取该溶液加入稀 无明显现象,再加足量
无明显现象,再加足量 溶液得到白色沉淀
溶液得到白色沉淀
(3)取(2)的上层清液加入 溶液和稀硝酸得到白色沉淀
溶液和稀硝酸得到白色沉淀
下列结论正确的是
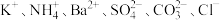 ,取该溶液进行如下实验
,取该溶液进行如下实验(1)取该溶液与足量
 溶液共热产生刺激性气体
溶液共热产生刺激性气体(2)另取该溶液加入稀
 无明显现象,再加足量
无明显现象,再加足量 溶液得到白色沉淀
溶液得到白色沉淀(3)取(2)的上层清液加入
 溶液和稀硝酸得到白色沉淀
溶液和稀硝酸得到白色沉淀下列结论正确的是
A.一定含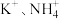 ,一定不含 ,一定不含 | B.一定含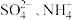 ,一定不含 ,一定不含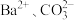 |
C.一定含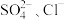 ,可能含 ,可能含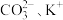 | D.一定含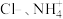 ,可能含 ,可能含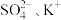 |
您最近半年使用:0次
名校
解题方法
7 . 能正确表示下列反应的方程式的是
A.向澄清的石灰水中通入 气体: 气体: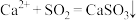 |
B.单质硅溶于烧碱溶液中: |
C. 的催化氧化反应: 的催化氧化反应: |
D.向氢硫酸 中通入氯气: 中通入氯气: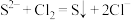 |
您最近半年使用:0次
8 . 四氧化三铁俗称磁性氧化铁,常用于制造录音磁带和电讯器材,也可作颜料和抛光剂。某工厂以硫铁矿烧渣(主要含有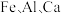 等元素的氧化物及
等元素的氧化物及 )为原料,制备
)为原料,制备 的工艺流程如图所示。
的工艺流程如图所示。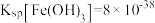 、
、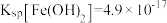 、
、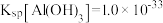 。
。
回答下列问题:
(1)“酸溶”硫铁矿烧渣时,为了加快酸溶速率可采取的措施有___________ (任写两条)。
(2)料渣1的主要成分有___________ (填化学式)。
(3)常温下,已知溶液中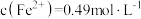 ,要使
,要使 沉淀完全,则“调
沉淀完全,则“调 ”的范围是
”的范围是___________ (保留2位有效数字,一般离子浓度 认为沉淀完全)。
认为沉淀完全)。
(4)加入 “沉铁”时,发生反应的离子方程式为
“沉铁”时,发生反应的离子方程式为___________ 。
(5)①“煅烧1”的目的是将 转化为
转化为 ,若“煅烧2”阶段发生反应时
,若“煅烧2”阶段发生反应时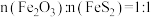 ,则该反应的化学方程式为
,则该反应的化学方程式为___________ 。
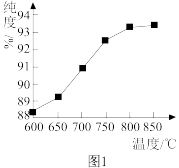
②“煅烧2”时温度对 的纯度有很大影响。已知温度对
的纯度有很大影响。已知温度对 纯度的影响如图1所示,则“煅烧2”时,温度最好控制在
纯度的影响如图1所示,则“煅烧2”时,温度最好控制在___________  。
。 )的晶胞如图2所示。已知:该晶胞底边边长为
)的晶胞如图2所示。已知:该晶胞底边边长为 ,高为
,高为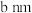 ,l号原子的高为
,l号原子的高为 。
。 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。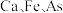 原子的个数之比为
原子的个数之比为___________ ;距2号原子最近的铁有___________ 个。
②该晶体的密度为___________  ,1号原子的坐标为
,1号原子的坐标为___________ 。
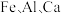 等元素的氧化物及
等元素的氧化物及 )为原料,制备
)为原料,制备 的工艺流程如图所示。
的工艺流程如图所示。
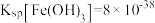 、
、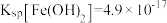 、
、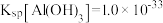 。
。回答下列问题:
(1)“酸溶”硫铁矿烧渣时,为了加快酸溶速率可采取的措施有
(2)料渣1的主要成分有
(3)常温下,已知溶液中
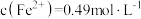 ,要使
,要使 沉淀完全,则“调
沉淀完全,则“调 ”的范围是
”的范围是 认为沉淀完全)。
认为沉淀完全)。(4)加入
 “沉铁”时,发生反应的离子方程式为
“沉铁”时,发生反应的离子方程式为(5)①“煅烧1”的目的是将
 转化为
转化为 ,若“煅烧2”阶段发生反应时
,若“煅烧2”阶段发生反应时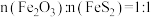 ,则该反应的化学方程式为
,则该反应的化学方程式为②“煅烧2”时温度对
 的纯度有很大影响。已知温度对
的纯度有很大影响。已知温度对 纯度的影响如图1所示,则“煅烧2”时,温度最好控制在
纯度的影响如图1所示,则“煅烧2”时,温度最好控制在 。
。
 )的晶胞如图2所示。已知:该晶胞底边边长为
)的晶胞如图2所示。已知:该晶胞底边边长为 ,高为
,高为 ,l号原子的高为
,l号原子的高为 。
。 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。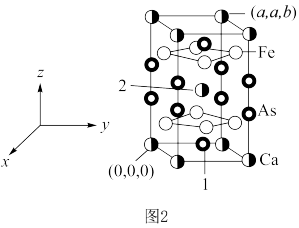
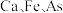 原子的个数之比为
原子的个数之比为②该晶体的密度为
 ,1号原子的坐标为
,1号原子的坐标为
您最近半年使用:0次
解题方法
9 . 硫酸四氨合铜晶体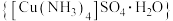 常作杀虫剂、媒染剂。某小组设计实验制备硫酸四氨合铜晶体并测定其纯度。
常作杀虫剂、媒染剂。某小组设计实验制备硫酸四氨合铜晶体并测定其纯度。
实验(一)制备 ,装置如图所示。
,装置如图所示。___________ 。该反应中浓硫酸表现出的性质有___________ 。
(2)持续反应一段时间后C装置中的现象为___________ 。
(3)将A装置中混合物缓慢倒人装有水的烧杯中,再加入过量的 ,充分反应后,过滤。将滤液蒸发浓缩、降温结晶、过滤,得到
,充分反应后,过滤。将滤液蒸发浓缩、降温结晶、过滤,得到 晶体。
晶体。
①不能向A装置的混合物中加入水,其原因是___________ 。
② 的作用是
的作用是___________ 。
实验(二)制备硫酸四氨合铜晶体。
 中蓝色沉淀溶解得到深蓝色的透明溶液,其原因是
中蓝色沉淀溶解得到深蓝色的透明溶液,其原因是___________ (写出离子方程式)。
(5)相对普通过滤,利用图2装置分离晶体,其突出优点有___________ (答一条即可)。
实验(三)测定硫酸四氨合铜晶体纯度。
取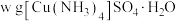 样品溶于蒸馏水配制成
样品溶于蒸馏水配制成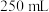 溶液,准确量取
溶液,准确量取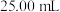 配制溶液,滴加适量的稀硫酸,充分反应。加入过量
配制溶液,滴加适量的稀硫酸,充分反应。加入过量 溶液,滴加3滴淀粉溶液,用
溶液,滴加3滴淀粉溶液,用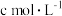
 溶液滴定,边滴边摇动锥形瓶至滴定终点,消耗
溶液滴定,边滴边摇动锥形瓶至滴定终点,消耗 溶液
溶液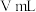 。相关反应:
。相关反应: ,
, ,
,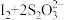
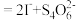 。
。
(6) 产品的纯度为
产品的纯度为___________ 。若①摇动锥形瓶时间过长,空气进入较多;②滴加稀硫酸过多,则上述两种情况可能会导致测得结果___________ (填字母)。(已知: 在酸性条件下不稳定,会发生歧化反应)
在酸性条件下不稳定,会发生歧化反应)
A.①偏高 ②偏低 B.①偏低 ②偏高 C.①偏高 ②偏高 D.①偏低 ②偏低
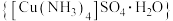 常作杀虫剂、媒染剂。某小组设计实验制备硫酸四氨合铜晶体并测定其纯度。
常作杀虫剂、媒染剂。某小组设计实验制备硫酸四氨合铜晶体并测定其纯度。实验(一)制备
 ,装置如图所示。
,装置如图所示。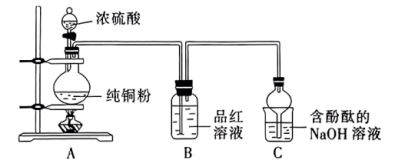
(2)持续反应一段时间后C装置中的现象为
(3)将A装置中混合物缓慢倒人装有水的烧杯中,再加入过量的
 ,充分反应后,过滤。将滤液蒸发浓缩、降温结晶、过滤,得到
,充分反应后,过滤。将滤液蒸发浓缩、降温结晶、过滤,得到 晶体。
晶体。①不能向A装置的混合物中加入水,其原因是
②
 的作用是
的作用是实验(二)制备硫酸四氨合铜晶体。
| 步骤 | 实验操作及主要现象 |
 | 取一定量 晶体溶于蒸馏水得到 晶体溶于蒸馏水得到 溶液 溶液 |
 | 向步骤 溶液中滴加一定量的氨水,产生蓝色沉淀;继续滴加氨水,蓝色沉淀逐渐溶解,最终得到深蓝色的透明溶液 溶液中滴加一定量的氨水,产生蓝色沉淀;继续滴加氨水,蓝色沉淀逐渐溶解,最终得到深蓝色的透明溶液 |
 | 向步骤 所得溶液中滴加 所得溶液中滴加 的乙醇,静置析出深蓝色晶体,用下图装置过滤 的乙醇,静置析出深蓝色晶体,用下图装置过滤 |
 | 取步骤 中晶体,用乙醇与浓氨水的混合液洗涤,再用乙醇与乙醚的混合液淋洗,然后将其在 中晶体,用乙醇与浓氨水的混合液洗涤,再用乙醇与乙醚的混合液淋洗,然后将其在 左右小心烘干,得到 左右小心烘干,得到 |
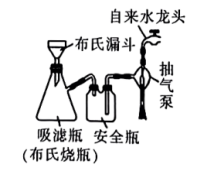
 中蓝色沉淀溶解得到深蓝色的透明溶液,其原因是
中蓝色沉淀溶解得到深蓝色的透明溶液,其原因是(5)相对普通过滤,利用图2装置分离晶体,其突出优点有
实验(三)测定硫酸四氨合铜晶体纯度。
取
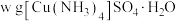 样品溶于蒸馏水配制成
样品溶于蒸馏水配制成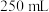 溶液,准确量取
溶液,准确量取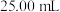 配制溶液,滴加适量的稀硫酸,充分反应。加入过量
配制溶液,滴加适量的稀硫酸,充分反应。加入过量 溶液,滴加3滴淀粉溶液,用
溶液,滴加3滴淀粉溶液,用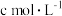
 溶液滴定,边滴边摇动锥形瓶至滴定终点,消耗
溶液滴定,边滴边摇动锥形瓶至滴定终点,消耗 溶液
溶液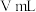 。相关反应:
。相关反应: ,
, ,
,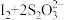
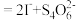 。
。(6)
 产品的纯度为
产品的纯度为 在酸性条件下不稳定,会发生歧化反应)
在酸性条件下不稳定,会发生歧化反应)A.①偏高 ②偏低 B.①偏低 ②偏高 C.①偏高 ②偏高 D.①偏低 ②偏低
您最近半年使用:0次
解题方法
10 . 一种从含银废催化剂[其主要成分为银和铼( ),还含有
),还含有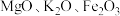 和
和 ]中回收银和铼的工艺流程如图所示。下列说法错误的是
]中回收银和铼的工艺流程如图所示。下列说法错误的是
 ),还含有
),还含有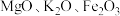 和
和 ]中回收银和铼的工艺流程如图所示。下列说法错误的是
]中回收银和铼的工艺流程如图所示。下列说法错误的是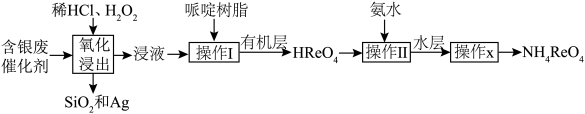
A.“氧化浸出”过程中铼被氧化,该反应中氧化剂与还原剂物质的量之比为 |
B.实验室中完成“操作 ”和“操作 ”和“操作 ”所需要的玻璃仪器主要有烧杯和分液漏斗 ”所需要的玻璃仪器主要有烧杯和分液漏斗 |
| C.“操作x”为结晶过程,该过程不可选用蒸发结晶,应选用降温结晶 |
D.“操作 ”过程中为加快反应速率,可在高温条件下进行 ”过程中为加快反应速率,可在高温条件下进行 |
您最近半年使用:0次



