1 . 钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在_______ 中。
(2)除去碳酸钠固体中碳酸氢钠的方法是______________ 。
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入_______ (填“铁粉”或“铜粉”)。
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:_______________ 。
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于__________ (填“碱性”或“两性”)氧化物。
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在
(2)除去碳酸钠固体中碳酸氢钠的方法是
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于
您最近一年使用:0次
2 . 黑木耳富含蛋白质、铁、具有还原性的维生素C等,每100 g黑木耳含铁量高达185 mg。
I.为了确定黑木耳中含有铁元素,甲同学设计实验方案如下。____________ 。
(2)步骤④检验Fe3+所用试剂是_____________ (填化学式)溶液。
(3)已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓,则滤液A中大量含有的阳离子 的离子符号为____________ 。
II.紫色的KMnO4溶液在酸性条件下具有强氧化性,其还原产物是无色的Mn2+。本实验用KMnO4酸性溶液来测定黑木耳中铁元素的含量,乙同学设计实验方案如下。_______ (填序号)。
a.Na b.Cu c.Fe
(5)步骤⑥的离子方程式为_______________ 。
(6)若乙同学实验操作规范,但测得含铁量远远偏高,其可能的原因是_______________ 。
I.为了确定黑木耳中含有铁元素,甲同学设计实验方案如下。
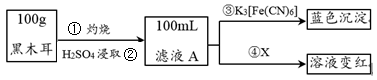
(2)步骤④检验Fe3+所用试剂是
(3)已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓,则滤液A中大量含有的
II.紫色的KMnO4溶液在酸性条件下具有强氧化性,其还原产物是无色的Mn2+。本实验用KMnO4酸性溶液来测定黑木耳中铁元素的含量,乙同学设计实验方案如下。
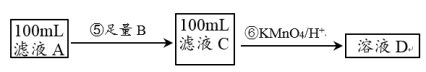
a.Na b.Cu c.Fe
(5)步骤⑥的离子方程式为
(6)若乙同学实验操作规范,但测得含铁量远远偏高,其可能的原因是
您最近一年使用:0次
名校
3 . 下列离子在指定溶液中一定能大量共存的是
A.无色透明的溶液中: 、 、 、 、 、 、 |
B.pH=3的溶液中: 、 、 、 、 、 、 |
C.使酚酞变红的溶液中: 、 、 、 、 、 、 |
D.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
2024-04-25更新
|
506次组卷
|
5卷引用:湖南省娄底市涟源市2023-2024学年高一下学期3月月考化学试题
4 . 下列化学用语不正确的是
A.石膏的化学式为 |
B.中子数为20的氯原子: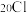 |
C.HClO的结构式: |
D.用电子式表示 的形成过程: 的形成过程: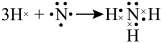 |
您最近一年使用:0次
5 . 按照要求回答问题。
(1) 的电子式为
的电子式为_______ ,写出其用于呼吸面具做供氧剂的化学方程式:_______ 。
(2)实验室用NaOH浓溶液配制0.1 mol·L NaOH溶液500 mL,需量取密度为1.4 g·cm
NaOH溶液500 mL,需量取密度为1.4 g·cm 质量分数为40%的NaOH溶液
质量分数为40%的NaOH溶液_______ mL(保留一位小数),该实验所需的玻璃仪器除玻璃棒、量筒、胶头滴管、烧杯之外,还有_______ 。
(3)非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,若A在常温下为气体单质,将装满气体C的试管倒扣在水槽中,溶液最终充满试管容积的 ,则C→D的化学方程式:
,则C→D的化学方程式:_______ 。 )是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用
)是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用 的反应原理来制备高铁酸钠,若制备1 mol
的反应原理来制备高铁酸钠,若制备1 mol  ,则该反应转移的电子为
,则该反应转移的电子为_______ mol。
(1)
 的电子式为
的电子式为(2)实验室用NaOH浓溶液配制0.1 mol·L
 NaOH溶液500 mL,需量取密度为1.4 g·cm
NaOH溶液500 mL,需量取密度为1.4 g·cm 质量分数为40%的NaOH溶液
质量分数为40%的NaOH溶液(3)非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,若A在常温下为气体单质,将装满气体C的试管倒扣在水槽中,溶液最终充满试管容积的
 ,则C→D的化学方程式:
,则C→D的化学方程式:
 )是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用
)是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用 的反应原理来制备高铁酸钠,若制备1 mol
的反应原理来制备高铁酸钠,若制备1 mol  ,则该反应转移的电子为
,则该反应转移的电子为
您最近一年使用:0次
6 . 氮及其化合物的变化关系如图所示。下列说法不正确的是

| A.路线①②③是工业生产硝酸的主要途径 |
| B.路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径 |
| C.上述所有反应均属于氧化还原反应 |
| D.路线③必须再加入氧化剂才能实现 |
您最近一年使用:0次
2024-04-05更新
|
312次组卷
|
2卷引用:湖南省娄底市涟源市2023-2024学年高一下学期3月月考化学试题
7 . 碱式氧化镍是镍电池的正极活性材料。利用镍渣(主要含N iO,及少量
iO,及少量 、CuO、CaO、BaO、
、CuO、CaO、BaO、 等杂质)制备碱式氧化镍的流程如下:
等杂质)制备碱式氧化镍的流程如下:
 iO,及少量
iO,及少量 、CuO、CaO、BaO、
、CuO、CaO、BaO、 等杂质)制备碱式氧化镍的流程如下:
等杂质)制备碱式氧化镍的流程如下: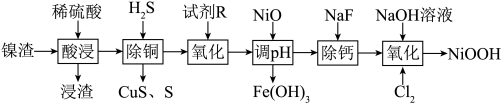
| A.粉碎镍渣可加快“酸浸”速率 |
B.浸渣的成分主要为 、 、 、 、 |
C.最后一步“氧化”工序中,若通入4.48 L  ,则理论上能够制备碱式氧化镍36.8 g ,则理论上能够制备碱式氧化镍36.8 g |
D.“除铜”时发生的氧化还原反应为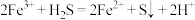 |
您最近一年使用:0次
8 . 以 固体为原料制备纯
固体为原料制备纯 ,其部分实验过程如下:
,其部分实验过程如下:
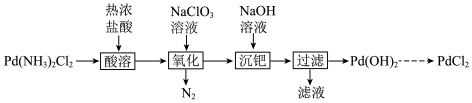
已知:① 具有顺反异构;
具有顺反异构;
②“酸溶”中生成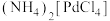 ;
;
③ 有两性,
有两性, ;
;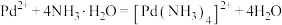
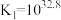 。
。
下列说法不正确的是
 固体为原料制备纯
固体为原料制备纯 ,其部分实验过程如下:
,其部分实验过程如下:
已知:①
 具有顺反异构;
具有顺反异构;②“酸溶”中生成
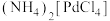 ;
;③
 有两性,
有两性, ;
;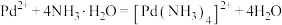
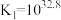 。
。下列说法不正确的是
A. 中的配位体为 中的配位体为 ,Pd的配位数为2 ,Pd的配位数为2 |
B.“氧化”过程中发生反应的离子方程式为: |
C. 的平衡常数 的平衡常数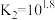 |
D.若氧化不充分,将会导致 的产率降低 的产率降低 |
您最近一年使用:0次
解题方法
9 . 湖湘文化底蕴深厚,湖南又是人杰地灵的好地方。下列有关说法正确的是
A.长沙天心阁古城墙始建于西汉,为砖石结构,砖石为青砖,成分中含有 |
| B.醴陵瓷器是中国国家地理标志,在高温釉烧过程中不涉及化学变化 |
| C.浏阳花炮的历史悠久,烟花其实就是金属单质灼烧时呈现的各种艳丽色彩 |
| D.湖南湘江鲲鹏科技有限公司是研制鲲鹏主板自主服务器的公司,鲲鹏主板的材料中用到铜 |
您最近一年使用:0次
名校
10 . 下列有关叙述正确的是
A.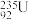 和 和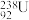 质子数相同,中子数不同,互为同素异形体 质子数相同,中子数不同,互为同素异形体 |
B.若某气体可使品红溶液褪色,则该气体一定为 |
| C.已知酸性:HI>HBr>HCl>HF,所以元素非金属性:I>Br>Cl>F |
D.同温同压下,等体积的 和 和 两种气体含有相同的分子数 两种气体含有相同的分子数 |
您最近一年使用:0次
2024-03-26更新
|
226次组卷
|
4卷引用:湖南省娄底市涟源市2023-2024学年高一下学期3月月考化学试题



