名校
1 . 下列离子方程式书写正确的是
A.铅酸蓄电池放电时的负极反应: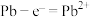 |
B.药物碘化钾片和加碘盐不可同时服用: |
C.向 溶液中加入足量NaOH溶液: 溶液中加入足量NaOH溶液: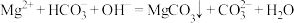 |
D.向食盐的氨水溶液中通入足量 气体后生成沉淀: 气体后生成沉淀: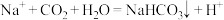 |
您最近一年使用:0次
名校
2 . 氨气在一定条件下催化还原含 的尾气,反应为
的尾气,反应为 ,下列说法错误的是
,下列说法错误的是
 的尾气,反应为
的尾气,反应为 ,下列说法错误的是
,下列说法错误的是| A.氮氧化物的排放可形成酸雨 |
| B.氨气分子的键角小于甲烷的键角 |
C.该反应的氧化产物和还原产物的质量比为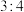 |
D.反应 能说明 能说明 不是酸性氧化物 不是酸性氧化物 |
您最近一年使用:0次
名校
解题方法
3 . PHB是一种可降解塑料,其结构简式为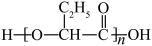 ,下列说法正确的是
,下列说法正确的是
| A.PHB属于电解质 |
| B.通过加聚反应可以制得PHB |
C.合成PHB的单体是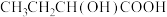 |
| D.1mol PHB最多与n mol氢气发生加成反应 |
您最近一年使用:0次
名校
解题方法
4 . 下列有关化学用语的说法正确的是
| A.基态磷原子价层电子的空间运动状态有4种 |
B.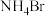 的电子式: 的电子式: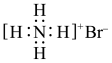 |
C. 的水解方程式: 的水解方程式: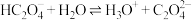 |
D.二氯甲烷的结构式有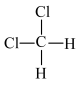 和 和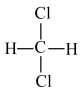 两种 两种 |
您最近一年使用:0次
2024-05-23更新
|
73次组卷
|
2卷引用:甘肃省白银市靖远县2024届高三下学期全真模拟化学试题
名校
解题方法
5 . 钴广泛应用于机械制造、电子电器、航空航天、电池制造等行业,是国家重要的战略资源。用含钴废料(主要成分为 ,含少量
,含少量 、
、 、CaO、MgO、
、CaO、MgO、 等)制备草酸钴晶体(
等)制备草酸钴晶体( )的工艺流程如图所示,试回答下列问题:
)的工艺流程如图所示,试回答下列问题:
① 具有强氧化性。
具有强氧化性。
② ,
, 。
。
(1)为提高含钴废料的浸出效率,可采取的措施是___________ (任写一条)。
(2) 在水溶液中的电离方程式为
在水溶液中的电离方程式为___________ ;浸出渣的主要成分为___________ (填化学式)。
(3)向“浸出液”中加入适量的 时,
时, 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(4)0.1 的
的 溶液中:
溶液中: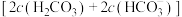
___________ (填“>”或“<”或“=”)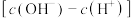 。
。
(5)①“除钙镁”后,滤液中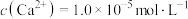 时,
时,
___________  。
。
②若“调pH”时溶液的pH偏低,将会导致 、
、 沉淀不完全,其原因是
沉淀不完全,其原因是___________ 。
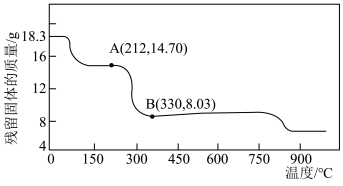
(6)将 在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知:
在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知: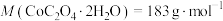 ]
] ,此过程中发生反应的化学方程式为
,此过程中发生反应的化学方程式为___________ 。
 ,含少量
,含少量 、
、 、CaO、MgO、
、CaO、MgO、 等)制备草酸钴晶体(
等)制备草酸钴晶体( )的工艺流程如图所示,试回答下列问题:
)的工艺流程如图所示,试回答下列问题: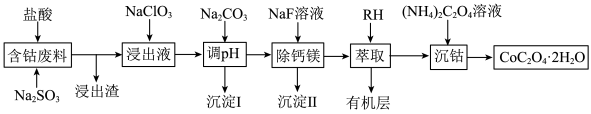
①
 具有强氧化性。
具有强氧化性。②
 ,
, 。
。(1)为提高含钴废料的浸出效率,可采取的措施是
(2)
 在水溶液中的电离方程式为
在水溶液中的电离方程式为(3)向“浸出液”中加入适量的
 时,
时, 发生反应的离子方程式为
发生反应的离子方程式为(4)0.1
 的
的 溶液中:
溶液中: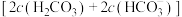
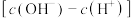 。
。(5)①“除钙镁”后,滤液中
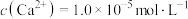 时,
时,
 。
。②若“调pH”时溶液的pH偏低,将会导致
 、
、 沉淀不完全,其原因是
沉淀不完全,其原因是(6)将
 在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知:
在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知: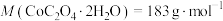 ]
]
 ,此过程中发生反应的化学方程式为
,此过程中发生反应的化学方程式为
您最近一年使用:0次
2024-05-22更新
|
70次组卷
|
3卷引用:甘肃省白银市靖远县2024届高三下学期全真模拟化学试题
名校
解题方法
6 . 常温下,下列各组离子在指定溶液中一定能大量共存的是
A.澄清透明溶液中: 、 、 、 、 、 、 |
B.加入铝能放出氢气的溶液中: 、 、 、 、 、 、 |
C.滴加淀粉-KI溶液显蓝色的溶液中: 、 、 、 、 、 、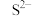 |
D.水电离出的氢离子浓度为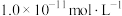 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
2024-05-22更新
|
90次组卷
|
2卷引用:甘肃省白银市靖远县2024届高三下学期全真模拟化学试题
名校
7 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.7.8g  中所含的阴离子总数大于0.1 中所含的阴离子总数大于0.1 |
B.标准状况下,2.24L HF中含有的原子数目为0.2 |
C.标准状况下,11.2L  溶于水,溶液中 溶于水,溶液中 、 、 、 、 和HClO的微粒数之和为 和HClO的微粒数之和为 |
D.0.1mol  与足量酸性 与足量酸性 溶液充分反应,转移的电子数为0.2 溶液充分反应,转移的电子数为0.2 |
您最近一年使用:0次
2024-05-21更新
|
78次组卷
|
2卷引用:甘肃省白银市靖远县2024届高三下学期全真模拟化学试题
名校
8 . 在可见光的照射下将 催化还原为
催化还原为 的反应历程如图所示(
的反应历程如图所示(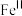 代表铁显+2价)。下列叙述错误的是
代表铁显+2价)。下列叙述错误的是
 催化还原为
催化还原为 的反应历程如图所示(
的反应历程如图所示(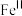 代表铁显+2价)。下列叙述错误的是
代表铁显+2价)。下列叙述错误的是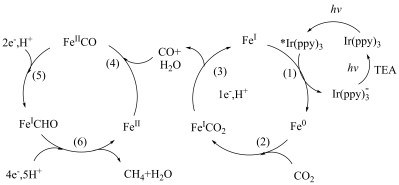
A.一段时间后, 数目基本保持不变 数目基本保持不变 | B.在上述循环中,铁元素化合价发生了变化 |
C.上述循环中只断裂和形成 键 键 | D. 催化还原过程中,CO是中间产物 催化还原过程中,CO是中间产物 |
您最近一年使用:0次
2024-05-19更新
|
84次组卷
|
3卷引用:甘肃省张掖市某校2023-2024学年高三下学期模拟考试化学试题
解题方法
9 . 甘肃矿产资源丰富,金属冶炼在国民经济发展中有着重要的作用。锰酸锂鲤离子蓄电池是第二代锂离子动力电池,工业上用某软锰矿(主要成分为 ,还含有少量铁、铝及硅的氧化物)为原料制备锰酸锂
,还含有少量铁、铝及硅的氧化物)为原料制备锰酸锂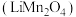 ,流程如图所示:
,流程如图所示:
(1)基态 原子的价电子排布式为
原子的价电子排布式为_______ , 元素位于元素周期表中的
元素位于元素周期表中的_______ 区。
(2)“酸浸”时,为了提升各物质的浸出速率,除了适当升高温度外,还可以采取的措施是_______ (写一条即可)。
(3)“还原”步骤得到的溶液中阳离子主要是 ,生成
,生成 的离子方程式为
的离子方程式为_______ ;滤渣1的主要成分为_______ 。
(4)已知某离子浓度[用 表示]形成沉淀与溶液
表示]形成沉淀与溶液 的关系如下图所示:
的关系如下图所示: 调节
调节 的范围是
的范围是_______ 。
(5)“沉锰”得到的是 和
和 滤饼,所得滤液回收可用于
滤饼,所得滤液回收可用于_______ 。
(6)“锂化”是将 和
和 按
按 的物质的量比配料,球磨
的物质的量比配料,球磨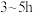 ,然后升温至
,然后升温至 ,保温
,保温 ,自然冷却至室温得产品,写出化学反应方程式:
,自然冷却至室温得产品,写出化学反应方程式:_______ 。
 ,还含有少量铁、铝及硅的氧化物)为原料制备锰酸锂
,还含有少量铁、铝及硅的氧化物)为原料制备锰酸锂 ,流程如图所示:
,流程如图所示:
(1)基态
 原子的价电子排布式为
原子的价电子排布式为 元素位于元素周期表中的
元素位于元素周期表中的(2)“酸浸”时,为了提升各物质的浸出速率,除了适当升高温度外,还可以采取的措施是
(3)“还原”步骤得到的溶液中阳离子主要是
 ,生成
,生成 的离子方程式为
的离子方程式为(4)已知某离子浓度[用
 表示]形成沉淀与溶液
表示]形成沉淀与溶液 的关系如下图所示:
的关系如下图所示: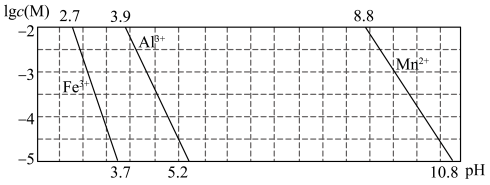
 调节
调节 的范围是
的范围是(5)“沉锰”得到的是
 和
和 滤饼,所得滤液回收可用于
滤饼,所得滤液回收可用于(6)“锂化”是将
 和
和 按
按 的物质的量比配料,球磨
的物质的量比配料,球磨 ,然后升温至
,然后升温至 ,保温
,保温 ,自然冷却至室温得产品,写出化学反应方程式:
,自然冷却至室温得产品,写出化学反应方程式:
您最近一年使用:0次
10 .  催化还原氮氧化物是目前应用最广泛的烟气脱硝技术。用活化的
催化还原氮氧化物是目前应用最广泛的烟气脱硝技术。用活化的 作催化剂,
作催化剂, 将
将 还原成
还原成 的一种反应历程如图所示。下列说法错误的是
的一种反应历程如图所示。下列说法错误的是
 催化还原氮氧化物是目前应用最广泛的烟气脱硝技术。用活化的
催化还原氮氧化物是目前应用最广泛的烟气脱硝技术。用活化的 作催化剂,
作催化剂, 将
将 还原成
还原成 的一种反应历程如图所示。下列说法错误的是
的一种反应历程如图所示。下列说法错误的是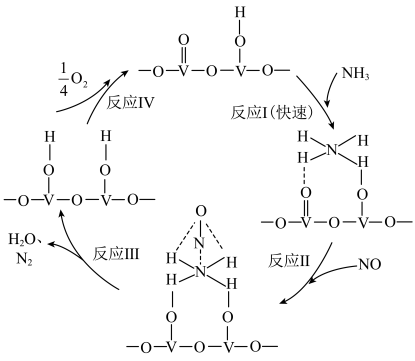
| A.该历程中能垒最高的是反应I |
| B.该历程中,V元素被氧化的只有反应Ⅳ |
C.该催化反应的总反应式为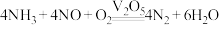 |
| D.整个历程中涉及极性键和非极性键的断裂和形成 |
您最近一年使用:0次



