1 . 用废铁屑(含少量杂质FeS)为原料制备摩尔盐 。实验装置如下(加热装置已略去):
。实验装置如下(加热装置已略去):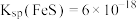 ,
,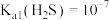 ,
,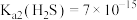 。
。
(1)A装置中的反应控制在50~60℃间进行的原因是_______ ;三颈烧瓶中液体试剂添加顺序为_______ 。(选填序号)
a.先滴加氨水,然后滴加稀硫酸,再水浴加热,反应一段时间后冷却
b.先滴加稀硫酸,然后水浴加热,再滴加氨水,反应一段时间后冷却
c.先滴加稀硫酸,然后水浴加热,反应一段时间后冷却,再滴加氨水
(2)反应一段时间后,C瓶中酸性 溶液颜色变浅,底部有淡黄色固体生成,发生反应的离子方程式为
溶液颜色变浅,底部有淡黄色固体生成,发生反应的离子方程式为_______ 。
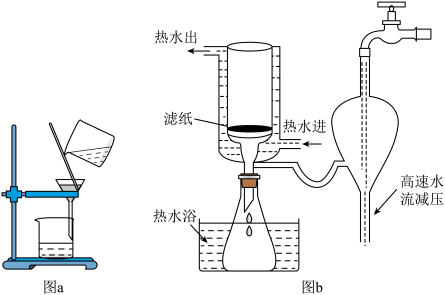
(3)A中反应完成后过滤采用如下图b装置,相对于图a装置而言其优点有_______ (写两点)。 溶液测定制得的
溶液测定制得的 中的n值。请补充完整实验方案:准确称取
中的n值。请补充完整实验方案:准确称取 样品,加入足量稀硫酸溶解后配成250.00mL溶液。使用移液管准确移取25.00mL于锥形瓶中,
样品,加入足量稀硫酸溶解后配成250.00mL溶液。使用移液管准确移取25.00mL于锥形瓶中,_______ 。[已知:二苯胺磺酸钠指示液在还原性氛围下为无色,氧化性氛围下为紫红色。](可使用的试剂和仪器: 溶液,二苯胺磺酸钠指示液,酸式滴定管,碱式滴定管)
溶液,二苯胺磺酸钠指示液,酸式滴定管,碱式滴定管)
将测定的n值与实际值进对比,测定值偏大。下列说法正确的是_______ 。(选填序号)
a.测定值偏大可能由于晶体干燥时失去了部分结晶水
b.测定值偏大可能由于晶体中含有部分 杂质
杂质
c.测定值偏大可能由于滴入指示剂过量
d.若通过 溶液测定n值,应滴定至向上层清液中继续滴加数滴
溶液测定n值,应滴定至向上层清液中继续滴加数滴 溶液后无明显现象,记录
溶液后无明显现象,记录 溶液的用量,测定n值
溶液的用量,测定n值
e.若通过 溶液测定n值,应向其中加入过量
溶液测定n值,应向其中加入过量 溶液,将所得固体过滤洗涤烘干至恒重,记录沉淀的质量,测定n值
溶液,将所得固体过滤洗涤烘干至恒重,记录沉淀的质量,测定n值
 。实验装置如下(加热装置已略去):
。实验装置如下(加热装置已略去):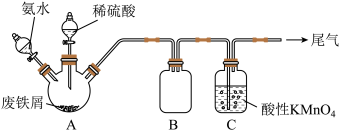
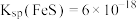 ,
,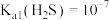 ,
,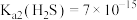 。
。(1)A装置中的反应控制在50~60℃间进行的原因是
a.先滴加氨水,然后滴加稀硫酸,再水浴加热,反应一段时间后冷却
b.先滴加稀硫酸,然后水浴加热,再滴加氨水,反应一段时间后冷却
c.先滴加稀硫酸,然后水浴加热,反应一段时间后冷却,再滴加氨水
(2)反应一段时间后,C瓶中酸性
 溶液颜色变浅,底部有淡黄色固体生成,发生反应的离子方程式为
溶液颜色变浅,底部有淡黄色固体生成,发生反应的离子方程式为(3)A中反应完成后过滤采用如下图b装置,相对于图a装置而言其优点有
 溶液测定制得的
溶液测定制得的 中的n值。请补充完整实验方案:准确称取
中的n值。请补充完整实验方案:准确称取 样品,加入足量稀硫酸溶解后配成250.00mL溶液。使用移液管准确移取25.00mL于锥形瓶中,
样品,加入足量稀硫酸溶解后配成250.00mL溶液。使用移液管准确移取25.00mL于锥形瓶中, 溶液,二苯胺磺酸钠指示液,酸式滴定管,碱式滴定管)
溶液,二苯胺磺酸钠指示液,酸式滴定管,碱式滴定管)将测定的n值与实际值进对比,测定值偏大。下列说法正确的是
a.测定值偏大可能由于晶体干燥时失去了部分结晶水
b.测定值偏大可能由于晶体中含有部分
 杂质
杂质c.测定值偏大可能由于滴入指示剂过量
d.若通过
 溶液测定n值,应滴定至向上层清液中继续滴加数滴
溶液测定n值,应滴定至向上层清液中继续滴加数滴 溶液后无明显现象,记录
溶液后无明显现象,记录 溶液的用量,测定n值
溶液的用量,测定n值e.若通过
 溶液测定n值,应向其中加入过量
溶液测定n值,应向其中加入过量 溶液,将所得固体过滤洗涤烘干至恒重,记录沉淀的质量,测定n值
溶液,将所得固体过滤洗涤烘干至恒重,记录沉淀的质量,测定n值
您最近一年使用:0次
2 . 氯碱工业中常用氨气检验氯气管道是否泄漏,原理为:3Cl2+8NH3=6NH4Cl+N2。下列说法正确的是
| A.该反应为复分解反应 | B.反应中氮元素全部被氧化 |
| C.转移2.4mol电子,生成0.1molN2 | D.若有白烟产生,说明Cl2泄漏 |
您最近一年使用:0次
3 . 环境保护是化学的重要任务,请完成下列问题。
(1)采用“联合脱硫脱氮技术”处理烟气(含 、
、 、NO)可获得含
、NO)可获得含 、
、 、
、 的副产品,工业流程如图1所示。
的副产品,工业流程如图1所示。 采用“气-液逆流”接触吸收法(如图2),其优点是
采用“气-液逆流”接触吸收法(如图2),其优点是___________ 。
②反应釜 中
中 转化为
转化为 反应的化学方程式为
反应的化学方程式为___________ 。
(2)烟气(主要污染物 、
、 )对人类生活环境造成很大的污染。工业上采取氧化、还原等方法将之除去,以达到净化目的。
)对人类生活环境造成很大的污染。工业上采取氧化、还原等方法将之除去,以达到净化目的。
①烟气经 预处理后用碱液吸收,可减少其中
预处理后用碱液吸收,可减少其中 、
、 的含量。已知NO可被
的含量。已知NO可被 氧化为
氧化为 ,
, 用NaOH溶液吸收生成两种盐,其中一种盐是NaNO3 ,另一种盐的化学式为
用NaOH溶液吸收生成两种盐,其中一种盐是NaNO3 ,另一种盐的化学式为___________ 。
②尿素 在高温条件下与NO反应转化成三种无毒气体,该反应的化学方程式为
在高温条件下与NO反应转化成三种无毒气体,该反应的化学方程式为___________ 。
(3)工业上氮的氧化物通常是用碱性溶液吸收。
①用 溶液吸收硝酸工业尾气中的
溶液吸收硝酸工业尾气中的 ,生成等物质的量的两种钠盐(其中一种为
,生成等物质的量的两种钠盐(其中一种为 )及一种气体,反应的离子方程式为
)及一种气体,反应的离子方程式为___________ 。
②NaOH溶液浓度越大黏稠度越高,用不同浓度的NaOH溶液吸收 (混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如图3所示,曲线
(混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如图3所示,曲线 表示NO的物质的量
表示NO的物质的量___________ (填“大于”“小于”或“等于”) 物质的量。当NaOH溶液浓度高于
物质的量。当NaOH溶液浓度高于 后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是
后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是___________ 。
(1)采用“联合脱硫脱氮技术”处理烟气(含
 、
、 、NO)可获得含
、NO)可获得含 、
、 、
、 的副产品,工业流程如图1所示。
的副产品,工业流程如图1所示。

 采用“气-液逆流”接触吸收法(如图2),其优点是
采用“气-液逆流”接触吸收法(如图2),其优点是②反应釜
 中
中 转化为
转化为 反应的化学方程式为
反应的化学方程式为(2)烟气(主要污染物
 、
、 )对人类生活环境造成很大的污染。工业上采取氧化、还原等方法将之除去,以达到净化目的。
)对人类生活环境造成很大的污染。工业上采取氧化、还原等方法将之除去,以达到净化目的。①烟气经
 预处理后用碱液吸收,可减少其中
预处理后用碱液吸收,可减少其中 、
、 的含量。已知NO可被
的含量。已知NO可被 氧化为
氧化为 ,
, 用NaOH溶液吸收生成两种盐,其中一种盐是NaNO3 ,另一种盐的化学式为
用NaOH溶液吸收生成两种盐,其中一种盐是NaNO3 ,另一种盐的化学式为②尿素
 在高温条件下与NO反应转化成三种无毒气体,该反应的化学方程式为
在高温条件下与NO反应转化成三种无毒气体,该反应的化学方程式为(3)工业上氮的氧化物通常是用碱性溶液吸收。
①用
 溶液吸收硝酸工业尾气中的
溶液吸收硝酸工业尾气中的 ,生成等物质的量的两种钠盐(其中一种为
,生成等物质的量的两种钠盐(其中一种为 )及一种气体,反应的离子方程式为
)及一种气体,反应的离子方程式为②NaOH溶液浓度越大黏稠度越高,用不同浓度的NaOH溶液吸收
 (混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如图3所示,曲线
(混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如图3所示,曲线 表示NO的物质的量
表示NO的物质的量 物质的量。当NaOH溶液浓度高于
物质的量。当NaOH溶液浓度高于 后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是
后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是
您最近一年使用:0次
4 . 氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题: 的说法中,不正确的是___________(填字母)。
的说法中,不正确的是___________(填字母)。
(2)氨气在氧化炉中发生反应的化学方程式为___________ 。
(3)氮的氧化物(NOx)是常见的大气污染物之一,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。当物质NO与NO2的物质的量之比为1:1时,与足量氨气能在催化剂作用下发生反应,生成两种无污染的物质,该反应的化学方程式为___________ 。
(4)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的污染,可用以下两种方法处理:
①可用ClO2将氮氧化物转化成 。向含ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为
。向含ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为___________ 。
②氨转化法。已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为___________ 。
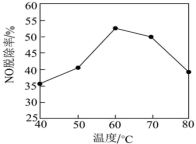
③还有人研究:在不同温度下经酸化处理的Ca(ClO)2溶液对NO脱除率的影响,结果如图所示。在60~80℃ 时,NO 脱除率下降的原因是___________ 。
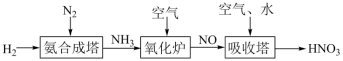
 的说法中,不正确的是___________(填字母)。
的说法中,不正确的是___________(填字母)。A.工业合成 需要在高温、高压、催化剂下进行 需要在高温、高压、催化剂下进行 |
B. 可用来生产碳铵和尿素等化肥 可用来生产碳铵和尿素等化肥 |
C. 可用浓硫酸或无水氯化钙干燥 可用浓硫酸或无水氯化钙干燥 |
D. 受热易分解,须置于冷暗处保存 受热易分解,须置于冷暗处保存 |
(3)氮的氧化物(NOx)是常见的大气污染物之一,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。当物质NO与NO2的物质的量之比为1:1时,与足量氨气能在催化剂作用下发生反应,生成两种无污染的物质,该反应的化学方程式为
(4)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的污染,可用以下两种方法处理:
①可用ClO2将氮氧化物转化成
 。向含ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为
。向含ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为②氨转化法。已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为
③还有人研究:在不同温度下经酸化处理的Ca(ClO)2溶液对NO脱除率的影响,结果如图所示。在60~80℃ 时,NO 脱除率下降的原因是
您最近一年使用:0次
5 . 我国科学家利用过渡金属氮化物(TMNS)作催化剂,在常温下实现氨气的合成,其反应机理如图所示。

| A.用15N2进行合成反应,产物中只有15NH3 |
| B.TMNS表面上的N原子被氧化为氨气 |
| C.TMNS表面上氨脱附产生的空位有利于吸附N2 |
| D.TMNS不参与氨气的合成反应 |
您最近一年使用:0次
6 . 室温下进行下列实验,根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀 | 气体X一定具有强氧化性 |
| B | 向Na2CO3溶液中加入盐酸,将产生的气体直接通入硅酸钠溶液中,产生白色胶状沉淀硅酸 | 酸性:盐酸>碳酸>硅酸 |
| C | 某溶液中加入硝酸酸化的Ba(NO3)2溶液,无现象,再滴加AgNO3溶液,有白色沉淀生成 | 溶液中一定含有Cl- |
| D | 向5mL 0.1mol/L FeCl3溶液中滴加1mL 0.1mol/L KI溶液,再滴加几滴KSCN溶液,观察溶液颜色变化 | FeCl3和KI反应为可逆反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 用软锰矿( ,含
,含 、
、 杂质)和方铅矿(PbS含少量FeS)为原料制备电极材料
杂质)和方铅矿(PbS含少量FeS)为原料制备电极材料 的工艺流程如下:
的工艺流程如下: ,
,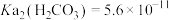 ,
,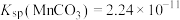
有关离子沉淀时的pH:
回答下列问题:
(1)“滤渣1”除了S、 外,还有
外,还有___________ (填化学式)。
(2)“试剂a”可以选用___________ (填标号),“除杂”应调pH范围是___________ 。
A.NaClO B. C.
C. D.NaOH
D.NaOH
(3)“沉锰”时发生反应的离子方程式为___________ 。
(4)“沉锰”后上层清液中
___________ 。
(5)“焙烧”时发生反应的化学方程式为___________ 。
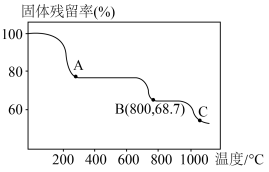
(6)碳酸锰在空气中加热,固体残留率随温度变化如图。碳酸锰在300℃时已完全脱碳,则B点对应的物质的化学式为___________ 。
 ,含
,含 、
、 杂质)和方铅矿(PbS含少量FeS)为原料制备电极材料
杂质)和方铅矿(PbS含少量FeS)为原料制备电极材料 的工艺流程如下:
的工艺流程如下: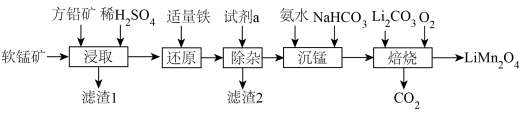
 ,
,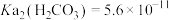 ,
,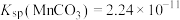
有关离子沉淀时的pH:
 |  |  |  | |
| 开始沉淀时 | 8.3 | 7.6 | 2.7 | 3.0 |
| 沉淀完全时 | 9.8 | 9.6 | 3.7 | 4.7 |
(1)“滤渣1”除了S、
 外,还有
外,还有(2)“试剂a”可以选用
A.NaClO B.
 C.
C. D.NaOH
D.NaOH(3)“沉锰”时发生反应的离子方程式为
(4)“沉锰”后上层清液中

(5)“焙烧”时发生反应的化学方程式为
(6)碳酸锰在空气中加热,固体残留率随温度变化如图。碳酸锰在300℃时已完全脱碳,则B点对应的物质的化学式为
您最近一年使用:0次
解题方法
8 . 下列反应的离子方程式正确的是
A.向硫化钠溶液中通入足量二氧化硫: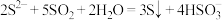 |
B.向 溶液中加入足量烧碱溶液: 溶液中加入足量烧碱溶液: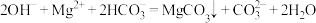 |
C.向次氯酸钙溶液中通入过量二氧化碳: |
D.向 溶液中通入少量 溶液中通入少量 : :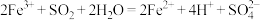 |
您最近一年使用:0次
7日内更新
|
153次组卷
|
2卷引用:江苏省部分学校2024届高三下学期高考模拟化学试题
9 . 化学与生产生活密切相关,下列物质应用中涉及氧化还原反应的是
A.利用葡萄糖酸- -内酯使豆浆凝固 -内酯使豆浆凝固 | B.使用含氟牙膏预防龋齿 |
| C.将植物油氢化以便于运输和储存 | D.利用明矾溶液清除铜镜表面的铜锈 |
您最近一年使用:0次
7日内更新
|
88次组卷
|
2卷引用:江苏省部分学校2024届高三下学期高考模拟化学试题
10 . 元素周期表中VIIA族元素及其化合物应用广泛。氢氟酸可用作雕刻玻璃; 可溶于苯、
可溶于苯、 等有机溶剂,极易水解;加碘盐中主要添加的是
等有机溶剂,极易水解;加碘盐中主要添加的是 ;卤素互化物(如ICl、
;卤素互化物(如ICl、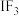 )具有强氧化性;卤化银具有感光性。下列化学反应表示正确的是
)具有强氧化性;卤化银具有感光性。下列化学反应表示正确的是
 可溶于苯、
可溶于苯、 等有机溶剂,极易水解;加碘盐中主要添加的是
等有机溶剂,极易水解;加碘盐中主要添加的是 ;卤素互化物(如ICl、
;卤素互化物(如ICl、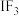 )具有强氧化性;卤化银具有感光性。下列化学反应表示正确的是
)具有强氧化性;卤化银具有感光性。下列化学反应表示正确的是A. 溶于水: 溶于水: |
B.ICl溶于NaOH溶液: |
C. 水解: 水解: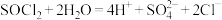 |
D. 用 用 溶液吸收: 溶液吸收: |
您最近一年使用:0次



