名校
解题方法
1 . 某小组按如下步骤探究二氧化硫与铜单质、Cu2+的反应:
ⅰ.按图示连接好装置。
ⅲ.关闭活塞b,打开活塞a.光亮的紫红色铜片很快变暗,并有黑色的Cu2S生成,同时溶液变为棕色,此时溶液中的铜元素以[CuCl3]2-(棕黄色)的形式存在。
ⅳ.静置后,取上层棕色的清液于试管中,加入一定量蒸馏水稀释,溶液中有白色沉淀CuCl析出。
(1)装置A中发生反应的化学方程式为___________ ,该反应中硫酸体现出的化学性质为___________ ;装置C的作用是___________ ,试剂m可选择___________ (填标号)。
a.饱和NaCl溶液 b.浓硫酸 c.NaOH浓溶液
(2)步骤ⅲ中,SO2在盐酸中与Cu反应的离子方程式为___________ ;步骤ⅳ中发生反应的离子方程式为[CuCl3]2-⇌CuCl↓+2Cl-,下列有关该反应的说法正确的是___________ (填标号)。
A.该反应中有电子的转移
B.反应经过足够长的时间后,[CuCl3]2-中的Cu元素能全部沉淀
C.溶液中,[CuCl3]2-和Cl-能同时存在
D.其他条件不变,当溶液的颜色不再改变时,表明该反应在该条件下达到最大限度
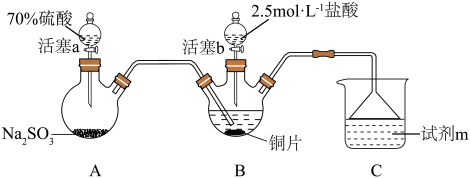
(3)在通风橱中利用如下装置进一步探究SO2与Cu2+的反应,盐桥(内有琼脂和饱和氯化钾溶液)用于连接两电极的电解质溶液。实验②中,闭合K后,C2电极上发生的电极反应为___________ ;不考虑其他副反应及Cu2+进入盐桥,实验②中,电路中转移0.02mole-时,左侧烧杯溶液中Cu2+的质量减少___________ g。
ⅰ.按图示连接好装置。
ⅲ.关闭活塞b,打开活塞a.光亮的紫红色铜片很快变暗,并有黑色的Cu2S生成,同时溶液变为棕色,此时溶液中的铜元素以[CuCl3]2-(棕黄色)的形式存在。
ⅳ.静置后,取上层棕色的清液于试管中,加入一定量蒸馏水稀释,溶液中有白色沉淀CuCl析出。
(1)装置A中发生反应的化学方程式为
a.饱和NaCl溶液 b.浓硫酸 c.NaOH浓溶液
(2)步骤ⅲ中,SO2在盐酸中与Cu反应的离子方程式为
A.该反应中有电子的转移
B.反应经过足够长的时间后,[CuCl3]2-中的Cu元素能全部沉淀
C.溶液中,[CuCl3]2-和Cl-能同时存在
D.其他条件不变,当溶液的颜色不再改变时,表明该反应在该条件下达到最大限度
(3)在通风橱中利用如下装置进一步探究SO2与Cu2+的反应,盐桥(内有琼脂和饱和氯化钾溶液)用于连接两电极的电解质溶液。实验②中,闭合K后,C2电极上发生的电极反应为
| 实验装置图 |
| ||
| 序号 | 试剂X | 实验现象 | |
| 电流计 | C1附近溶液 | ||
| ① | 0.1mol·L-1CuSO4溶液 | 指针几乎不偏转 | 无明显现象 |
| ② | 0.1mol·L-1NaCl和0.1mol·L-1CuSO4的混合溶液(足量) | 指针明显偏转 | 溶液变棕黄色 |
您最近半年使用:0次
解题方法
2 . 下列关于元素及其化合物的性质说法错误的是
| A.饱和氯化铁溶液可制备氢氧化铁胶体 |
| B.普通玻璃由纯碱、石灰石和石英砂制成,其熔点很高 |
| C.镁在空气中燃烧可生成氧化镁和氮化镁 |
| D.铁、铜与足量的单质硫反应均生成其低价硫化物 |
您最近半年使用:0次
3 . 下列离子方程式或电极反应式书写不正确的是
A.CaS与浓硝酸反应: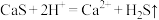 |
B.用硫化亚铁除去废水中的汞离子: |
C.泡沫灭火器的反应原理是: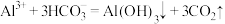 |
D. 溶液与过量 溶液与过量 反应: 反应: |
您最近半年使用:0次
名校
解题方法
4 . 亚硝酸钙 可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应
可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应 利用如下装置制备亚硝酸钙(加热及夹持装置略)。
利用如下装置制备亚硝酸钙(加热及夹持装置略)。 溶液能将NO氧化为
溶液能将NO氧化为 。
。
回答下列问题:
(1)检查装置气密性,加入相应的试剂。先通 ,其目的是
,其目的是________ 。通 后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开
后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开 ,使稀硝酸滴入三颈烧瓶中;(iv)关闭
,使稀硝酸滴入三颈烧瓶中;(iv)关闭 ,打开
,打开 ,通入
,通入 。操作(ii)是
。操作(ii)是________ 。
(2)仪器a的名称为________ ,装置D中盛装的试剂是________ (填名称),装置E的作用是________ 。
(3)制备的产品 样品中含有杂质
样品中含有杂质 ,通过下列方法可测定产品的纯度:称量mg样品溶于水,加
,通过下列方法可测定产品的纯度:称量mg样品溶于水,加 固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作:
固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作: ;“还原
;“还原 ”时加入
”时加入 的
的 标准液,“滴定剩余
标准液,“滴定剩余 ”时消耗
”时消耗 的
的 标准溶液VmL。“滴定剩余
标准溶液VmL。“滴定剩余 ”过程中发生反应的离子方程式为
”过程中发生反应的离子方程式为________ ,样品中 的纯度为
的纯度为________ (用含m、V的式子表示)。
 可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应
可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应 利用如下装置制备亚硝酸钙(加热及夹持装置略)。
利用如下装置制备亚硝酸钙(加热及夹持装置略)。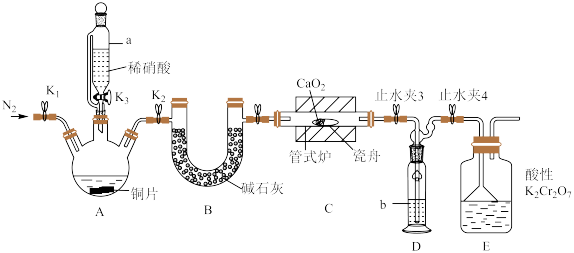
 溶液能将NO氧化为
溶液能将NO氧化为 。
。回答下列问题:
(1)检查装置气密性,加入相应的试剂。先通
 ,其目的是
,其目的是 后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开
后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开 ,使稀硝酸滴入三颈烧瓶中;(iv)关闭
,使稀硝酸滴入三颈烧瓶中;(iv)关闭 ,打开
,打开 ,通入
,通入 。操作(ii)是
。操作(ii)是(2)仪器a的名称为
(3)制备的产品
 样品中含有杂质
样品中含有杂质 ,通过下列方法可测定产品的纯度:称量mg样品溶于水,加
,通过下列方法可测定产品的纯度:称量mg样品溶于水,加 固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作:
固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作: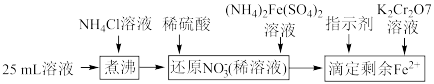
 ;“还原
;“还原 ”时加入
”时加入 的
的 标准液,“滴定剩余
标准液,“滴定剩余 ”时消耗
”时消耗 的
的 标准溶液VmL。“滴定剩余
标准溶液VmL。“滴定剩余 ”过程中发生反应的离子方程式为
”过程中发生反应的离子方程式为 的纯度为
的纯度为
您最近半年使用:0次
今日更新
|
7次组卷
|
2卷引用:2024届青海省西宁市大通县高三下学期三模理科综合试题-高中化学
解题方法
5 . 火法炼铜过程中产生的副产品白烟尘常含有ZnO、 、CuO、CdO、
、CuO、CdO、 、PbO等固体物质,白烟尘综合利用可提高资源利用率,保护环境,其工艺流程如图所示。
、PbO等固体物质,白烟尘综合利用可提高资源利用率,保护环境,其工艺流程如图所示。
①常温下, 的溶解度是
的溶解度是 ,
, 的溶解度是1g。
的溶解度是1g。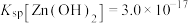 ,
, 。
。
② 易溶于盐酸,生成
易溶于盐酸,生成 :
: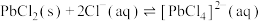 。
。
③胶体对 、
、 有吸附作用。
有吸附作用。
回答下列问题:
(1)酸浸过程得到的浸出液中,砷元素主要以 的形式存在,
的形式存在, 中As的化合价为
中As的化合价为___________ 。
(2)用硫酸、混酸(硫酸与盐酸)体系分别对白烟尘进行直接浸出,实验结果显示混酸体系可以进一步提高As、Cd的浸出率,但会导致铅的溶解,铅溶解的原因是___________ 。
(3)表1、表2是在其他条件一定时,铁铜摩尔置换比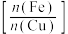 、温度对铜的置换率和品位(固体产物中所含某种金属或有用成分的多少)的影响。
、温度对铜的置换率和品位(固体产物中所含某种金属或有用成分的多少)的影响。
表1铁铜摩尔置换比对铜置换率和品位的影响
表2温度对铜置换率和品位的影响
①从浸出液中置换铜的最佳铁铜摩尔置换比和最佳温度分别是___________ 。
②铁置换铜的铁铜摩尔置换比要比理论值1.0高,可能的原因是___________ 。
(4)在一定条件下,研究初始pH对沉砷率的影响,在pH=2时,稳定在98%左右,随着pH增大和温度升高,锌和镉的损失明显增加,原因是___________ 。
(5)写出“沉锌镉”时生成 的离子方程式:
的离子方程式:___________ 。若常温下“沉锌镉”后滤液中 的浓度降低为
的浓度降低为 ,此时滤液的pH为
,此时滤液的pH为___________ 。
(6)向锌镉沉淀中加入NaOH溶液,调整pH至12, 沉淀溶解,则该反应的离子方程式为
沉淀溶解,则该反应的离子方程式为___________ 。
 、CuO、CdO、
、CuO、CdO、 、PbO等固体物质,白烟尘综合利用可提高资源利用率,保护环境,其工艺流程如图所示。
、PbO等固体物质,白烟尘综合利用可提高资源利用率,保护环境,其工艺流程如图所示。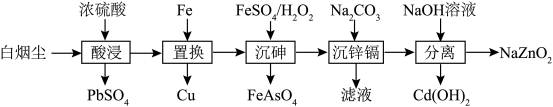
①常温下,
 的溶解度是
的溶解度是 ,
, 的溶解度是1g。
的溶解度是1g。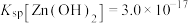 ,
, 。
。②
 易溶于盐酸,生成
易溶于盐酸,生成 :
: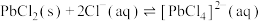 。
。③胶体对
 、
、 有吸附作用。
有吸附作用。回答下列问题:
(1)酸浸过程得到的浸出液中,砷元素主要以
 的形式存在,
的形式存在, 中As的化合价为
中As的化合价为(2)用硫酸、混酸(硫酸与盐酸)体系分别对白烟尘进行直接浸出,实验结果显示混酸体系可以进一步提高As、Cd的浸出率,但会导致铅的溶解,铅溶解的原因是
(3)表1、表2是在其他条件一定时,铁铜摩尔置换比
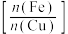 、温度对铜的置换率和品位(固体产物中所含某种金属或有用成分的多少)的影响。
、温度对铜的置换率和品位(固体产物中所含某种金属或有用成分的多少)的影响。表1铁铜摩尔置换比对铜置换率和品位的影响
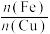 | 置换率/% | Cu品位/% |
| 1.2 | 74.87 | 51.22 |
| 1.4 | 92.17 | 72.82 |
| 1.6 | 99.92 | 72.08 |
| 温度/℃ | 置换率/% | Cu品位/% |
| 30 | 99.92 | 72.08 |
| 60 | 99.93 | 70.34 |
| 80 | 99.86 | 69.98 |
②铁置换铜的铁铜摩尔置换比要比理论值1.0高,可能的原因是
(4)在一定条件下,研究初始pH对沉砷率的影响,在pH=2时,稳定在98%左右,随着pH增大和温度升高,锌和镉的损失明显增加,原因是
(5)写出“沉锌镉”时生成
 的离子方程式:
的离子方程式: 的浓度降低为
的浓度降低为 ,此时滤液的pH为
,此时滤液的pH为(6)向锌镉沉淀中加入NaOH溶液,调整pH至12,
 沉淀溶解,则该反应的离子方程式为
沉淀溶解,则该反应的离子方程式为
您最近半年使用:0次
6 .  是一种橙红色液体,易水解产生使品红溶液褪色的气体,常作橡胶工业的硫化剂。某同学设计如图装置制备
是一种橙红色液体,易水解产生使品红溶液褪色的气体,常作橡胶工业的硫化剂。某同学设计如图装置制备 (熔点:―76℃,沸点:138℃)。下列说法错误的是
(熔点:―76℃,沸点:138℃)。下列说法错误的是
 是一种橙红色液体,易水解产生使品红溶液褪色的气体,常作橡胶工业的硫化剂。某同学设计如图装置制备
是一种橙红色液体,易水解产生使品红溶液褪色的气体,常作橡胶工业的硫化剂。某同学设计如图装置制备 (熔点:―76℃,沸点:138℃)。下列说法错误的是
(熔点:―76℃,沸点:138℃)。下列说法错误的是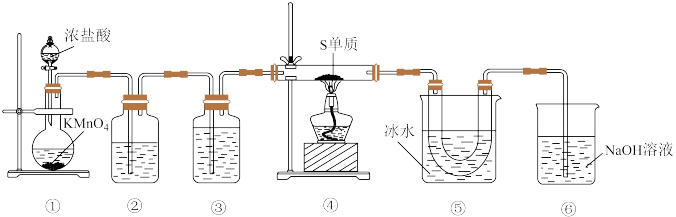
A. 分子中含有非极性共价键 分子中含有非极性共价键 |
B.装置②③中分别装有饱和 溶液、浓硫酸 溶液、浓硫酸 |
C.制备 的过程中可能发生反应: 的过程中可能发生反应: |
| D.该实验装置中有一处明显缺陷,可将装置⑥换成装有碱石灰的球形干燥管 |
您最近半年使用:0次
解题方法
7 . 甘肃矿产资源丰富,金属冶炼在国民经济发展中有着重要的作用。锰酸锂鲤离子蓄电池是第二代锂离子动力电池,工业上用某软锰矿(主要成分为 ,还含有少量铁、铝及硅的氧化物)为原料制备锰酸锂
,还含有少量铁、铝及硅的氧化物)为原料制备锰酸锂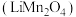 ,流程如图所示:
,流程如图所示:
(1)基态 原子的价电子排布式为
原子的价电子排布式为_______ , 元素位于元素周期表中的
元素位于元素周期表中的_______ 区。
(2)“酸浸”时,为了提升各物质的浸出速率,除了适当升高温度外,还可以采取的措施是_______ (写一条即可)。
(3)“还原”步骤得到的溶液中阳离子主要是 ,生成
,生成 的离子方程式为
的离子方程式为_______ ;滤渣1的主要成分为_______ 。
(4)已知某离子浓度[用 表示]形成沉淀与溶液
表示]形成沉淀与溶液 的关系如下图所示:
的关系如下图所示: 调节
调节 的范围是
的范围是_______ 。
(5)“沉锰”得到的是 和
和 滤饼,所得滤液回收可用于
滤饼,所得滤液回收可用于_______ 。
(6)“锂化”是将 和
和 按
按 的物质的量比配料,球磨
的物质的量比配料,球磨 ,然后升温至
,然后升温至 ,保温
,保温 ,自然冷却至室温得产品,写出化学反应方程式:
,自然冷却至室温得产品,写出化学反应方程式:_______ 。
 ,还含有少量铁、铝及硅的氧化物)为原料制备锰酸锂
,还含有少量铁、铝及硅的氧化物)为原料制备锰酸锂 ,流程如图所示:
,流程如图所示:
(1)基态
 原子的价电子排布式为
原子的价电子排布式为 元素位于元素周期表中的
元素位于元素周期表中的(2)“酸浸”时,为了提升各物质的浸出速率,除了适当升高温度外,还可以采取的措施是
(3)“还原”步骤得到的溶液中阳离子主要是
 ,生成
,生成 的离子方程式为
的离子方程式为(4)已知某离子浓度[用
 表示]形成沉淀与溶液
表示]形成沉淀与溶液 的关系如下图所示:
的关系如下图所示: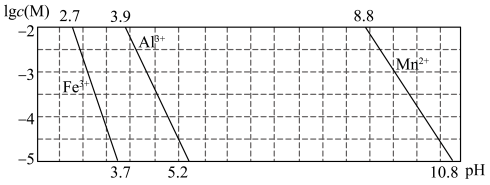
 调节
调节 的范围是
的范围是(5)“沉锰”得到的是
 和
和 滤饼,所得滤液回收可用于
滤饼,所得滤液回收可用于(6)“锂化”是将
 和
和 按
按 的物质的量比配料,球磨
的物质的量比配料,球磨 ,然后升温至
,然后升温至 ,保温
,保温 ,自然冷却至室温得产品,写出化学反应方程式:
,自然冷却至室温得产品,写出化学反应方程式:
您最近半年使用:0次
8 .  催化还原氮氧化物是目前应用最广泛的烟气脱硝技术。用活化的
催化还原氮氧化物是目前应用最广泛的烟气脱硝技术。用活化的 作催化剂,
作催化剂, 将
将 还原成
还原成 的一种反应历程如图所示。下列说法错误的是
的一种反应历程如图所示。下列说法错误的是
 催化还原氮氧化物是目前应用最广泛的烟气脱硝技术。用活化的
催化还原氮氧化物是目前应用最广泛的烟气脱硝技术。用活化的 作催化剂,
作催化剂, 将
将 还原成
还原成 的一种反应历程如图所示。下列说法错误的是
的一种反应历程如图所示。下列说法错误的是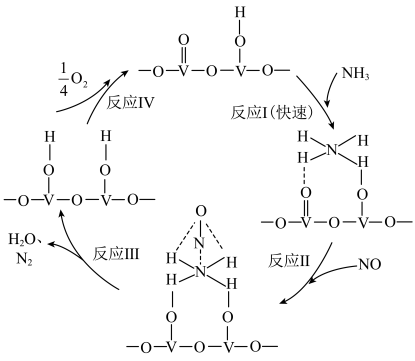
| A.该历程中能垒最高的是反应I |
| B.该历程中,V元素被氧化的只有反应Ⅳ |
C.该催化反应的总反应式为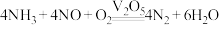 |
| D.整个历程中涉及极性键和非极性键的断裂和形成 |
您最近半年使用:0次
9 . 下列有关物质结构与性质的说法错误的是
| A.乙醇可与水互溶,是因为乙醇分子与水分子之间形成了氢键 |
B.熔融 能导电,是由于熔融状态下产生了自由移动的 能导电,是由于熔融状态下产生了自由移动的 和 和 |
| C.超分子是两种或两种以上的分子(包括离子)通过化学键形成的分子聚集体 |
D. 溶于氨水,是由于 溶于氨水,是由于 与 与 反应生成了可溶性配合物 反应生成了可溶性配合物 |
您最近半年使用:0次
10 . 下列叙述对应的离子方程式正确的是
A.向 溶液中滴加稀氨水: 溶液中滴加稀氨水: |
B.向苯酚钠溶液中通入少量CO2: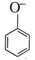 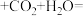 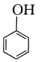 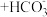 |
C.酸性 溶液氧化 溶液氧化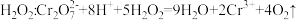 |
D. 溶液与过量 溶液与过量 溶液反应: 溶液反应: |
您最近半年使用:0次