名校
1 . 将 9.2g 铜和铁的混合物放入一定体积的稀硝酸溶液中,充分反应后得到标准状况下1.12LNO ,有金属剩余;向所得溶液中继续加入足量的稀硫酸,金属完全溶解且又得到标准状况下1.12LNO 。若向反应后的溶液中加入 KSCN 溶液,溶液不变红,则下列说法中正确的是
| A.原混合物中铜和铁各 0.1mol |
| B.第一次剩余金属全部为铜 |
| C.反应后的溶液中溶质为硝酸亚铁和硝酸铜 |
| D.若向反应后的溶液中再加入足量稀硝酸,又可得到约标准状况下 0.37LNO |
您最近一年使用:0次
解题方法
2 . 化学镀镍法得到的镀层均匀性,硬度等性能都较好,一种化学镀工艺流程如图所示:
②Ni(OH)2难溶于水;
③NaOH能稳定NaBH4,降低其水解率,NaBH4的水解反应:NaBH4+4H2O=Na[B(OH)4]+4H2;
有关材料下列说法正确的是
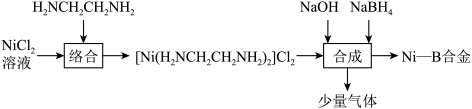
②Ni(OH)2难溶于水;
③NaOH能稳定NaBH4,降低其水解率,NaBH4的水解反应:NaBH4+4H2O=Na[B(OH)4]+4H2;
有关材料下列说法正确的是
| A.上述流程涉及到的物质中,含配位键的物质有2种 |
| B.“络合”时,将NiCl2溶液滴入到少量乙二胺(H2NCH2CH2NH2)中 |
| C.流程中使用H2NCH2CH2NH2,有利于调控溶液pH得到均匀性、硬度等性能较好的镀层 |
| D.“合成”时,NaBH4既作氧化剂又作还原剂 |
您最近一年使用:0次
3 . 下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 海带中提取碘单质时,用酒精作萃取剂 | 液体分层,下层溶液为紫红色 | 碘在有机溶剂中溶解度较大 |
| B | 稀盐酸加入碳酸钙后,将生成气体直接通入硅酸钠溶液中 | 生成白色胶状沉淀 | 非金属性: |
| C | 向 溶液中逐滴加入稀氨水至过量 溶液中逐滴加入稀氨水至过量 | 产生白色沉淀,并逐渐增多,后慢慢溶解 | 碱性: |
| D | 向足量 溶液中通入少量氯气,再加入淀粉 溶液中通入少量氯气,再加入淀粉 溶液 溶液 | 溶液先变橙色,后变为蓝色 | 氧化性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下,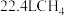 与 与 充分反应,生成的 充分反应,生成的 分子数为 分子数为 |
B. 与 与 的混合气体中含有的质子数为 的混合气体中含有的质子数为 |
C. 正丁烷和 正丁烷和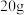 异丁烷的混合物中共价键数目为 异丁烷的混合物中共价键数目为 |
D.向密闭容器中充入 和 和 ,充分反应时转移电子 ,充分反应时转移电子 |
您最近一年使用:0次
名校
5 . 以高铅硫化锌原矿[主要含有ZnS,含有少量PbS、 、
、 、FeS、
、FeS、 (氧化铟)等]为原料制备单质Zn的工艺流程如图所示:
(氧化铟)等]为原料制备单质Zn的工艺流程如图所示: 。
。
②电解液浓度过大会导致溶液黏度变大,离子迁移速率低,电解效率低。
回答下列问题:
(1)“沸腾焙烧”的目的是______ ;其中杂质FeS充分焙烧产生大量废气,废气中主要成分的空间结构为______ 。
(2)“滤渣Ⅰ”的主要成分为______ 。
(3)“除铁”时 转化为FeOOH的离子方程式为
转化为FeOOH的离子方程式为______ 。
(4)“电解”硫酸锌溶液制备Zn的化学方程式为______ ,工业所需电解液浓度为40~60 的理由是
的理由是______ ,可用______ 光谱证明阴极析出的固体为Zn。
 、
、 、FeS、
、FeS、 (氧化铟)等]为原料制备单质Zn的工艺流程如图所示:
(氧化铟)等]为原料制备单质Zn的工艺流程如图所示:
 。
。②电解液浓度过大会导致溶液黏度变大,离子迁移速率低,电解效率低。
回答下列问题:
(1)“沸腾焙烧”的目的是
(2)“滤渣Ⅰ”的主要成分为
(3)“除铁”时
 转化为FeOOH的离子方程式为
转化为FeOOH的离子方程式为(4)“电解”硫酸锌溶液制备Zn的化学方程式为
 的理由是
的理由是
您最近一年使用:0次
6 . 下列化学用语的表达正确的是
A.乙醛的空间填充模型为: |
B.基态Ge原子的最高能层电子排布式为: |
C.基态铍原子最外层电子的电子云轮廓图为: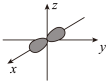 |
D.次氯酸钙溶液与过量亚硫酸氢钠溶液反应的离子方程式为: |
您最近一年使用:0次
7 . 光照下,氧化锌纳米棒具有优异的光催化活性,可用于制备过氧化氢,反应机理如图所示( 表示电子跃迁产生的空穴)。下列叙述错误的是
表示电子跃迁产生的空穴)。下列叙述错误的是
 表示电子跃迁产生的空穴)。下列叙述错误的是
表示电子跃迁产生的空穴)。下列叙述错误的是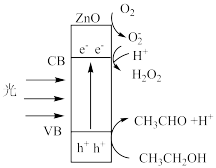
| A.反应过程中吸收了光能,说明总反应为吸热反应 |
B.中间体 含有单电子,结构不稳定、反应活性强 含有单电子,结构不稳定、反应活性强 |
C.理论上生成 和 和 的物质的量之比为1:1 的物质的量之比为1:1 |
D.乙醇发生的反应可表示为 |
您最近一年使用:0次
名校
解题方法
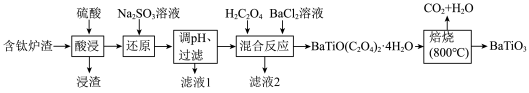
8 . BaTiO3,被用作陶瓷电容器的介电材料、麦克风和其他传感器的压电材料。以含钛炉渣(主要成分是TiO2,含少量Fe2O3、CaO、SiO2等)为原料制备BaTiO3的流程如下:
回答下列问题:
(1)下列为Ba粒子简化电子排布式,其中能量最高的是 (填字母)。
(2)“还原”中发生反应的离子方程式为________ 。若省去“还原”工艺,则________ 。
(3)设计实验检验滤液1中是否含有Fe2+:________ 。
(4)BaTiO(C2O4)2·4H2O中Ti的化合价为________ ,“焙烧”发生反应的化学方程式为________ 。
(5)经X射线分析鉴定,钛酸钡(BaTiO3)的晶胞结构如下图所示(Ti4+、Ba2+均与O2-相接触),已知晶胞边长为 pm,O2-的半径为
pm,O2-的半径为 pm,则Ti4+、Ba2+的半径分别为
pm,则Ti4+、Ba2+的半径分别为______ pm、______ pm。(用含 、
、 的代数式表示)
的代数式表示)
| 金属离子 | TiO2+ | Fe2+ | Fe3+ |
| 开始沉淀的pH | 0.5 | 6.3 | 1.5 |
| 完全沉淀的pH | 2.5 | 8.3 | 2.8 |
(1)下列为Ba粒子简化电子排布式,其中能量最高的是 (填字母)。
| A.[Xe]6s2 | B.[Xe]6s1 | C.[Xe]6s16p1 | D.[Xe]6s0p2 |
(2)“还原”中发生反应的离子方程式为
(3)设计实验检验滤液1中是否含有Fe2+:
(4)BaTiO(C2O4)2·4H2O中Ti的化合价为
(5)经X射线分析鉴定,钛酸钡(BaTiO3)的晶胞结构如下图所示(Ti4+、Ba2+均与O2-相接触),已知晶胞边长为
 pm,O2-的半径为
pm,O2-的半径为 pm,则Ti4+、Ba2+的半径分别为
pm,则Ti4+、Ba2+的半径分别为 、
、 的代数式表示)
的代数式表示)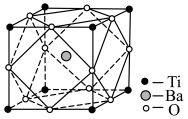
您最近一年使用:0次
名校
9 . 下列化学用语表示错误的是
| A.碳化硅的化学式:SiC | B.甲醛中π键的电子云轮廓图: |
C. 的电子式: 的电子式: | D.邻羟基苯甲醛的分子内氢键: |
您最近一年使用:0次
昨日更新
|
53次组卷
|
3卷引用:湖北省黄冈中学2024届高三下学期5月第三次模拟考试化学试题
10 . 亚氯酸钠 是一种重要的含氯消毒剂。马蒂逊法制备亚氯酸钠的流程如图,下列说法错误的是
是一种重要的含氯消毒剂。马蒂逊法制备亚氯酸钠的流程如图,下列说法错误的是
 是一种重要的含氯消毒剂。马蒂逊法制备亚氯酸钠的流程如图,下列说法错误的是
是一种重要的含氯消毒剂。马蒂逊法制备亚氯酸钠的流程如图,下列说法错误的是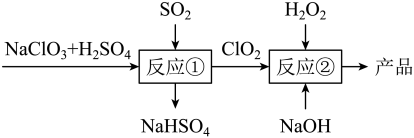
A.反应①阶段,参加反应的 和 和 的物质的量之比为2:1 的物质的量之比为2:1 |
B.反应②条件下, 的氧化性大于 的氧化性大于 |
C.反应②中的 可用 可用 代替 代替 |
D.若反应①通过原电池来实现,则 是正极产物 是正极产物 |
您最近一年使用:0次



