1 . 下列化学用语书写正确的一项是
| A.烧碱:KOH | B.硫离子的离子符号: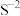 |
| C.苏打:NaHCO3 | D.硫酸钾在水中的电离方程式: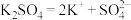 |
您最近一年使用:0次
名校
2 . 《说文》中记述:天生者称卤,煮成者叫盐。食盐的主要成分是
| A.NaOH | B. | C.NaCl | D. |
您最近一年使用:0次
解题方法
3 . 下表是元素周期表的一部分,针对编号①~⑫元素,回答下列有关问题:
(1)在这些元素中,非金属性最强的元素是_______ (填元素符号,下同),最不活泼的元素是_______ 。
(2)写出元素①对应气态氢化物的化学式和电子式:_______ 、_______ 。
(3)在元素③和④中,单质与水反应较剧烈的是_______ (填元素符号),它与水反应的化学方程式是_______ 。
(4)在元素③、④与⑤的最高价氧化物对应的水化物中,碱性最弱是_______ (填化学式)。
(5)能证明⑧和⑫单质氧化性强弱的实验事实 用离子方程式表示)是
用离子方程式表示)是_______ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |  |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 四 | ⑩ | ⑪ | ⑫ |
(2)写出元素①对应气态氢化物的化学式和电子式:
(3)在元素③和④中,单质与水反应较剧烈的是
(4)在元素③、④与⑤的最高价氧化物对应的水化物中,碱性最弱是
(5)能证明⑧和⑫单质氧化性强弱的实验事实
 用离子方程式表示)是
用离子方程式表示)是
您最近一年使用:0次
4 . 溴及其化合物是重要的化工基础原料,广泛应用于制药、染料、电子、日化等行业。
Ⅰ.用图所示装置A可制取氯气。将纯净的氯气通入装置C的NaBr溶液中可以在实验室制取少量溴单质。_______ 。
(2)为了富集生成的溴单质,用热空气吹出,并在装置D中收集,则装置D中可选用的试剂为_______。
Ⅱ.工业上从海水中提取 过程更为复杂。研究集中在空气吹出法,空气吹出法提溴对原料的适应性高,但吹出设备庞大,且能耗高。某工厂针对空气吹出法的缺点进行工艺改造,提出连续双段真空提溴工艺,如图转化过程:
过程更为复杂。研究集中在空气吹出法,空气吹出法提溴对原料的适应性高,但吹出设备庞大,且能耗高。某工厂针对空气吹出法的缺点进行工艺改造,提出连续双段真空提溴工艺,如图转化过程:_______ 。主反应塔1中温度保持在82~99℃,减少了水蒸气的用量。从化学性质的角度分析这么做的主要目的有两点:①减少氯气与水的反应,②减少_______ 反应。从经济角度来看这么做还可以减少的_______ 用量。
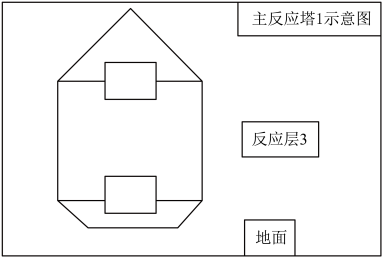
(4)为了让原料卤水与氯气在主反应塔1中更充分反应,请将正确装置对应的选项填在图中“□”处:_______ 。_______ 。冷凝器需要铺设循环冷却水管道,循环冷却水管道中水流方向是_______ (填“从地面到顶端”或“从顶端到地面”),请说明原因_______ 。
(6)在分离器中经冷凝、分离、纯化后制得精溴。少量氯、溴与混合废气需要经过水蒸气喷射泵喷入气体吸收器。此时,还需进行酸化调节,再经过排水管通入主反应塔1中循环利用。请写出吸收器中酸化调节主要发生的离子反应方程式:_______ 。
Ⅰ.用图所示装置A可制取氯气。将纯净的氯气通入装置C的NaBr溶液中可以在实验室制取少量溴单质。
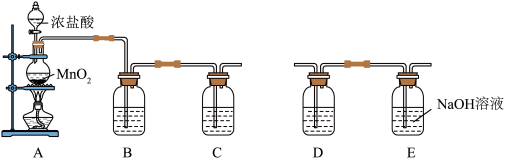
(2)为了富集生成的溴单质,用热空气吹出,并在装置D中收集,则装置D中可选用的试剂为_______。
A. | B.NaOH | C.KI | D. |
Ⅱ.工业上从海水中提取
 过程更为复杂。研究集中在空气吹出法,空气吹出法提溴对原料的适应性高,但吹出设备庞大,且能耗高。某工厂针对空气吹出法的缺点进行工艺改造,提出连续双段真空提溴工艺,如图转化过程:
过程更为复杂。研究集中在空气吹出法,空气吹出法提溴对原料的适应性高,但吹出设备庞大,且能耗高。某工厂针对空气吹出法的缺点进行工艺改造,提出连续双段真空提溴工艺,如图转化过程:
(4)为了让原料卤水与氯气在主反应塔1中更充分反应,请将正确装置对应的选项填在图中“□”处:

(6)在分离器中经冷凝、分离、纯化后制得精溴。少量氯、溴与混合废气需要经过水蒸气喷射泵喷入气体吸收器。此时,还需进行酸化调节,再经过排水管通入主反应塔1中循环利用。请写出吸收器中酸化调节主要发生的离子反应方程式:
您最近一年使用:0次
名校
解题方法
5 . 1869年俄国化学家门捷列夫制出第一张 元素周期表,元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。针对下表中的短周期元素,回答以下问题:______ 。
(2)①和④形成的10电子阳离子的电子式______ ,由①⑤⑧三种元素组成的具有漂白性物质的结构式______ 。
(3)⑥和⑦的最高价氧化物对应水化物之间反应的化学方程式______ 。
(4)下列能比较元素②和③金属性强弱的实验事实是(填字母)______ 。
a.在化合物中②的化合价比③的低 b.②的单质能与冷水剧烈反应而③的单质不能
c.②的最高价氧化物对应水化物的碱性比③强 d.②单质的熔点比③单质的低
(5)与第三周期主族元素的离子半径相对大小相符的曲线标号______ 。 纳米复合物)能以太阳光为能源,使水分解获得
纳米复合物)能以太阳光为能源,使水分解获得 ,其原理如图所示。反应①的化学方程式是
,其原理如图所示。反应①的化学方程式是______ 。

(2)①和④形成的10电子阳离子的电子式
(3)⑥和⑦的最高价氧化物对应水化物之间反应的化学方程式
(4)下列能比较元素②和③金属性强弱的实验事实是(填字母)
a.在化合物中②的化合价比③的低 b.②的单质能与冷水剧烈反应而③的单质不能
c.②的最高价氧化物对应水化物的碱性比③强 d.②单质的熔点比③单质的低
(5)与第三周期主族元素的离子半径相对大小相符的曲线标号
a. b.
b. c.
c.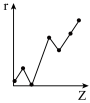 d.
d.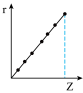
 纳米复合物)能以太阳光为能源,使水分解获得
纳米复合物)能以太阳光为能源,使水分解获得 ,其原理如图所示。反应①的化学方程式是
,其原理如图所示。反应①的化学方程式是
您最近一年使用:0次
名校
解题方法
6 . 海洋资源的利用具有非常广阔的前景。地球上99%的溴元素以溴离子的形式存在于海水中,因此人们也把溴称为“海洋元素”。空气吹出法工艺是目前“海水提溴”的最主要方法之一,海水提溴的工艺流程如图:______ 这一物理性质将低浓度Br2分离出来。
(2)“吸收塔”中发生的离子反应为______ ;请你设计实验说明“吸收塔”中含硫微粒的主要存在形式:______ 。
(3)已知常压下Br2的沸点是59℃。蒸馏塔中温度控制在______的范围内较合适。
(4)探究“氧化”的适宜条件,测得不同条件下溶液中被氧化的Br-的百分含量如图: 表示加入氯元素与海水中溴元素物质的量之比。
表示加入氯元素与海水中溴元素物质的量之比。
“氧化”的适宜条件为______ 。
(5)(CNO)2、(CN)2、(SCN)2被称为拟卤素单质,具有卤素相似的性质。为了探究Br2、(CN)2、(CNO)2、(SCN)2的氧化性强弱,进行实验,实验操作及现象如下:
已知:拟卤素单质及钾盐水溶液均为无色。
①如果氧化产物为(SCN)2,写出操作乙中反应的离子方程式:______ 。
②某同学得出结论,氧化性:(CNO)2>Br2>(CN)2>(SCN)2。该结论是否合理?并说明理由______

(2)“吸收塔”中发生的离子反应为
(3)已知常压下Br2的沸点是59℃。蒸馏塔中温度控制在______的范围内较合适。
| A.20℃~30℃ | B.45℃~55℃ | C.75℃~85℃ | D.100℃~110℃ |
(4)探究“氧化”的适宜条件,测得不同条件下溶液中被氧化的Br-的百分含量如图:
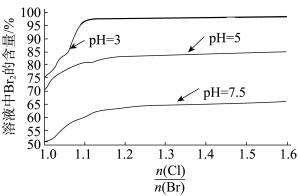
 表示加入氯元素与海水中溴元素物质的量之比。
表示加入氯元素与海水中溴元素物质的量之比。“氧化”的适宜条件为
(5)(CNO)2、(CN)2、(SCN)2被称为拟卤素单质,具有卤素相似的性质。为了探究Br2、(CN)2、(CNO)2、(SCN)2的氧化性强弱,进行实验,实验操作及现象如下:
实验操作 | 现象 | |
甲 | 向KCNO溶液中滴加几滴溴水,振荡 | 溶液不褪色 |
乙 | 向KSCN溶液中滴加溴水,振荡 | 溶液褪色 |
丙 | 向KCN溶液中滴加溴水,振荡 | 溶液褪色 |
①如果氧化产物为(SCN)2,写出操作乙中反应的离子方程式:
②某同学得出结论,氧化性:(CNO)2>Br2>(CN)2>(SCN)2。该结论是否合理?并说明理由
您最近一年使用:0次
名校
7 . A、B、C、D、E、F、G为短周期主族元素,且原子序数依次递增。A、E同主族,D、F同主族。A与其他非金属元素化合时易形成共价化合物,E与其他非金属元素化合时易形成离子化合物, 与
与 核外电子排布相同。由以上元素组成的物质BD和
核外电子排布相同。由以上元素组成的物质BD和 具有相同的电子数。回答以下问题:
具有相同的电子数。回答以下问题:
(1)写出元素的名称:B_______ ,D_______ 。
(2)G元素在元素周期表的位置是_______ 。
(3) 的离子结构示意图为
的离子结构示意图为_______ 。
(4)用电子式表示 的形成过程:
的形成过程:_______ 。
(5)由A、D、E三种元素形成的化合物含有的化学键有_______ 。
(6)由题(5)的化合物与元素G的最高价氧化物的水化物反应的化学方程式是_______ 。
(7)设计实验验证B、F两元素的非金属性强弱(用离子方程式表示)_______ 。
(8)由B、C、E三种元素组成的某剧毒化合物EBC不慎泄漏时,消防人员通常采用喷洒由A、D两元素按原子数1∶1组成的化合物溶液的方式处理,以减少污染。反应生成一种酸式盐和一种气体,二者的水溶液均呈碱性,则该反应的离子方程式为_______ 。
 与
与 核外电子排布相同。由以上元素组成的物质BD和
核外电子排布相同。由以上元素组成的物质BD和 具有相同的电子数。回答以下问题:
具有相同的电子数。回答以下问题:(1)写出元素的名称:B
(2)G元素在元素周期表的位置是
(3)
 的离子结构示意图为
的离子结构示意图为(4)用电子式表示
 的形成过程:
的形成过程:(5)由A、D、E三种元素形成的化合物含有的化学键有
(6)由题(5)的化合物与元素G的最高价氧化物的水化物反应的化学方程式是
(7)设计实验验证B、F两元素的非金属性强弱(用离子方程式表示)
(8)由B、C、E三种元素组成的某剧毒化合物EBC不慎泄漏时,消防人员通常采用喷洒由A、D两元素按原子数1∶1组成的化合物溶液的方式处理,以减少污染。反应生成一种酸式盐和一种气体,二者的水溶液均呈碱性,则该反应的离子方程式为
您最近一年使用:0次
8 . 铍的氧化物广泛应用于原子能、航天、电子、陶瓷等领域,是重要的战略物资。利用绿柱石(主要化学成分为 ,还含有一定量的
,还含有一定量的 和
和 )生产
)生产 的一种工艺流程如下。
的一种工艺流程如下。
①绿柱石主要化学成分写成氧化物的形式为: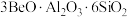
② 与
与 在周期表位置符合对角线规则,
在周期表位置符合对角线规则, 与
与 性质相似,
性质相似, 与
与 性质相似
性质相似
③ 被沉淀完全的
被沉淀完全的 ;
;
回答问题:
(1)粉碎的目的是______ ;
(2)无水 可用作聚合反应的催化剂。
可用作聚合反应的催化剂。 、
、 与
与 在600~800℃制备
在600~800℃制备 且生成一种毒性气体,化学方程式为
且生成一种毒性气体,化学方程式为_____ 。
(3)残渣主要成分是(填化学式)_____ 。浸取中浓硫酸的作用除了用于溶解矿石外,还起的作用_____ ;
(4)该流程中能循环使用的物质是_____ (填化学式)。
(5)沉铍时,用氢氧化钠溶液代替氨水得到 的量可能减少,用离子方程说明理由
的量可能减少,用离子方程说明理由_____ 。
(6)wg绿柱石( 含量14%)经过一系列反应后得到
含量14%)经过一系列反应后得到 ag(纯度90%),则
ag(纯度90%),则 的产率为
的产率为_____ 。
 ,还含有一定量的
,还含有一定量的 和
和 )生产
)生产 的一种工艺流程如下。
的一种工艺流程如下。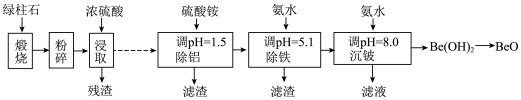
①绿柱石主要化学成分写成氧化物的形式为:
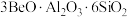
②
 与
与 在周期表位置符合对角线规则,
在周期表位置符合对角线规则, 与
与 性质相似,
性质相似, 与
与 性质相似
性质相似③
 被沉淀完全的
被沉淀完全的 ;
;回答问题:
(1)粉碎的目的是
(2)无水
 可用作聚合反应的催化剂。
可用作聚合反应的催化剂。 、
、 与
与 在600~800℃制备
在600~800℃制备 且生成一种毒性气体,化学方程式为
且生成一种毒性气体,化学方程式为(3)残渣主要成分是(填化学式)
(4)该流程中能循环使用的物质是
(5)沉铍时,用氢氧化钠溶液代替氨水得到
 的量可能减少,用离子方程说明理由
的量可能减少,用离子方程说明理由(6)wg绿柱石(
 含量14%)经过一系列反应后得到
含量14%)经过一系列反应后得到 ag(纯度90%),则
ag(纯度90%),则 的产率为
的产率为
您最近一年使用:0次
名校
9 . 下列装置及操作能达到对应目的的是
|
|
A.用乙醇萃取碘水中的 后分液 后分液 | B.用蒸发法提取食盐水中的NaCl |
|
|
| C.用升华法分离碘和氯化铵固体 | D.用过滤法除去 胶体中含有的杂质NaCl 胶体中含有的杂质NaCl |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 下列说法中,不正确的是
A.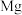 的摩尔质量是 的摩尔质量是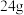 |
B.标况下,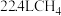 的物质的量为 的物质的量为 |
C.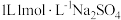 溶液中含有 溶液中含有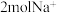 |
D.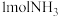 中含有的分子数约为 中含有的分子数约为 |
您最近一年使用:0次







