名校
1 . 氢氧化铬是一种两性氢氧化物,主要用于制备三价铬盐及三氧化二铬,也可用于油漆、颜料生产及羊毛处理等。利用铬渣(铬以低价态含氧酸盐的形式存在,主要杂质为铁、铝、硅、磷等的化合物)制备氢氧化铬的流程如图。已知:最高价铬酸根离子在酸性介质中以 形式存在,在碱性介质中以
形式存在,在碱性介质中以 形式存在,
形式存在, 在pH>12时开始溶解。下列说法错误的是
在pH>12时开始溶解。下列说法错误的是
 形式存在,在碱性介质中以
形式存在,在碱性介质中以 形式存在,
形式存在, 在pH>12时开始溶解。下列说法错误的是
在pH>12时开始溶解。下列说法错误的是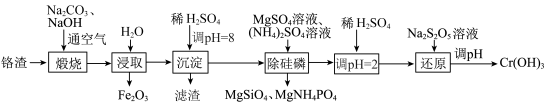
A. 常用作红色涂料 常用作红色涂料 |
B.滤渣中含有 |
C.“煅烧”后铬被氧化为 |
D.“还原”工序发生的反应为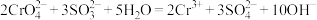 |
您最近一年使用:0次
名校
2 . 光催化 转化与选择性有机合成耦合到同一反应系统中,具有实现可持续经济和社会发展目标的潜力。其中某种反应如下,设
转化与选择性有机合成耦合到同一反应系统中,具有实现可持续经济和社会发展目标的潜力。其中某种反应如下,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 转化与选择性有机合成耦合到同一反应系统中,具有实现可持续经济和社会发展目标的潜力。其中某种反应如下,设
转化与选择性有机合成耦合到同一反应系统中,具有实现可持续经济和社会发展目标的潜力。其中某种反应如下,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是CO2+2n
 n
n +nNH3+H2O+CO+xH2
+nNH3+H2O+CO+xH2
| A.该反应为缩聚反应 |
B.1mol  含有的 含有的 键数为4 键数为4 |
C.1mol 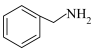 含有的碳碳双键数为3 含有的碳碳双键数为3 |
D.该反应每消耗1mol  ,生成 ,生成 分子的数目为 分子的数目为 |
您最近一年使用:0次
解题方法
3 . 根据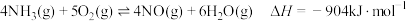 ,下列说法
,下列说法不正确 的是
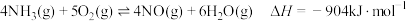 ,下列说法
,下列说法A.反应的 |
B.有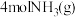 和 和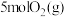 在反应器中充分反应,能放出 在反应器中充分反应,能放出 热量 热量 |
C.断裂1mol 键的同时,断裂 键的同时,断裂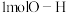 键,说明该反应达到平衡状态 键,说明该反应达到平衡状态 |
D.每消耗 转移电子的数目约为 转移电子的数目约为 |
您最近一年使用:0次
名校
解题方法
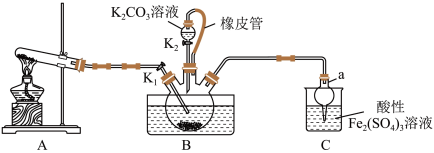
4 . 硫氰化钾(KSCN)是一种用途广泛的化工原料,常用于染料、药物的生产。实验小组设计如图实验装置模拟工业制备 KSCN 并进行相关探究实验。___________ 。
(2)装置A用于实验室制备氨气,反应的化学方程式为___________ 。
(3)装置B中,三颈烧瓶内盛放有 CS₂、水和固体催化剂,通入氨气的导管口需要浸没在 CS₂液体中,其目的是___________ (写两点)。
(4)KSCN 溶液的制备:实验开始时打开K₁,加热装置A、D,待三颈烧瓶内液体不分层后,熄灭装置A处的酒精灯,关闭K₁,移开水浴。将装置B继续加热至 待 NH₄HS 完全分解后(
待 NH₄HS 完全分解后(  打开 K₂,缓缓滴入适量的)
打开 K₂,缓缓滴入适量的)  溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是
溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是___________ 。
(5)尾气处理:装置C 中仪器a的名称是___________ ,酸性Fe₂(SO₄)₃溶液用于除去尾气中两种污染性气体,其中一种气体M能使酚酞溶液变红,另一种气体N能使溶液产生淡黄色沉淀,写出除去气体N的离子方程式___________ 。
(6)过滤装置C中吸收尾气后的悬浊液,得到滤液x。取少量滤液x进行如图实验[已知 (白色)]:
(白色)]:___________ [可供选择的试剂:  溶液、
溶液、  溶液、
溶液、  溶液、
溶液、  溶液]。
溶液]。

(2)装置A用于实验室制备氨气,反应的化学方程式为
(3)装置B中,三颈烧瓶内盛放有 CS₂、水和固体催化剂,通入氨气的导管口需要浸没在 CS₂液体中,其目的是
(4)KSCN 溶液的制备:实验开始时打开K₁,加热装置A、D,待三颈烧瓶内液体不分层后,熄灭装置A处的酒精灯,关闭K₁,移开水浴。将装置B继续加热至
 待 NH₄HS 完全分解后(
待 NH₄HS 完全分解后(  打开 K₂,缓缓滴入适量的)
打开 K₂,缓缓滴入适量的)  溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是
溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是(5)尾气处理:装置C 中仪器a的名称是
(6)过滤装置C中吸收尾气后的悬浊液,得到滤液x。取少量滤液x进行如图实验[已知
 (白色)]:
(白色)]: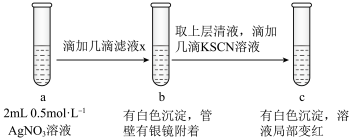
 溶液、
溶液、  溶液、
溶液、  溶液、
溶液、  溶液]。
溶液]。
您最近一年使用:0次
名校
解题方法
5 . 某科研人员提出:HCHO 与 O₂在羟基磷灰石(HAP)表面催化氧化生成(  和
和 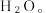 该历程示意图如下(图中只画出了 HAP 的部分结构)。下列说法正确的是
该历程示意图如下(图中只画出了 HAP 的部分结构)。下列说法正确的是
 和
和 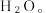 该历程示意图如下(图中只画出了 HAP 的部分结构)。下列说法正确的是
该历程示意图如下(图中只画出了 HAP 的部分结构)。下列说法正确的是
| A.用 HAP 高效去除居室污染,符合绿色化学理念 |
| B.在反应示意图中,有 C—H键的断裂和C==O键的形成 |
| C.根据图示信息,CO₂分子中的氧原子全部来自O₂ |
| D.反应前后分子种类、原子种类均发生了变化 |
您最近一年使用:0次
名校
6 . 下列选项所示的物质间转化均能一步实现的是
A.NaCl(aq)→ Cl₂(g)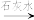 漂白粉(s) 漂白粉(s) |
B.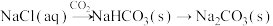 |
C.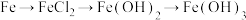 |
D. |
您最近一年使用:0次
名校
解题方法
7 . 下列有关化学用语的表示错误的是
A.苯的空间填充模型:  | B.次氯酸的结构式: H—O—Cl |
| C.乙炔的结构简式: CH≡CH | D.乙酸的电子式: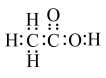 |
您最近一年使用:0次
解题方法
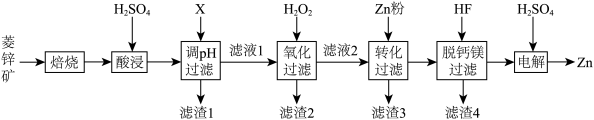
8 . 以菱锌矿(主要含有ZnCO3,另含有少量CaO、Fe2O3、FeO、CoO、CuO、SiO2等)为原料电解制Zn的流程如图:
(1)“酸浸”时为提高锌的浸出率,可采取的措施有___________ (写出一种即可)。
(2)“调pH过滤”中,物质X最适宜选择___________ (填标号)。
A.NaOH B.Ca(OH)2 C.NH3·H2O
(3)“氧化过滤”中,Fe2+转化为Fe(OH)3沉淀的离子方程式为___________ 。若反应结束时,溶液pH为5,则残留的c(Fe3+)=___________ mol·L-l。
(4)H2O2是常见绿色氧化剂,原因是___________ 。
(5)“脱钙镁过滤”后,溶液中 =
=___________ 。
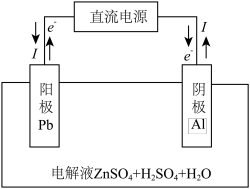
(6)“电解”装置示意如图,开始通电后,阳极表面生成PbO2,保护阳极不被酸性电解液腐蚀,相应的电极反应式为___________ 。
| 物质 | Fe(OH)3 | Zn(OH)2 | MgF2 | CaF2 |
| Ksp | 2.7×10-39 | 1.3×10-17 | 5.2×10-11 | 3.9×10-9 |
(1)“酸浸”时为提高锌的浸出率,可采取的措施有
(2)“调pH过滤”中,物质X最适宜选择
A.NaOH B.Ca(OH)2 C.NH3·H2O
(3)“氧化过滤”中,Fe2+转化为Fe(OH)3沉淀的离子方程式为
(4)H2O2是常见绿色氧化剂,原因是
(5)“脱钙镁过滤”后,溶液中
 =
=(6)“电解”装置示意如图,开始通电后,阳极表面生成PbO2,保护阳极不被酸性电解液腐蚀,相应的电极反应式为
您最近一年使用:0次
解题方法
9 . 室温下,下列各组离子在指定溶液中一定能大量共存的是
A.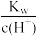 =1×10-13mol·L-1的溶液中K+、Na+、 =1×10-13mol·L-1的溶液中K+、Na+、 、 、 |
B.水电离的c(OH-)=1×10-13mol·L-1的溶液:Na+、 、Br-、Ba2+ 、Br-、Ba2+ |
C.pH=2的溶液: 、Cl-、Fe2+、 、Cl-、Fe2+、 |
D. =1012的溶液:Fe2+、Al3+、 =1012的溶液:Fe2+、Al3+、 、I- 、I- |
您最近一年使用:0次
10 . 设NA为阿伏加德罗常数的值,下列说法错误的是
| A.1L0.1mol·L-1CH3COONa溶液中,CH3COO-的数目小于0.1NA |
| B.常温下,1LpH=1的H2SO4溶液中,H+的数目为0.1NA |
| C.32gSO2与过量O2反应生成的SO3分子数为0.5NA |
| D.电解饱和食盐水收集到标准状况下2.24L氯气,转移电子数为0.2NA |
您最近一年使用:0次



