解题方法
1 . 钠、铁及它们的化合物在生产、生活中有着重要的用途。
(1)某汽车安全气囊的产气药剂主要含有 、
、 、
、 、
、 等物质。当汽车发生碰撞时,
等物质。当汽车发生碰撞时, 迅速分解产生
迅速分解产生 和Na,同时放出大量的热,
和Na,同时放出大量的热, 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。
① 是助氧化剂,可处理产生的Na,其中氯元素的化合价是
是助氧化剂,可处理产生的Na,其中氯元素的化合价是___________ 。
② 是主氧化剂,也可处理产生的Na,反应为
是主氧化剂,也可处理产生的Na,反应为 ,反应中
,反应中 是
是___________ (填“还原产物”或“氧化产物”)。
(2)铁及其重要化合物之间的部分转化关系如图所示。___________ (填序号);
a.金红石(TiO2) b.赤铁矿(Fe2O3) c.辉铜矿(Cu2S)
②实现Fe转化为Fe2+可选用足量的___________ (填序号);
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
③在点燃的条件下,Fe与足量Cl2剧烈反应后,将产物溶于水,再滴加KSCN溶液,则溶液变为血红色,证明产物为FeCl3,写出氯气和铁反应的化学方程式为___________ 。
④在FeSO4中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为___________ ,此过程中发生的氧化还原反应为(用化学方程式表达)___________ 。
(1)某汽车安全气囊的产气药剂主要含有
 、
、 、
、 、
、 等物质。当汽车发生碰撞时,
等物质。当汽车发生碰撞时, 迅速分解产生
迅速分解产生 和Na,同时放出大量的热,
和Na,同时放出大量的热, 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。①
 是助氧化剂,可处理产生的Na,其中氯元素的化合价是
是助氧化剂,可处理产生的Na,其中氯元素的化合价是②
 是主氧化剂,也可处理产生的Na,反应为
是主氧化剂,也可处理产生的Na,反应为 ,反应中
,反应中 是
是(2)铁及其重要化合物之间的部分转化关系如图所示。
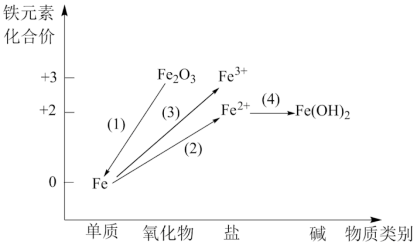
a.金红石(TiO2) b.赤铁矿(Fe2O3) c.辉铜矿(Cu2S)
②实现Fe转化为Fe2+可选用足量的
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
③在点燃的条件下,Fe与足量Cl2剧烈反应后,将产物溶于水,再滴加KSCN溶液,则溶液变为血红色,证明产物为FeCl3,写出氯气和铁反应的化学方程式为
④在FeSO4中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为
您最近一年使用:0次
2 . 下表列出了①~⑥六种元素在周期表中的位置。
回答下列问题(用化学用语填空):
(1)元素①的一种核素中,含有1个质子和1个中子,表示该核素组成的符号是___________ 。
(2)上述元素中,原子半径最大的是___________ (填元素符号)。
(3)由元素①、⑥组成的化合物的电子式为___________ 。
(4)元素⑤和⑥最高价氧化物对应的水化物酸性由强到弱的顺序是___________ (填化学式)。
(5)金属性:③___________ ④(填“>”或“<”),它们的最高价氧化物对应的水化物反应的离子方程式为___________ 。
(6)下列说法正确的是___________ (填序号)。
a.元素②、③组成的化合物只有一种
b.元素②的气态氢化物稳定性高于元素⑤的气态氢化物
c.元素⑥在化合物中呈现的最高化合价为+7价
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ |
(1)元素①的一种核素中,含有1个质子和1个中子,表示该核素组成的符号是
(2)上述元素中,原子半径最大的是
(3)由元素①、⑥组成的化合物的电子式为
(4)元素⑤和⑥最高价氧化物对应的水化物酸性由强到弱的顺序是
(5)金属性:③
(6)下列说法正确的是
a.元素②、③组成的化合物只有一种
b.元素②的气态氢化物稳定性高于元素⑤的气态氢化物
c.元素⑥在化合物中呈现的最高化合价为+7价
您最近一年使用:0次
解题方法
3 . Ⅰ.某小组同学探究Na2CO3的性质。
(1)用Na2CO3固体配制100 mL 0.200 mol·L-1Na2CO3溶液。
①用到的仪器有:天平、药匙、量筒、烧杯、玻璃棒、胶头滴管和___________ 。
②计算需要Na2CO3固体的质量是___________ g。
③下列情况中,会使所配溶液浓度偏高的是___________ (填字母)。
a.转移时,没有洗涤烧杯和玻璃棒
b.定容时,眼睛俯视刻度线
c.摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
(2)探究Na2CO3与盐酸的反应。向0.200 mol·L-1Na2CO3溶液中滴加稀盐酸,开始无气泡,继续滴加,产生气泡,反应的离子方程式为: +H+=
+H+= 、
、___________ 。
Ⅱ.某化学兴趣小组设计如下实验探究KMnO4固体与草酸(H2C2O4,具有还原性)反应的产物,以其产物为原料制备氯气:
室温下,取KMnO4固体于锥形瓶中,加入适量的草酸(H2C2O4)溶液,振荡,充分反应,可以观察到有黑色沉淀产生,溶液变为无色,同时生成无色无味的气体M,将燃着的木条靠近锥形瓶瓶口时木条熄灭。
分析实验并回答相应问题。
(3)M的化学式是___________ 。
(4)将充分反应后的混合物过滤,检验滤液中金属阳离子的方法及现象为___________ 、___________ 。向滤液中加入盐酸时又产生无色无味气体。
(5)将滤渣加入浓盐酸中加热,产生黄绿色气体,该反应的离子方程式为___________ 。
(1)用Na2CO3固体配制100 mL 0.200 mol·L-1Na2CO3溶液。
①用到的仪器有:天平、药匙、量筒、烧杯、玻璃棒、胶头滴管和
②计算需要Na2CO3固体的质量是
③下列情况中,会使所配溶液浓度偏高的是
a.转移时,没有洗涤烧杯和玻璃棒
b.定容时,眼睛俯视刻度线
c.摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
(2)探究Na2CO3与盐酸的反应。向0.200 mol·L-1Na2CO3溶液中滴加稀盐酸,开始无气泡,继续滴加,产生气泡,反应的离子方程式为:
 +H+=
+H+= 、
、Ⅱ.某化学兴趣小组设计如下实验探究KMnO4固体与草酸(H2C2O4,具有还原性)反应的产物,以其产物为原料制备氯气:
室温下,取KMnO4固体于锥形瓶中,加入适量的草酸(H2C2O4)溶液,振荡,充分反应,可以观察到有黑色沉淀产生,溶液变为无色,同时生成无色无味的气体M,将燃着的木条靠近锥形瓶瓶口时木条熄灭。
分析实验并回答相应问题。
(3)M的化学式是
(4)将充分反应后的混合物过滤,检验滤液中金属阳离子的方法及现象为
(5)将滤渣加入浓盐酸中加热,产生黄绿色气体,该反应的离子方程式为
您最近一年使用:0次
名校
4 . 某磁铁矿石A的主要成分是磁性氧化铁(Fe3O4),还含少量的Al2O3、Cu2O。某工厂利用此矿石进行有关物质的回收利用,其中溶液F的溶质为常见的补铁剂,工艺流程如图(已知Cu2O不溶于水和碱,但溶于强酸:Cu2O+2H+=Cu+Cu2++H2O)。根据流程回答下列问题:___________ 。
(2)溶液D中含有的金属阳离子有___________ 。试剂X为___________ ,固体E为___________ 。
(3)操作1的名称为___________ 。
(4)在溶液F中滴加NaOH溶液的现象是___________ 。
(5)已知E为红色固体,写出证明E中无Cu2O的方法:___________ (写出实验操作与现象)。
(6)工业废水中含有的 (酸性条件存在)常利用溶液F将其还原为Cr3+,以便后续沉淀除去,写出该氧化还原反应的离子方程式:
(酸性条件存在)常利用溶液F将其还原为Cr3+,以便后续沉淀除去,写出该氧化还原反应的离子方程式:___________ 。

(2)溶液D中含有的金属阳离子有
(3)操作1的名称为
(4)在溶液F中滴加NaOH溶液的现象是
(5)已知E为红色固体,写出证明E中无Cu2O的方法:
(6)工业废水中含有的
 (酸性条件存在)常利用溶液F将其还原为Cr3+,以便后续沉淀除去,写出该氧化还原反应的离子方程式:
(酸性条件存在)常利用溶液F将其还原为Cr3+,以便后续沉淀除去,写出该氧化还原反应的离子方程式:
您最近一年使用:0次
名校
解题方法
5 . 把3.0 mol·L−1 CuSO4溶液和1.0 mol·L−1 Fe2(SO4)3溶液等体积混合(假设混合后液体的体积等于混合前两种溶液的体积之和),向溶液中加入足量铁粉,经足够长的时间后,铁粉有剩余。此时溶液中Fe2+的物质的量浓度为
| A.3.0 mol· L −1 | B.2.5 mol· L −1 | C.2.0mol· L −1 | D.1.0 mol· L −1 |
您最近一年使用:0次
名校
解题方法
6 . 对下列图像与相关陈述对应的是
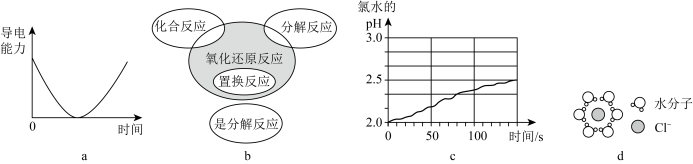
| A.图a:向稀硫酸中逐滴加入BaCl2溶液,混合液导电能力随时间变化的曲线 |
| B.图b:8Al+3Fe3O4 = 4Al2O3+9Fe的反应类型属于图中阴影部分 |
| C.图c:光照过程中氯水的pH随时间变化的曲线 |
| D.图d:NaCl固体溶解形成的水合氯离子示意图 |
您最近一年使用:0次
名校
解题方法
7 . 下列离子反应方程式正确的是
A.氯气通入冷的石灰乳: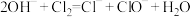 |
B.向NaHCO3溶液中滴入少量澄清石灰水: |
C.向明矾溶液中滴加Ba(OH)2溶液到 恰好完全沉淀时: 恰好完全沉淀时: |
| D.向FeI2溶液中通入少量氯气:Cl2 + 2I- = 2Cl- + I2 |
您最近一年使用:0次
名校
8 . 一定条件下,氨气和氟气发生反应:4NH3+3F2 =NF3 +3NH4F,其中产物NF3分子结构和NH3相似。下列有关说法错误的是
| A.NF3分子含有极性共价键 | B.NF3中原子均达8电子稳定结构 |
| C.氧化剂与还原剂物质的量之比 3:4 | D.NH4F中既有离子键又有极性键 |
您最近一年使用:0次
名校
解题方法
9 . 下列各组离子在给定条件的溶液中一定能大量共存的是
A.在强酸性溶液中: 、 、 、 、 、MnO 、MnO |
B.加入铝粉有大量氢气产生的溶液中: 、Mg2+、SO 、Mg2+、SO 、NO 、NO |
C.酸性溶液中:Fe3+ 、I-、  、 、 |
D.滴入酚酞显红色的溶液中: 、Cs+、CH3COO-、Cl- 、Cs+、CH3COO-、Cl- |
您最近一年使用:0次
名校
10 . 下列实验中,所使用的装置(夹持装置略)、试剂和操作方法都正确的是
|
|
|
|
| A.配制一定浓度的稀硫酸 | B.观察Fe(OH)2的生成 | C.除去Fe(OH)3胶体中的FeCl3 | D.检验草木灰中含 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次