1 . 氯化亚铜(CuCl)广泛应用于有机合成,难溶于水和乙醇,在潮湿空气中易氧化和水解。某学习小组探究CuCl的制备并测定纯度。回答下列问题:
已知:①
②某些含铜化合物和离子在水中的颜色和状态如下表:
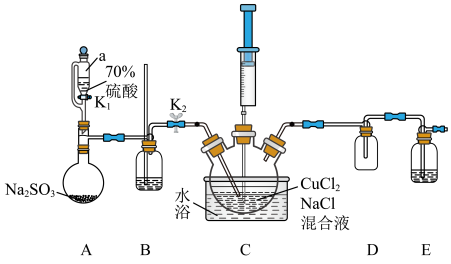
Ⅰ.组装仪器,检查装置气密性,添加药品;
Ⅱ.水浴加热三颈烧瓶,打开K1、K2;
Ⅲ.待三颈烧瓶中溶液由黄绿色变为无色,关闭K1、K2;
Ⅳ.通过注射器向三颈烧瓶中加入水,生成白色沉淀,一段时间后部分沉淀变为棕红色。
(1)仪器a的名称为___________ ;B的作用为___________ (答出一点即可)。
(2)步骤Ⅲ反应的离子方程式为___________ 。
(3)步骤Ⅳ中,沉淀由白色转化为棕红色的原因___________ 。
(4)为防止生成棕红色固体,还需在原步骤Ⅰ中通过注射器往三颈烧瓶中加入一定量___________ (药品名称),再按上述步骤进行实验即可。
(5)产品先快速水洗后再醇洗,醇洗的目的为___________ 。
(6)测定CuCl产品纯度:将10.00 g产品溶于硝酸,配成250 mL溶液,取25.00 mL,加20.00 mL 0.5000 mol/L AgNO3溶液,充分反应后,加少量硝基苯覆盖沉淀。NH4Fe(SO4)2溶液作指示剂,用0.1000mol/L NH4SCN标准溶液滴定过量的AgNO3溶液,平行实验三次,平均消耗NH4SCN溶液10.00 mL。产品的纯度为___________ ,若未加入硝基苯会导致测定结果___________ (填“偏高”或“偏低”或“无影响”)。
[已知: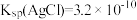 ,
,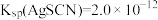 ]。
]。
已知:①

②某些含铜化合物和离子在水中的颜色和状态如下表:
| 化合物或离子 | CuCl | [CuCl4]2- | [CuCl3]2- | CuOH | Cu2O |
| 颜色和状态 | 白色沉淀 | 黄绿色溶液 | 无色溶液 | 黄色沉淀 | 棕红色沉淀 |
Ⅰ.组装仪器,检查装置气密性,添加药品;
Ⅱ.水浴加热三颈烧瓶,打开K1、K2;
Ⅲ.待三颈烧瓶中溶液由黄绿色变为无色,关闭K1、K2;
Ⅳ.通过注射器向三颈烧瓶中加入水,生成白色沉淀,一段时间后部分沉淀变为棕红色。
(1)仪器a的名称为
(2)步骤Ⅲ反应的离子方程式为
(3)步骤Ⅳ中,沉淀由白色转化为棕红色的原因
(4)为防止生成棕红色固体,还需在原步骤Ⅰ中通过注射器往三颈烧瓶中加入一定量
(5)产品先快速水洗后再醇洗,醇洗的目的为
(6)测定CuCl产品纯度:将10.00 g产品溶于硝酸,配成250 mL溶液,取25.00 mL,加20.00 mL 0.5000 mol/L AgNO3溶液,充分反应后,加少量硝基苯覆盖沉淀。NH4Fe(SO4)2溶液作指示剂,用0.1000mol/L NH4SCN标准溶液滴定过量的AgNO3溶液,平行实验三次,平均消耗NH4SCN溶液10.00 mL。产品的纯度为
[已知:
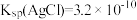 ,
,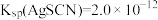 ]。
]。
您最近一年使用:0次
2 . 某小组在实验室模拟侯氏制碱工艺制备 ,装置如图所示(夹持装置略去),下列离子方程式错误的是
,装置如图所示(夹持装置略去),下列离子方程式错误的是
 ,装置如图所示(夹持装置略去),下列离子方程式错误的是
,装置如图所示(夹持装置略去),下列离子方程式错误的是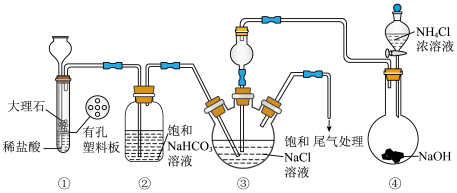
A.①中: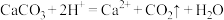 | B.②中: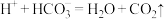 |
C.③中: | D.④中: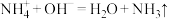 |
您最近一年使用:0次
3 . 硼氢化钠可作还原剂,与水反应的化学方程式为 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.3.8g 固体中含有的离子数为0.2 固体中含有的离子数为0.2 |
B.pH=7的纯水中含有的 数为 数为 |
C.0.1 mol 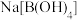 中含有的 中含有的 键数为0.4 键数为0.4 |
D.生成22.4L(已折算成标准状况)的 时,转移的电子数为2 时,转移的电子数为2 |
您最近一年使用:0次
2024·浙江宁波·二模
4 . 下列化学反应与方程式相符的是
A.氢氧化钠溶液中加入过量草酸: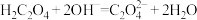 |
B.碱性条件下,氢氧化铁与次氯酸钠溶液反应制备高铁酸钠 : :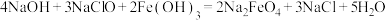 |
C.工业制取高纯硅: |
D.尿素与甲醛反应生成某线型脲醛树脂: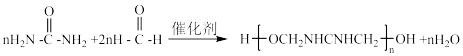 |
您最近一年使用:0次
解题方法
5 . 下列说法中不正确的是
| A.书写共价化合物的电子式只需把结构式中的一个单键改成一对电子即可 |
B.已知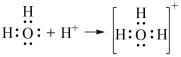 ,可见,成键的一方不提供电子也可能形成化学键 ,可见,成键的一方不提供电子也可能形成化学键 |
| C.某种化合物溶于水导电,不能说明这种化合物是离子化合物 |
D. 、 、 分子中每个原子最外层均满足8电子结构 分子中每个原子最外层均满足8电子结构 |
您最近一年使用:0次
名校
6 . 某实验小组探究 的制取、性质及其应用。按要求回答下列问题。
的制取、性质及其应用。按要求回答下列问题。
已知:① 是难溶于水的白色固体 ②
是难溶于水的白色固体 ② (无色)
(无色)
【实验ⅰ】探究 的制取(如下图所示装置,夹持装置略)
的制取(如下图所示装置,夹持装置略) 溶液(
溶液( )中通入
)中通入 一段时间,至C中溶液的pH为7时向其中滴加一定量
一段时间,至C中溶液的pH为7时向其中滴加一定量 溶液,产生白色沉淀,过滤、洗涤、干燥,得到
溶液,产生白色沉淀,过滤、洗涤、干燥,得到 固体。
固体。
(1)盛装稀盐酸的仪器名称为________ ,试剂a为________ 。
(2)向 溶液中通入
溶液中通入 的目的可能是
的目的可能是________ 。
(3)pH为7时滴加一定量 溶液产生白色沉淀的离子方程式为
溶液产生白色沉淀的离子方程式为________ 。
(4)同学甲在C中出现白色沉淀之后继续通 ,阐述你认为同学甲的操作合理与否及理由
,阐述你认为同学甲的操作合理与否及理由________ 。
【实验ⅱ和实验ⅲ】探究 的性质
的性质 ,请写出步骤②反应的离子方程式:
,请写出步骤②反应的离子方程式:_________ 。
(6)对比实验ⅱ和实验ⅲ,得出实验结论(填1点即可):_________ 。
【实验ⅳ】探究 的应用
的应用
(7)将 溶于乳酸
溶于乳酸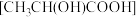 中制得可溶性的乳酸亚铁补血剂。同学乙用酸性
中制得可溶性的乳酸亚铁补血剂。同学乙用酸性 测定该补血剂中亚铁含量,再计算乳酸亚铁的质量分数。发现乳酸亚铁的质量分数总是大于100%(操作误差略),其原因是
测定该补血剂中亚铁含量,再计算乳酸亚铁的质量分数。发现乳酸亚铁的质量分数总是大于100%(操作误差略),其原因是________ 。
 的制取、性质及其应用。按要求回答下列问题。
的制取、性质及其应用。按要求回答下列问题。已知:①
 是难溶于水的白色固体 ②
是难溶于水的白色固体 ② (无色)
(无色)【实验ⅰ】探究
 的制取(如下图所示装置,夹持装置略)
的制取(如下图所示装置,夹持装置略)实验i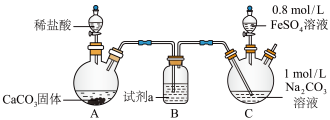
 溶液(
溶液( )中通入
)中通入 一段时间,至C中溶液的pH为7时向其中滴加一定量
一段时间,至C中溶液的pH为7时向其中滴加一定量 溶液,产生白色沉淀,过滤、洗涤、干燥,得到
溶液,产生白色沉淀,过滤、洗涤、干燥,得到 固体。
固体。(1)盛装稀盐酸的仪器名称为
(2)向
 溶液中通入
溶液中通入 的目的可能是
的目的可能是(3)pH为7时滴加一定量
 溶液产生白色沉淀的离子方程式为
溶液产生白色沉淀的离子方程式为(4)同学甲在C中出现白色沉淀之后继续通
 ,阐述你认为同学甲的操作合理与否及理由
,阐述你认为同学甲的操作合理与否及理由【实验ⅱ和实验ⅲ】探究
 的性质
的性质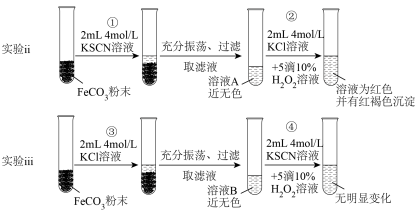
 ,请写出步骤②反应的离子方程式:
,请写出步骤②反应的离子方程式:(6)对比实验ⅱ和实验ⅲ,得出实验结论(填1点即可):
【实验ⅳ】探究
 的应用
的应用(7)将
 溶于乳酸
溶于乳酸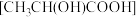 中制得可溶性的乳酸亚铁补血剂。同学乙用酸性
中制得可溶性的乳酸亚铁补血剂。同学乙用酸性 测定该补血剂中亚铁含量,再计算乳酸亚铁的质量分数。发现乳酸亚铁的质量分数总是大于100%(操作误差略),其原因是
测定该补血剂中亚铁含量,再计算乳酸亚铁的质量分数。发现乳酸亚铁的质量分数总是大于100%(操作误差略),其原因是
您最近一年使用:0次
7 . 酸浸法回收废炉渣中(主要为铜、钴、镍、铁等金属元素的氧化物)的铜、钴、镍的流程如下: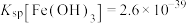 ,
, .
.
(1)“磨细”过程的目的是____________ .
(2)酸浸液中大量铁元素以 存在,加入
存在,加入 可减少铁屑的消耗从而降低成本,
可减少铁屑的消耗从而降低成本, 与
与 反应过程中会产生气泡,其离子方程式为
反应过程中会产生气泡,其离子方程式为____________ .
(3)“滤渣2”主要成分为______ (填化学式)。
(4)“镍钴分离”过程 发生反应的离子方程式为
发生反应的离子方程式为____________ .
(5)“酸溶1”过程用 替换HCl,从绿色化学角度分析其可行性
替换HCl,从绿色化学角度分析其可行性____________ 。
(6)“焙烧”过程发生反应的化学方程式为____________ 。
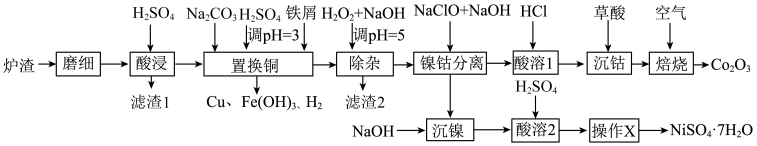
(7)已知当 mol⋅L
mol⋅L 时,认为其沉淀完全。“沉镍”过程的目的是为了将
时,认为其沉淀完全。“沉镍”过程的目的是为了将 .此时应调节溶液的pH为
.此时应调节溶液的pH为______ 。
(8)“操作X”采用的结晶方法为______ 。
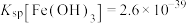 ,
, .
.(1)“磨细”过程的目的是
(2)酸浸液中大量铁元素以
 存在,加入
存在,加入 可减少铁屑的消耗从而降低成本,
可减少铁屑的消耗从而降低成本, 与
与 反应过程中会产生气泡,其离子方程式为
反应过程中会产生气泡,其离子方程式为(3)“滤渣2”主要成分为
(4)“镍钴分离”过程
 发生反应的离子方程式为
发生反应的离子方程式为(5)“酸溶1”过程用
 替换HCl,从绿色化学角度分析其可行性
替换HCl,从绿色化学角度分析其可行性(6)“焙烧”过程发生反应的化学方程式为
(7)已知当
 mol⋅L
mol⋅L 时,认为其沉淀完全。“沉镍”过程的目的是为了将
时,认为其沉淀完全。“沉镍”过程的目的是为了将 .此时应调节溶液的pH为
.此时应调节溶液的pH为(8)“操作X”采用的结晶方法为
您最近一年使用:0次
名校
8 . 下列叙述正确的是
| A.物质只有气、液、固三种聚集状态 |
| B.液体与晶体混合物叫液晶 |
| C.超分子内部分子之间通过价键、氢键、静电作用,疏水作用,弱配位键相结合 |
| D.晶体有固定熔点、沸点,非晶体没有固定熔点、沸点 |
您最近一年使用:0次
9 . 下列相关微粒的说法正确的是
A.H2O的电子式: | B.中子数为20的氯原子: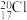 |
C.Na+的结构示意图: | D. 的空间构型为平面三角形 的空间构型为平面三角形 |
您最近一年使用:0次
名校
解题方法
10 . 2.48g铁铜合金完全溶解于80mL 4.0 稀硝酸中,得到标准状况下672mL NO气体(假设此时无其他气体产生),下列说法正确的是
稀硝酸中,得到标准状况下672mL NO气体(假设此时无其他气体产生),下列说法正确的是
 稀硝酸中,得到标准状况下672mL NO气体(假设此时无其他气体产生),下列说法正确的是
稀硝酸中,得到标准状况下672mL NO气体(假设此时无其他气体产生),下列说法正确的是A.反应后溶液中不存在 |
| B.该合金中铁与铜的物质的量之比是1∶2 |
C.反应后溶液(忽略溶液体积变化)中 |
D.向反应后的溶液中加入2.0 NaOH溶液至金属离子恰好全部沉淀时,需加入NaOH溶液的体积是120mL NaOH溶液至金属离子恰好全部沉淀时,需加入NaOH溶液的体积是120mL |
您最近一年使用:0次



