名校
解题方法
1 . 下列离子方程式书写的正确的是
A.向 溶液中加入适量 溶液中加入适量 : : |
B.食醋去除水垢中的 : :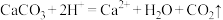 |
C.过量 通入NaClO溶液中: 通入NaClO溶液中: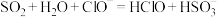 |
D.向氯化铵的溶液中加入热的浓NaOH: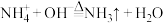 |
您最近一年使用:0次
名校
解题方法
2 . 离子化合物 和
和 与水的反应分别为①
与水的反应分别为①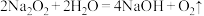 ;②
;②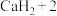
 。下列说法正确的是
。下列说法正确的是
 和
和 与水的反应分别为①
与水的反应分别为①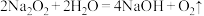 ;②
;②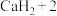
 。下列说法正确的是
。下列说法正确的是A. 、 、 中均有离子键和共价键 中均有离子键和共价键 |
| B.①中水发生氧化反应,②中水发生还原反应 |
C. 中阴、阳离子个数比为1∶2, 中阴、阳离子个数比为1∶2, 中阴、阳离子个数比为2∶1 中阴、阳离子个数比为2∶1 |
D.当反应①和②中转移的电子数相同时,产生的 和 和 的物质的量相同 的物质的量相同 |
您最近一年使用:0次
3 . 用 表示阿伏加德罗常数的值。下列叙述正确的是
表示阿伏加德罗常数的值。下列叙述正确的是
 表示阿伏加德罗常数的值。下列叙述正确的是
表示阿伏加德罗常数的值。下列叙述正确的是A.2.24L(标准状况)苯在 中完全燃烧,得到0.6 中完全燃烧,得到0.6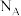 个 个 分子 分子 |
B.1mol乙烯分子中含有的碳氢键数为6 |
C.1.2g Mg在空气中完全燃烧生成MgO和 ,转移电子数为0.1 ,转移电子数为0.1 |
D.含0.2mol HCl的浓盐酸与足量 反应,生成 反应,生成 的数为0.1 的数为0.1 |
您最近一年使用:0次
名校
解题方法
4 . 下列化学用语正确的是
A.中子数为8的氧原子: | B.甲烷的空间填充模型: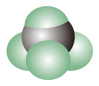 |
C.NaOH的电子式: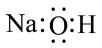 | D.氟离子( )的结构示意图: )的结构示意图: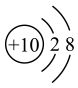 |
您最近一年使用:0次
名校
5 . 门捷列夫在研究周期表时预言了“类硅”元素锗和“类铝”元素镓等11种元素。锗及其化合物应用于航空航天测控、光纤通讯等领域。一种提纯二氧化锗粗品(主要含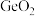 、
、 )的工艺如下:
)的工艺如下: 与碱反应生成
与碱反应生成 ;
; 与碱反应生成
与碱反应生成 。
。
ii. 极易水解生成
极易水解生成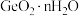 ;
; 沸点
沸点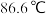 。
。
(1) 位于同主族
位于同主族 的下一周期,
的下一周期, 在周期表中的位置是
在周期表中的位置是___________ 。
(2)从原子结构角度解释金属性 比
比 强的原因
强的原因___________ 。
(3)“氧化”过程是将 氧化为
氧化为 ,其离子方程式为
,其离子方程式为___________ 。
(4)加盐酸蒸馏生成 ,生成
,生成 的化学方程式为
的化学方程式为___________ 。
(5)高纯二氧化锗的含量常采用碘酸钾 滴定法进行测定。碘酸钾
滴定法进行测定。碘酸钾 与碘化钾(KI)在酸性情况下会生成使淀粉变蓝的碘单质。配平离子方程式
与碘化钾(KI)在酸性情况下会生成使淀粉变蓝的碘单质。配平离子方程式___________ 。

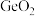 、
、 )的工艺如下:
)的工艺如下: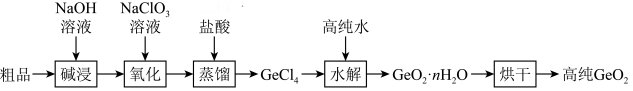
 与碱反应生成
与碱反应生成 ;
; 与碱反应生成
与碱反应生成 。
。ii.
 极易水解生成
极易水解生成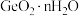 ;
; 沸点
沸点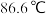 。
。(1)
 位于同主族
位于同主族 的下一周期,
的下一周期, 在周期表中的位置是
在周期表中的位置是(2)从原子结构角度解释金属性
 比
比 强的原因
强的原因(3)“氧化”过程是将
 氧化为
氧化为 ,其离子方程式为
,其离子方程式为(4)加盐酸蒸馏生成
 ,生成
,生成 的化学方程式为
的化学方程式为(5)高纯二氧化锗的含量常采用碘酸钾
 滴定法进行测定。碘酸钾
滴定法进行测定。碘酸钾 与碘化钾(KI)在酸性情况下会生成使淀粉变蓝的碘单质。配平离子方程式
与碘化钾(KI)在酸性情况下会生成使淀粉变蓝的碘单质。配平离子方程式
您最近一年使用:0次
名校
6 . 如图是部分短周期主族元素原子半径与原子序数的关系图。
(1)写出A在元素周期表中的位置___________ 。比较Z、Q两种元素的简单离子半径大小___________ ;M的原子结构示意图为___________ 。
(2)图中最活泼的金属是___________ ,将其单质在氧气中加热,生成的产物为___________ 。
该元素的最高价氧化物对应的水化物与L的最高价氧化物对应的水化物发生反应的离子方程式为___________ 。
(3)比较X、R两种元素的简单气态氢化物的沸点高低___________ ;B的氢化物在常温下跟该元素的最高价氧化物对应的水化物发生反应生成的物质的化学式___________ 。
(4)最高价氧化物的水化物中酸性最强的是___________ 。(填化学式)
(5)用一个化学方程式证明X单质氧化性比Q的强:___________ 。

(1)写出A在元素周期表中的位置
(2)图中最活泼的金属是
该元素的最高价氧化物对应的水化物与L的最高价氧化物对应的水化物发生反应的离子方程式为
(3)比较X、R两种元素的简单气态氢化物的沸点高低
(4)最高价氧化物的水化物中酸性最强的是
(5)用一个化学方程式证明X单质氧化性比Q的强:
您最近一年使用:0次
名校
7 . 下列化学用语表述正确的是
A.Na+的结构示意图: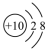 | B.中子数为8的氮原子: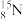 |
C.二氧化碳分子结构模型: | D.NH4Br的电子式: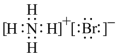 |
您最近一年使用:0次
名校
8 . 如图是四种常见有机物的球棍模型示意图。下列说法不正确的是
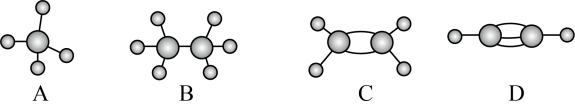
| A.A与Cl2在光照条件下发生反应得到的有机物是混合物 |
| B.B不能使酸性高锰酸钾溶液褪色 |
| C.C分子中所有原子都在同一平面 |
| D.D最多能与1molBr2发生加成反应 |
您最近一年使用:0次
名校
9 . 在100mL混合液中,HNO3和H2SO4的物质的量浓度分别为0.4mol·L-1,0.1mol·L-1,向该混合液中加入1.92g铜粉,加热,待充分反应后,所得溶液中Cu2+的物质的量浓度(mol·L-1)是
| A.0.15 | B.0.45 | C.0.3 | D.0.225 |
您最近一年使用:0次
名校
10 . 下列有关离子(或物质)的检验、现象及结论,都正确的是
| A.向某溶液中滴加氯水,再滴加KSCN溶液,溶液变成红色,该溶液中一定含有Fe2+ |
| B.向某溶液中滴加KSCN溶液,溶液变成红色,该溶液中一定不存在Fe2+ |
| C.将某种铁的氧化物溶于足量的稀硫酸中,取其溶液滴加酸性KMnO4溶液,振荡,溶液褪色,原氧化物中含有+2价铁 |
| D.向久置的FeCl2溶液中滴入用硫酸酸化的H2O2溶液,溶液变黄,滴加KSCN溶液,溶液变成红色,说明发生氧化还原反应,且氧化性:H2O2<Fe3+ |
您最近一年使用:0次



