解题方法
1 . 我国科学家研究发现,使用GaZrOx双金属氧化物可形成氧空位,具有催化氧化性能,实现CO2加氢制甲醇(MT)。Zr基态原子核外价电子排布式为4d25s2。下列说法错误的是

| A.步骤a到b有极性键的断裂与形成 |
| B.氧空位越多越有利于加快速率 |
| C.步骤(2)Zr(Ⅲ)将电子转移给CO2形成Zr(Ⅱ),起到活化CO2的作用 |
| D.步骤(4)可制得甲醇 |
您最近一年使用:0次
解题方法
2 . 下列各组离子能大量共存,且加入相应试剂后发生反应的离子方程式正确的是
| 选项 | 离子组 | 加入试剂 | 加入试剂后发生的离子反应 |
| A |  、 、 、 、 |  溶液 溶液 |  |
| B |  、 、 、 、 | 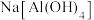 溶液 溶液 | 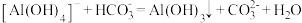 |
| C |  、 、 、 、 | 通入少量 | 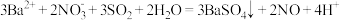 |
| D |  、 、 、 、 | 通入过量 | 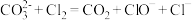 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 乙醛与新制 悬浊液发生反应:
悬浊液发生反应: ,设
,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 悬浊液发生反应:
悬浊液发生反应: ,设
,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 中含 中含 键数目为 键数目为 |
B.标准状况下,消耗 时,转移电子的数目为 时,转移电子的数目为 |
C. 溶液中含有的 溶液中含有的 数目小于 数目小于 |
D.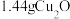 含有的质子数为 含有的质子数为 |
您最近一年使用:0次
4 . 松花蛋(皮蛋)是一种用禽蛋加工制成的食品。制作松花蛋的原料泥需要 、食品级金属盐(较常用的是
、食品级金属盐(较常用的是 )等。下列说法错误的是
)等。下列说法错误的是
 、食品级金属盐(较常用的是
、食品级金属盐(较常用的是 )等。下列说法错误的是
)等。下列说法错误的是| A.蛋黄成分中的油脂是天然高分子 |
B.蛋清遇 会聚沉,这个过程发生了蛋白质的变性 会聚沉,这个过程发生了蛋白质的变性 |
| C.蛋壳膜可用于提纯、精制胶体 |
D.制作过程中生成的 可以堵住蛋壳的气孔来调节 可以堵住蛋壳的气孔来调节 渗透量 渗透量 |
您最近一年使用:0次
5 . 一种电池的总反应为4Li+2SOCl2=SO2↑+4LiCl+S,设NA为阿伏加德罗常数的值。下列说法错误的是
| A.1molSOCl2中所含的共价键数目为4NA |
| B.每生成1molS,转移2NA个电子 |
| C.标准状况下,22.4LSO2中电子的数目为32NA |
| D.1.0L1.0mol•L-1LiCl溶液中Cl-数目为1.0NA |
您最近一年使用:0次
解题方法
6 . 下列离子方程式正确且能准确解释相应实验现象的是
A.向苯酚钠溶液中通入CO2,溶液变浑浊:2C6H5O-+CO2+H2O=2C6H5OH+CO |
| B.NaClO溶液与FeI2溶液反应,溶液变为红棕色:2ClO-+2Fe2++H2O=2Fe3++2Cl-+2OH- |
| C.向Fe(SCN)3溶液中滴加NaF溶液,红色褪去:Fe3++6F-=[FeF6]3- |
D.向氯水中通入SO2,黄绿色褪去:SO2+Cl2+2H2O=SO +2Cl-+4H+ +2Cl-+4H+ |
您最近一年使用:0次
2024·山东日照·模拟预测
名校
解题方法
7 . 镓、锗都是重要的半导体原材料,利用锌浸出渣(主要成分有ZnO、Ga2O3、GeO2、还有FeO、Fe2O3、Bi2O3等杂质)制备镓和锗的流程如下:
Ⅱ.该工艺条件下,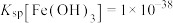 ,
,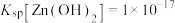
Ⅲ.镓与铝的性质相似,但高纯度的镓难溶于酸或碱。
回答下列问题:
(1)“浸渣”的主要成分为___________ 。
(2)“降铁浓缩”中 为
为 ,则除
,则除 时应控制pH的范围是
时应控制pH的范围是___________ (已知:当溶液中某离子浓度小于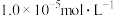 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。
(3)若用H2R表示单宁酸,“沉锗”的反应原理为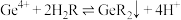 ,该操作中需调节pH为2.5,不能过高或过低,原因是
,该操作中需调节pH为2.5,不能过高或过低,原因是___________ 。
(4)HGaCl4与过量氢氧化钠反应的化学方程式为___________ 。“电解”得到单质镓,阴极的电极反应为___________ 。
(5)步骤①—③目的为___________ ,“还原”过程中参与反应的H2体积为89.6 L(标准状况下),则理论上步骤①中消耗SOCl2物质的量为___________ 。

Ⅱ.该工艺条件下,
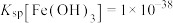 ,
,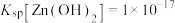
Ⅲ.镓与铝的性质相似,但高纯度的镓难溶于酸或碱。
回答下列问题:
(1)“浸渣”的主要成分为
(2)“降铁浓缩”中
 为
为 ,则除
,则除 时应控制pH的范围是
时应控制pH的范围是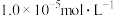 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。(3)若用H2R表示单宁酸,“沉锗”的反应原理为
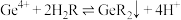 ,该操作中需调节pH为2.5,不能过高或过低,原因是
,该操作中需调节pH为2.5,不能过高或过低,原因是(4)HGaCl4与过量氢氧化钠反应的化学方程式为
(5)步骤①—③目的为
您最近一年使用:0次
2024-05-15更新
|
147次组卷
|
3卷引用:T11-工业流程题
8 . 锆( )是一种重要的战略金属。一种以氧氯化锆(主要含
)是一种重要的战略金属。一种以氧氯化锆(主要含 ,还含有少量
,还含有少量 、
、 等元素)为原料生产金属锆的工艺流程如下:
等元素)为原料生产金属锆的工艺流程如下: 、
、 、
、 ;
;
② 时,
时, ,
, ;
;
③“还原”前后相关物质沸点如下:
回答下列问题:
(1) 是
是 的同族相邻元素,基态
的同族相邻元素,基态 原子的价电子排布式是
原子的价电子排布式是___________ 。
(2) 通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的
通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的 ,再以盐酸酸化得到
,再以盐酸酸化得到 ,写出酸化过程的离子方程式
,写出酸化过程的离子方程式___________ 。
(3)“沉淀”后,废液中 ,则废液中
,则废液中 为
为___________  。
。
(4)“沸腾氯化”时, 转化为
转化为 ,同时生成一种还原性气体,该反应的化学方程式为
,同时生成一种还原性气体,该反应的化学方程式为___________ 。
(5)①气态 通常以二聚体
通常以二聚体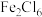 的形式存在,分子结构为
的形式存在,分子结构为 ,二聚体中
,二聚体中 的杂化轨道类型为
的杂化轨道类型为___________ 。 易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为
易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为___________ 。
②“还原”的主要目的是___________ 。
(6)下列金属冶炼方法与本工艺流程中加入 冶炼
冶炼 的方法相似的是___________
的方法相似的是___________
(7)实验室可以用络合滴定法快速测定“酸浸”溶液中锆的含量,步骤如下:___________ ,继续摇动锥形瓶,观察溶液颜色变化。
②已知 与EDTA发生
与EDTA发生 络合反应,则酸浸液中含量(以
络合反应,则酸浸液中含量(以 计)为
计)为___________  。
。
 )是一种重要的战略金属。一种以氧氯化锆(主要含
)是一种重要的战略金属。一种以氧氯化锆(主要含 ,还含有少量
,还含有少量 、
、 等元素)为原料生产金属锆的工艺流程如下:
等元素)为原料生产金属锆的工艺流程如下: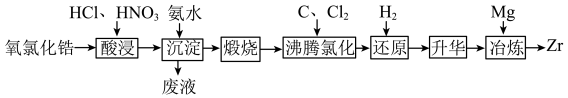
 、
、 、
、 ;
;②
 时,
时, ,
, ;
;③“还原”前后相关物质沸点如下:
| 物质 |  |  |  |  |  |
| 沸点 | 331 | 315 | 1300 | 700 | 1150 |
(1)
 是
是 的同族相邻元素,基态
的同族相邻元素,基态 原子的价电子排布式是
原子的价电子排布式是(2)
 通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的
通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的 ,再以盐酸酸化得到
,再以盐酸酸化得到 ,写出酸化过程的离子方程式
,写出酸化过程的离子方程式(3)“沉淀”后,废液中
 ,则废液中
,则废液中 为
为 。
。(4)“沸腾氯化”时,
 转化为
转化为 ,同时生成一种还原性气体,该反应的化学方程式为
,同时生成一种还原性气体,该反应的化学方程式为(5)①气态
 通常以二聚体
通常以二聚体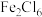 的形式存在,分子结构为
的形式存在,分子结构为 ,二聚体中
,二聚体中 的杂化轨道类型为
的杂化轨道类型为 易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为
易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为②“还原”的主要目的是
(6)下列金属冶炼方法与本工艺流程中加入
 冶炼
冶炼 的方法相似的是___________
的方法相似的是___________| A.高炉炼铁 | B.电解熔融氯化钠制钠 |
| C.铝热反应制锰 | D.氧化汞分解制汞 |
(7)实验室可以用络合滴定法快速测定“酸浸”溶液中锆的含量,步骤如下:

②已知
 与EDTA发生
与EDTA发生 络合反应,则酸浸液中含量(以
络合反应,则酸浸液中含量(以 计)为
计)为 。
。
您最近一年使用:0次
9 . 连二亚硫酸钠 俗称保险粉,是印染工业中常用的漂白剂。实验室制备流程如下:
俗称保险粉,是印染工业中常用的漂白剂。实验室制备流程如下:
 俗称保险粉,是印染工业中常用的漂白剂。实验室制备流程如下:
俗称保险粉,是印染工业中常用的漂白剂。实验室制备流程如下: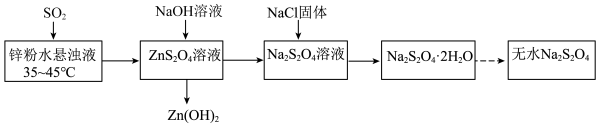
| A.将锌粉溶于水形成悬浊液可以提高反应速率 |
B.生成 的反应中氧化剂和还原剂物质的量之比为 的反应中氧化剂和还原剂物质的量之比为 |
C.温度超过 会导致 会导致 溶解度降低 溶解度降低 |
D.加入 有利于 有利于 析出,提高产率 析出,提高产率 |
您最近一年使用:0次
解题方法
10 . 下列离子方程式书写错误的是
A.向银氨溶液中滴入乙醛: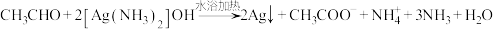 |
B.向硫代硫酸钠溶液中加入稀硫酸: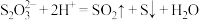 |
C.向漂白粉溶液中通入少量 : :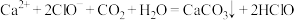 |
D.向加有 的 的 溶液中通入 溶液中通入 : :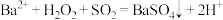 |
您最近一年使用:0次



