1 . 用 与
与 制备纳米零价铁的反应为
制备纳米零价铁的反应为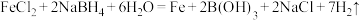 。设
。设 为阿伏伽德罗常数的值,下列说法正确的是
为阿伏伽德罗常数的值,下列说法正确的是
 与
与 制备纳米零价铁的反应为
制备纳米零价铁的反应为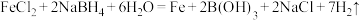 。设
。设 为阿伏伽德罗常数的值,下列说法正确的是
为阿伏伽德罗常数的值,下列说法正确的是A.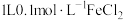 溶液中 溶液中 数为 数为 |
B.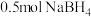 固体中 固体中 键数为 键数为 |
C.每生成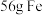 ,转移的电子数为 ,转移的电子数为 |
D. 中采取 中采取 杂化的原子数为 杂化的原子数为 |
您最近一年使用:0次
2 . 锆( )是一种重要的战略金属。一种以氧氯化锆(主要含
)是一种重要的战略金属。一种以氧氯化锆(主要含 ,还含有少量
,还含有少量 、
、 等元素)为原料生产金属锆的工艺流程如下:
等元素)为原料生产金属锆的工艺流程如下: 、
、 、
、 ;
;
② 时,
时, ,
, ;
;
③“还原”前后相关物质沸点如下:
回答下列问题:
(1) 是
是 的同族相邻元素,基态
的同族相邻元素,基态 原子的价电子排布式是
原子的价电子排布式是___________ 。
(2) 通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的
通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的 ,再以盐酸酸化得到
,再以盐酸酸化得到 ,写出酸化过程的离子方程式
,写出酸化过程的离子方程式___________ 。
(3)“沉淀”后,废液中 ,则废液中
,则废液中 为
为___________  。
。
(4)“沸腾氯化”时, 转化为
转化为 ,同时生成一种还原性气体,该反应的化学方程式为
,同时生成一种还原性气体,该反应的化学方程式为___________ 。
(5)①气态 通常以二聚体
通常以二聚体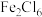 的形式存在,分子结构为
的形式存在,分子结构为 ,二聚体中
,二聚体中 的杂化轨道类型为
的杂化轨道类型为___________ 。 易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为
易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为___________ 。
②“还原”的主要目的是___________ 。
(6)下列金属冶炼方法与本工艺流程中加入 冶炼
冶炼 的方法相似的是___________
的方法相似的是___________
(7)实验室可以用络合滴定法快速测定“酸浸”溶液中锆的含量,步骤如下:___________ ,继续摇动锥形瓶,观察溶液颜色变化。
②已知 与EDTA发生
与EDTA发生 络合反应,则酸浸液中含量(以
络合反应,则酸浸液中含量(以 计)为
计)为___________  。
。
 )是一种重要的战略金属。一种以氧氯化锆(主要含
)是一种重要的战略金属。一种以氧氯化锆(主要含 ,还含有少量
,还含有少量 、
、 等元素)为原料生产金属锆的工艺流程如下:
等元素)为原料生产金属锆的工艺流程如下: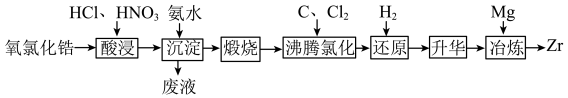
 、
、 、
、 ;
;②
 时,
时, ,
, ;
;③“还原”前后相关物质沸点如下:
| 物质 |  |  |  |  |  |
| 沸点 | 331 | 315 | 1300 | 700 | 1150 |
(1)
 是
是 的同族相邻元素,基态
的同族相邻元素,基态 原子的价电子排布式是
原子的价电子排布式是(2)
 通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的
通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的 ,再以盐酸酸化得到
,再以盐酸酸化得到 ,写出酸化过程的离子方程式
,写出酸化过程的离子方程式(3)“沉淀”后,废液中
 ,则废液中
,则废液中 为
为 。
。(4)“沸腾氯化”时,
 转化为
转化为 ,同时生成一种还原性气体,该反应的化学方程式为
,同时生成一种还原性气体,该反应的化学方程式为(5)①气态
 通常以二聚体
通常以二聚体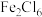 的形式存在,分子结构为
的形式存在,分子结构为 ,二聚体中
,二聚体中 的杂化轨道类型为
的杂化轨道类型为 易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为
易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为②“还原”的主要目的是
(6)下列金属冶炼方法与本工艺流程中加入
 冶炼
冶炼 的方法相似的是___________
的方法相似的是___________| A.高炉炼铁 | B.电解熔融氯化钠制钠 |
| C.铝热反应制锰 | D.氧化汞分解制汞 |
(7)实验室可以用络合滴定法快速测定“酸浸”溶液中锆的含量,步骤如下:

②已知
 与EDTA发生
与EDTA发生 络合反应,则酸浸液中含量(以
络合反应,则酸浸液中含量(以 计)为
计)为 。
。
您最近一年使用:0次
3 . 连二亚硫酸钠 俗称保险粉,是印染工业中常用的漂白剂。实验室制备流程如下:
俗称保险粉,是印染工业中常用的漂白剂。实验室制备流程如下:
 俗称保险粉,是印染工业中常用的漂白剂。实验室制备流程如下:
俗称保险粉,是印染工业中常用的漂白剂。实验室制备流程如下: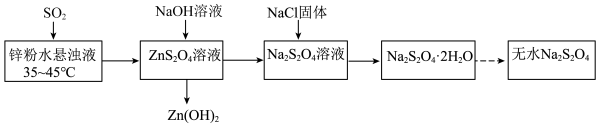
| A.将锌粉溶于水形成悬浊液可以提高反应速率 |
B.生成 的反应中氧化剂和还原剂物质的量之比为 的反应中氧化剂和还原剂物质的量之比为 |
C.温度超过 会导致 会导致 溶解度降低 溶解度降低 |
D.加入 有利于 有利于 析出,提高产率 析出,提高产率 |
您最近一年使用:0次
解题方法
4 . 下列离子方程式书写错误的是
A.向银氨溶液中滴入乙醛: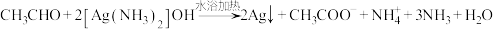 |
B.向硫代硫酸钠溶液中加入稀硫酸: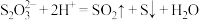 |
C.向漂白粉溶液中通入少量 : :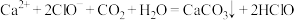 |
D.向加有 的 的 溶液中通入 溶液中通入 : :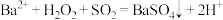 |
您最近一年使用:0次
解题方法
5 . 下列说法中不正确的是
| A.书写共价化合物的电子式只需把结构式中的一个单键改成一对电子即可 |
B.已知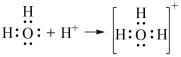 ,可见,成键的一方不提供电子也可能形成化学键 ,可见,成键的一方不提供电子也可能形成化学键 |
| C.某种化合物溶于水导电,不能说明这种化合物是离子化合物 |
D. 、 、 分子中每个原子最外层均满足8电子结构 分子中每个原子最外层均满足8电子结构 |
您最近一年使用:0次
解题方法
6 . 下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白(涉及表中元素一律用对应化学符号表示):
(1)在这些元素中,化学性质最不活泼的是:_____________ (填具体元素符号,下同),原子结构示意图为_____________ 。元素⑩名称为_____________ ,在周期表中的位置_________________ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是_________________ ,碱性最强的化合物的电子式是:_________________________ 。
(3)用电子式表示元素②的常见单质_____________ 其结构式为_________________ 。
(4)表示①与⑦的化合物的电子式为_________________ ,该化合物是由_____________ (填“极性”、“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的简单离子,离子半径由大到小的顺序是_________ 。
(6)元素③的简单氢化物的结构式为_____________________ ;该氢化物常温下和元素⑦的单质反应的化学方程式为 _____________________ 。
| 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)用电子式表示元素②的常见单质
(4)表示①与⑦的化合物的电子式为
(5)③、⑥、⑦三种元素形成的简单离子,离子半径由大到小的顺序是
(6)元素③的简单氢化物的结构式为
您最近一年使用:0次
7 . 分类是科学研究的重要方法,下列物质分类不正确的是
A.酸性氧化物: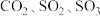 | B.强电解质: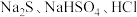 |
C.共价化合物: | D.离子化合物: |
您最近一年使用:0次
8 . 化学学科需要借助化学专用语言描述,下列有关化学用语描述正确的是
A.二氧化硅的分子式为 | B.质子数为92,中子数为143的铀原子: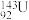 |
C.乙烯的球棍模型: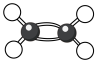 | D. 的电子式: 的电子式: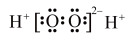 |
您最近一年使用:0次
9 . 化学与人类生产、生活密切相关,利用所学知识进行填空(用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(1)下列物质能导电且属于电解质的是___________(填字母)。
(2)NaH可在野外作生氢剂,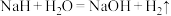 ,该反应中氧化产物和还原产物的质量比为
,该反应中氧化产物和还原产物的质量比为___________ 。
(3)标准状况下,44.8L 对应的物质的量是
对应的物质的量是___________ ,含有的化学键类型为___________ 键(填共价键或离子键)。 电子式为:
电子式为:___________ ,CaF2的电子式为:___________ 。
(4)氮的氧化物是大气污染的主要污染物之一,对人类危害很大,每天行驶的汽车排放的尾气中就含有大量的氮氧化物。标准状况下,将盛满二氧化氮的大试管倒扣在盛水的水槽中,充分吸收后,其反应的的化学方程式是___________ ,试管内溶液的物质的量浓度是___________ 。
 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。(1)下列物质能导电且属于电解质的是___________(填字母)。
| A.氯化钠固体 | B.熔融的氯化钠 | C.氯化钠溶液 | D.钠 |
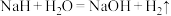 ,该反应中氧化产物和还原产物的质量比为
,该反应中氧化产物和还原产物的质量比为(3)标准状况下,44.8L
 对应的物质的量是
对应的物质的量是 电子式为:
电子式为:(4)氮的氧化物是大气污染的主要污染物之一,对人类危害很大,每天行驶的汽车排放的尾气中就含有大量的氮氧化物。标准状况下,将盛满二氧化氮的大试管倒扣在盛水的水槽中,充分吸收后,其反应的的化学方程式是
您最近一年使用:0次
10 . 液氨与CS2在加热条件下可发生反应生成NH4HS和NH4SCN。NA为阿伏加德罗常数的值,下列说法错误的是
| A.2 g ND3与CS2的混合物中,中子数为NA |
| B.工业合成氨中每生成1 mol NH3,转移的电子数为3NA |
| C.1 L0.1 mol/LNH4HS溶液中,氢原子数为0.5NA |
| D.1 mol NH4SCN晶体中,σ键数目为6NA |
您最近一年使用:0次



