1 . 化学是一门以实验为基础的自然科学。根据题意回答下列问题:
(1)在 溶液中逐滴滴入
溶液中逐滴滴入 溶液,观察到
溶液,观察到___________ (填“蓝色”或“红色”)的沉淀。
(2)铜和浓硫酸在加热时反应,产生无色刺激性气味的气体___________ (填化学式),能漂白___________ (填“蓝色”或“红色”)品红溶液。
(3)铜和浓硝酸反应剧烈,产生红棕色气体,离子方程式为___________ ;铜和稀硝酸反应缓慢,化学方程式为___________ ;对比现象可以说明浓硝酸的氧化性比稀硝酸___________ (填“强”或“弱”)。
(1)在
 溶液中逐滴滴入
溶液中逐滴滴入 溶液,观察到
溶液,观察到(2)铜和浓硫酸在加热时反应,产生无色刺激性气味的气体
(3)铜和浓硝酸反应剧烈,产生红棕色气体,离子方程式为
您最近一年使用:0次
2 . 下列各组离子能大量共存的是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
3 . 对于下列实验,能正确描述的离子方程式是
A.铁和足量的稀硝酸反应: |
B.向 溶液中滴加稀盐酸: 溶液中滴加稀盐酸: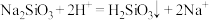 |
C.硅酸钠溶液与醋酸溶液混合: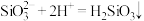 |
D. 溶液与 溶液与 溶液混合: 溶液混合: |
您最近一年使用:0次
4 . 设 为阿伏加德罗常数的值,下列判断正确的是
为阿伏加德罗常数的值,下列判断正确的是
 为阿伏加德罗常数的值,下列判断正确的是
为阿伏加德罗常数的值,下列判断正确的是A. 个NO分子的体积为 个NO分子的体积为 |
B.标准状况下,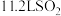 所含的原子数为 所含的原子数为 |
C. 与足量硝酸充分反应转移的电子数为 与足量硝酸充分反应转移的电子数为 |
D.含 个 个 分子的浓硫酸与足量铜反应可制得 分子的浓硫酸与足量铜反应可制得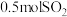 |
您最近一年使用:0次
解题方法
5 . 近年来科学家提出一种新型 减排方式,利用光致热催化还原
减排方式,利用光致热催化还原 制备含碳化合物。催化剂吸收太阳光转化为热能,光生电子和热电子转移到催化剂表面的活性位点与
制备含碳化合物。催化剂吸收太阳光转化为热能,光生电子和热电子转移到催化剂表面的活性位点与 反应。下图为
反应。下图为 还原为HCOOH或CO的可能反应路径。
还原为HCOOH或CO的可能反应路径。
 减排方式,利用光致热催化还原
减排方式,利用光致热催化还原 制备含碳化合物。催化剂吸收太阳光转化为热能,光生电子和热电子转移到催化剂表面的活性位点与
制备含碳化合物。催化剂吸收太阳光转化为热能,光生电子和热电子转移到催化剂表面的活性位点与 反应。下图为
反应。下图为 还原为HCOOH或CO的可能反应路径。
还原为HCOOH或CO的可能反应路径。路径①:
路径②:
A.路径①中 中心碳原子杂化方式由 中心碳原子杂化方式由 转变为 转变为 |
| B.路径②中第一步未发生氧化还原反应 |
C.路径①和②可看出 的吸附模式会影响 的吸附模式会影响 和 和 的选择性 的选择性 |
D.路径②中每生成 ,反应共转移 ,反应共转移 ,同时产生 ,同时产生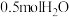 |
您最近一年使用:0次
6 . 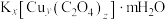 是一种重要的化工原料,其制备及各微粒的测定原理如下:
是一种重要的化工原料,其制备及各微粒的测定原理如下:
 .实验方法:称取
.实验方法:称取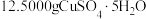 和
和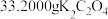 分别溶于水中,在85~90℃下混合浓缩,然后冷却到10℃,并将所得的沉淀减压过滤,迅速加以洗涤,烘干,晶体产率为60%。
分别溶于水中,在85~90℃下混合浓缩,然后冷却到10℃,并将所得的沉淀减压过滤,迅速加以洗涤,烘干,晶体产率为60%。
 .重量法测定配合物中结晶水含量
.重量法测定配合物中结晶水含量
将 配合物称重18.9000g于150℃下恒温2h,取出称量,反复几次,恒温称重,直到重量不再变化,称得重量为16.7400g。
配合物称重18.9000g于150℃下恒温2h,取出称量,反复几次,恒温称重,直到重量不再变化,称得重量为16.7400g。
 .配合物中
.配合物中 及
及 含量
含量
将 中的剩余固体先用1mol/L的
中的剩余固体先用1mol/L的 将其溶解配成250ml溶液,取25ml用酸性
将其溶解配成250ml溶液,取25ml用酸性 标准溶液滴定溶液中的
标准溶液滴定溶液中的 ,消耗
,消耗 0.0048mol;滴定后的溶液中铜以
0.0048mol;滴定后的溶液中铜以 形式存在,通过控制溶液酸度,用间接碘法测定配合物中铜的含量
形式存在,通过控制溶液酸度,用间接碘法测定配合物中铜的含量
回答下列问题:
(1)该配合物的配体及配位原子分别是___________ 、___________ 。
(2)本实验减压过滤所需的主要仪器有抽气泵、吸滤瓶及___________ 、___________ 。
(3)根据题干信息分析步骤 使用的洗涤剂为
使用的洗涤剂为___________ 。
(4)酸性滴定的离子反应方程式为___________ 。
(5)已知: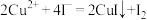 向滴定后的溶液加入足量的KI溶液,用0.6
向滴定后的溶液加入足量的KI溶液,用0.6
 溶液滴定,以淀粉溶液作指示剂,滴定终点的现象为
溶液滴定,以淀粉溶液作指示剂,滴定终点的现象为___________ ;若消耗 溶液的体积为10.00mL。
溶液的体积为10.00mL。 ,步骤
,步骤 中配合物铜的物质的量
中配合物铜的物质的量___________ mol。
(6)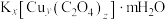 的化学式为:
的化学式为:___________ 。
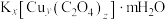 是一种重要的化工原料,其制备及各微粒的测定原理如下:
是一种重要的化工原料,其制备及各微粒的测定原理如下: .实验方法:称取
.实验方法:称取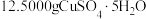 和
和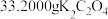 分别溶于水中,在85~90℃下混合浓缩,然后冷却到10℃,并将所得的沉淀减压过滤,迅速加以洗涤,烘干,晶体产率为60%。
分别溶于水中,在85~90℃下混合浓缩,然后冷却到10℃,并将所得的沉淀减压过滤,迅速加以洗涤,烘干,晶体产率为60%。 .重量法测定配合物中结晶水含量
.重量法测定配合物中结晶水含量将
 配合物称重18.9000g于150℃下恒温2h,取出称量,反复几次,恒温称重,直到重量不再变化,称得重量为16.7400g。
配合物称重18.9000g于150℃下恒温2h,取出称量,反复几次,恒温称重,直到重量不再变化,称得重量为16.7400g。 .配合物中
.配合物中 及
及 含量
含量将
 中的剩余固体先用1mol/L的
中的剩余固体先用1mol/L的 将其溶解配成250ml溶液,取25ml用酸性
将其溶解配成250ml溶液,取25ml用酸性 标准溶液滴定溶液中的
标准溶液滴定溶液中的 ,消耗
,消耗 0.0048mol;滴定后的溶液中铜以
0.0048mol;滴定后的溶液中铜以 形式存在,通过控制溶液酸度,用间接碘法测定配合物中铜的含量
形式存在,通过控制溶液酸度,用间接碘法测定配合物中铜的含量回答下列问题:
(1)该配合物的配体及配位原子分别是
(2)本实验减压过滤所需的主要仪器有抽气泵、吸滤瓶及
(3)根据题干信息分析步骤
 使用的洗涤剂为
使用的洗涤剂为(4)酸性滴定的离子反应方程式为
(5)已知:
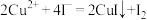 向滴定后的溶液加入足量的KI溶液,用0.6
向滴定后的溶液加入足量的KI溶液,用0.6
 溶液滴定,以淀粉溶液作指示剂,滴定终点的现象为
溶液滴定,以淀粉溶液作指示剂,滴定终点的现象为 溶液的体积为10.00mL。
溶液的体积为10.00mL。 ,步骤
,步骤 中配合物铜的物质的量
中配合物铜的物质的量(6)
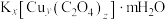 的化学式为:
的化学式为:
您最近一年使用:0次
7 . 亚硝酸钠 是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是
是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是
 是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是
是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是A.滴定前滴定管尖嘴处有气泡,滴定后无气泡会使测得的 含量偏高 含量偏高 |
B.亚硝酸根( )空间结构为V形 )空间结构为V形 |
| C.酸性高锰酸钾溶液可以鉴别食盐和亚硝酸钠 |
D.滴定过程离子反应为: |
您最近一年使用:0次
8 . Romanenko利用微生物电池将 针催化还原的工作原理如图所示,下列说法正确的是
针催化还原的工作原理如图所示,下列说法正确的是
 针催化还原的工作原理如图所示,下列说法正确的是
针催化还原的工作原理如图所示,下列说法正确的是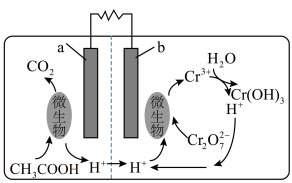
| A.b极电势比a极电势低 |
B.a极反应式: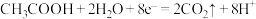 |
C.每处理1mol ,至少消耗 ,至少消耗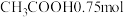 |
D.每生成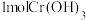 ,左池 ,左池 增加4mol 增加4mol |
您最近一年使用:0次
9 . 下列化学用语或表述正确的是
A. 的VSEPR模型为 的VSEPR模型为 |
B.Sc的原子结构示意图为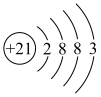 |
C.硼酸 的结构简式为 的结构简式为 |
D.等物质的量的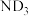 与 与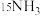 含有中子数前者多 含有中子数前者多 |
您最近一年使用:0次
名校
解题方法
10 . 以某铜矿石制备Cu(NO3)2晶体的工艺流程如图所示,已知铜矿石的主要成分为Cu2S和少量SiO2,滤液I中含Cu2+,滤渣I可回收单质S和SiO2。_______ 。
(2)铜矿石“氧化浸出”前需碾碎的目的是________ 。
(3)“滤液Ⅱ”中的金属阳离子为________ 。
(4)“反应”中生成Cu(NO3)2的离子方程式为________ 。
(5)“沉铁”后分离出沉淀的操作的名称为________ ,该操作在实验室进行时用到的玻璃仪器有________ 。
(6)“气体”与足量空气混合被水吸收过程中发生反应的化学方程式为________ ,其生成物可循环到上述流程中的________ (填“氧化浸出”“还原”“反应”或“沉铁”)过程中再利用。

(2)铜矿石“氧化浸出”前需碾碎的目的是
(3)“滤液Ⅱ”中的金属阳离子为
(4)“反应”中生成Cu(NO3)2的离子方程式为
(5)“沉铁”后分离出沉淀的操作的名称为
(6)“气体”与足量空气混合被水吸收过程中发生反应的化学方程式为
您最近一年使用:0次
2024-04-23更新
|
289次组卷
|
3卷引用:安徽省亳州市第二完全中学2023-2024学年高一下学期3月第一次月考化学试题



