解题方法
1 . 锌是一种应用广泛的金属。一种以闪锌矿(主要成分为ZnS,还含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:
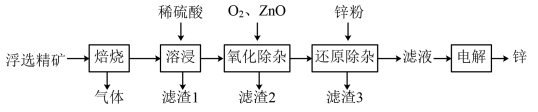
相关金属离子[c(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如表:
回答下列问题:
(1)焙烧过程中主要反应的化学方程式为____ 。
(2)滤渣1的主要成分除SiO2外还有____ 。
(3)氧化除杂工序中通入氧气的作用是____ ,ZnO的作用是____ 。
(4)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为____ 。为什么不能省去“还原除杂”步骤,直接在“氧化除杂”步骤中除去Cd2+____ 。
(5)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为____ ;沉积锌后的电解液可返回___ 工序继续使用。
(6)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质,“氧压酸浸”中发生的主要反应的离子方程式为____ 。

相关金属离子[c(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如表:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 | 7.4 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.2 | 9.4 |
(1)焙烧过程中主要反应的化学方程式为
(2)滤渣1的主要成分除SiO2外还有
(3)氧化除杂工序中通入氧气的作用是
(4)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为
(5)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为
(6)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质,“氧压酸浸”中发生的主要反应的离子方程式为
您最近一年使用:0次
解题方法
2 . 下列过程中的化学反应,相应的离子方程式正确的是
| A.“84消毒液”与洁厕灵(主要成分为浓盐酸)混用:ClO-+Cl-+2H+=Cl2↑+H2O |
B.石灰石与醋酸反应:CO +2CH3COOH=2CH3COO-+CO2↑+H2O +2CH3COOH=2CH3COO-+CO2↑+H2O |
| C.硫化亚铁加入稀硝酸中:FeS+2H+=Fe2++H2S↑ |
| D.硫酸铝溶液中滴加过量氢氧化钾溶液:Al3++3OH-=Al(OH)3↓ |
您最近一年使用:0次
2022-05-24更新
|
273次组卷
|
2卷引用:新疆克拉玛依市2022届高三第三次模拟检测理综化学试题
名校
3 . 利用反应CCl4+4Na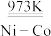 C(金刚石)+4NaCl可实现人工合成金刚石。下列关于该反应的说法错误的是
C(金刚石)+4NaCl可实现人工合成金刚石。下列关于该反应的说法错误的是
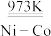 C(金刚石)+4NaCl可实现人工合成金刚石。下列关于该反应的说法错误的是
C(金刚石)+4NaCl可实现人工合成金刚石。下列关于该反应的说法错误的是 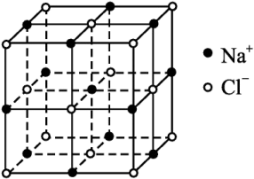
| A.C(金刚石)属于共价晶体 |
| B.该反应利用了Na的强还原性 |
| C.CCl4和C(金刚石)中的C的杂化方式相同 |
| D.NaCl晶胞如上图,NaCl晶体中每个Cl-周围有8个Na+ |
您最近一年使用:0次
2022-04-21更新
|
857次组卷
|
23卷引用:新疆克拉玛依市高级中学2021-2022学年高二下学期期末考试化学试题
新疆克拉玛依市高级中学2021-2022学年高二下学期期末考试化学试题山东省2020年普通高中学业水平等级考试模拟试题【省级联考】山东省2020届新高考模拟统考化学试题福建省莆田市仙游县第二中学2019-2020学年高二下学期期中考试化学试题山东省济南市章丘区第四中学2021届高三上学期第一次教学质量检测(8月)化学试题江苏省响水中学2020-2021学年高二上学期学情分析(一)化学试题(已下线)第37讲 晶体结构与性质(精练)-2021年高考化学一轮复习讲练测(鲁科版2019)选择性必修2 模块综合测评山东省济南市第一中学2021-2022学年高二下学期3月月考化学试题黑龙江省鸡西实验中学2021-2022学年高二下学期第一次月考化学试题广东省深圳市龙岗区龙城高级中学2021-2022学年高二下学期期中考试化学试题黑龙江省绥化市第九中学2021-2022学年高二下学期第二次月考化学试题黑龙江绥化市第一中学2021-2022学年高三下学期临考冲刺化学试题第三章 本章达标检测2江苏省苏州市2021-2022学年高二上学期期末模块测评化学试题黑龙江省绥化市第九中学2021-2022学年高二下学期期末考试化学试题山东省菏泽市单县第二中学2021-2022学年高二3月月考化学试题广东省梅州市大埔县虎山中学2022-2023学年高三上学期第一次段考(8月)化学试题(已下线)第31讲 晶体结构与性质(练)-2023年高考化学一轮复习讲练测(新教材新高考)山西省太原市英才学校2021-2022学年高二下学期线上期中化学试题山东省新泰市第一中学2022-2023学年高二下学期第一次大单元考试化学试题湖南省岳阳县第一中学2023-2024学年高二上学期1月期末化学试题四川省绵阳中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
4 . 一种用于合成治疗免疫疾病药的物质,其结构如图所示,其中X、Y、Z、Q、W为1~20号元素且原子序数依次增大,Z与Q同主族,Q和W的简单离子具有相同的电子层结构。下列叙述正确的是
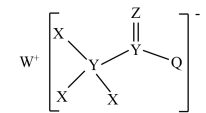

| A.第一电离能:Q>Z>W |
| B.电负性:X>Y>Z |
| C.WZX与WXQ均是强电解质,水溶液之间可以发生复分解反应 |
| D.W2Q2Z3与X2QZ4溶液反应生成黄色浑浊和无色气体属于非氧化还原反应 |
您最近一年使用:0次
2022-03-10更新
|
451次组卷
|
6卷引用:新疆克拉玛依市高级中学2021-2022学年高二下学期期末考试化学试题
新疆克拉玛依市高级中学2021-2022学年高二下学期期末考试化学试题辽宁省铁岭市六校2021-2022学年高三下学期3月联考化学试题(已下线)提升卷04-【新高考新题型】2022年高考化学选择题标准化练习20卷(山东专用)(已下线)必刷卷04-2022年高考化学考前信息必刷卷(山东专用) 陕西省宝鸡市金台区2021-2022学年高二下学期期末考试化学试题新疆乌鲁木齐市第七十中学2021-2022学年高二下学期期中考试化学试题
解题方法
5 . 设NA为阿伏加德罗常数的值,下列说法正确的是
A.1L0.1mol·L-1NH4Cl溶液中, 的数量为0.1NA 的数量为0.1NA |
| B.2.0gH218O与D2O的混合物中所含中子数为NA |
| C.56gFe溶于过量硝酸,电子转移数为2NA |
| D.标准状况下,2.24LCCl4含有的共价键数为0.4NA |
您最近一年使用:0次
解题方法
6 . 由下列实验及现象能推出相应结论的是
| 实验 | 现象 | 结论 | |
| A | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状碳并产生刺激性气味 | 浓硫酸具有吸水性和强氧化性 |
| B | 向溶液中先滴加双氧水,再滴加KSCN溶液 | 溶液变血红色 | 原溶液中含有Fe2+ |
| C | 将石蜡油蒸汽通过炽热的碎瓷片,再将生成的气体通入溴水中 | 溴水褪色 | 产物为烷烃 |
| D | 将金属钠放在燃烧匙中点燃,迅速伸入集满CO2的集气瓶 | 集气瓶中产生大量白烟,瓶内有黑色颗粒产生 | CO2具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 已知NA是阿伏加德罗常数的值,下列说法正确的是
| A.1mol氮气与3mol氢气反应,生成的氨分子数目为2NA |
| B.14g聚乙烯与聚丙烯的混合物,含C-H键的数目为2NA |
| C.电解饱和食盐水,当阳极产生11.2LH2时,转移的电子数为NA |
| D.常温下,3L0.1mol•L-1FeCl3溶液所含Fe3+数目为0.3NA |
您最近一年使用:0次
名校
解题方法
8 . 今年一月以来,我国部分地区突发的新型冠状病毒肺炎威胁着人们的身体健康。以下是人们在面对“新型冠状病毒肺炎”时的一些认识,你认为符合科学道理的是
| A.家庭消毒时,消毒液越浓越好 |
| B.“84”消毒液与洁厕灵混用可以增强消毒效果 |
| C.该病毒可以通过气溶胶传播(指飞沫混合在空气中形成气溶胶),飞沫直径在1~100nm之间 |
| D.健康人员使用过的口罩不可按照生活垃圾分类丢弃,应视作医疗废弃物严格按照医疗废弃物有关流程处理。 |
您最近一年使用:0次
2021-11-03更新
|
255次组卷
|
3卷引用:新疆克拉玛依市2020届高三第三次模拟检测理综化学试题
9 . 目前新能源技术被不断利用,高铁电池技术就是科研机构着力研究的一个方向。
(1)高铁酸钾—锌电池(碱性介质)是一种典型的高铁电池,则该种电池负极材料是___________ 。
(2)工业上常采用NaClO氧化法生产高铁酸钾(K2FeO4),K2FeO4在碱性环境中稳定,在中性和酸性条件下不稳定。反应原理为:
Ⅰ.在碱性条件下,利用NaClO氧化Fe(NO3)3制得Na2FeO4:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4+3NaCl+6NaNO3+5H2O
Ⅱ.Na2FeO4与KOH反应生成K2FeO4,主要的生产流程如下:
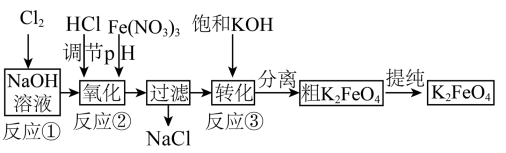
①写出反应①的离子方程式___________ 。
②请写出生产流程中“转化”(反应③)的化学方程式___________ 。
③该反应是在低温下进行的,说明此温度下Ksp(K2FeO4)___________ Ksp(Na2FeO4)(填“>”“<”或“=”)。
④“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用___________ 溶液。
a.H2O B.CH3COONa、异丙醇 C.NH4Cl、异丙醇 D.Fe(NO3)3、异丙醇
(3)已知K2FeO4在水溶液中可以发生:4 +10H2O
+10H2O 4Fe(OH)3+8OH-+3O2↑,则K2FeO4可以在水处理中的作用是
4Fe(OH)3+8OH-+3O2↑,则K2FeO4可以在水处理中的作用是___________ 。
(4) 在水溶液中的存在形态图如图所示。
在水溶液中的存在形态图如图所示。
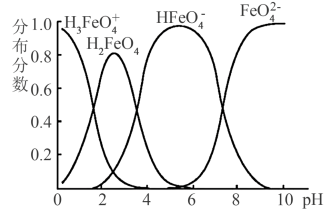
①若向pH=10的这种溶液中加硫酸至pH=2,HFeO 的分布分数的变化情况是
的分布分数的变化情况是___________ 。
②若向pH=6的这种溶液中滴加KOH溶液,则溶液中含铁元素的微粒中,___________ 转化为___________ 。(填化学式)
(1)高铁酸钾—锌电池(碱性介质)是一种典型的高铁电池,则该种电池负极材料是
(2)工业上常采用NaClO氧化法生产高铁酸钾(K2FeO4),K2FeO4在碱性环境中稳定,在中性和酸性条件下不稳定。反应原理为:
Ⅰ.在碱性条件下,利用NaClO氧化Fe(NO3)3制得Na2FeO4:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4+3NaCl+6NaNO3+5H2O
Ⅱ.Na2FeO4与KOH反应生成K2FeO4,主要的生产流程如下:

①写出反应①的离子方程式
②请写出生产流程中“转化”(反应③)的化学方程式
③该反应是在低温下进行的,说明此温度下Ksp(K2FeO4)
④“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
a.H2O B.CH3COONa、异丙醇 C.NH4Cl、异丙醇 D.Fe(NO3)3、异丙醇
(3)已知K2FeO4在水溶液中可以发生:4
 +10H2O
+10H2O 4Fe(OH)3+8OH-+3O2↑,则K2FeO4可以在水处理中的作用是
4Fe(OH)3+8OH-+3O2↑,则K2FeO4可以在水处理中的作用是(4)
 在水溶液中的存在形态图如图所示。
在水溶液中的存在形态图如图所示。
①若向pH=10的这种溶液中加硫酸至pH=2,HFeO
 的分布分数的变化情况是
的分布分数的变化情况是②若向pH=6的这种溶液中滴加KOH溶液,则溶液中含铁元素的微粒中,
您最近一年使用:0次
2021-11-03更新
|
739次组卷
|
3卷引用:新疆克拉玛依市2021届高三第三次模拟检测理综化学试题
10 . 雄黄(As4S4)具有驱虫解毒功效,雌黄(As2S3)是雄黄的伴生矿物,二者可以相互转化,转化过程如下,下列有关说法错误的是


| A.H2O参加了该转化过程 |
| B.若1 mol雄黄发生Ⅱ反应转移28 mol电子,则a为SO3 |
| C.已知亚砷酸具有两性,Ⅳ反应是酸碱中和反应 |
| D.As2O3是砒霜的主要成分,它是亚砷酸(H3AsO3)的酸酐 |
您最近一年使用:0次



