名校
解题方法
1 . 锌电解阳极泥(主要成分为 和
和 ,还有少量锰铅氧化物
,还有少量锰铅氧化物 和
和 )是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题:
)是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题: 易溶于水,不溶于乙醇
易溶于水,不溶于乙醇
②在较高温度及酸性催化条件下,葡萄糖能发生如图反应: 时
时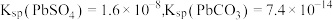
(1)已知 中
中 为
为 价,
价, 为
为 价和
价和 价,该氧化物中
价,该氧化物中 价和
价和 价
价 的物质的量之比为
的物质的量之比为_______ 。
(2)“还原酸浸”过程中主要反应的离子方程式为_______ ,该过程中实际葡萄糖加入量远大于理论需要量,其原因是_______ 。
(3)整个流程中可循环利用的物质是_______ (填名称)。获得 晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是
晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是_______ 。
(4)书写相关反应的离子方程式,并通过计算说明 时,可用
时,可用 溶液将“滤渣1”中的
溶液将“滤渣1”中的 完全转化为
完全转化为 的原因
的原因_______ 。
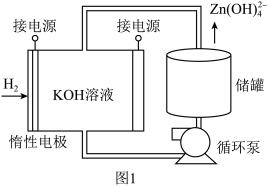
(5)通过氢电极增压法可制得单质锌,装置如图1所示。电解池工作时总反应的离子方程式为_______ 。 和
和 作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。
作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。
① 和
和 中
中 与
与 之间、
之间、 与
与 之间的离子键成分的百分数大小比较及解释
之间的离子键成分的百分数大小比较及解释_______ 。
② 晶胞结构如图2所示,其中
晶胞结构如图2所示,其中 代表
代表 。当
。当 位于晶胞的体心时,
位于晶胞的体心时, 于晶胞的
于晶胞的_______ 位置(填“顶点”“面心”“棱心”或“晶胞内”)。
 和
和 ,还有少量锰铅氧化物
,还有少量锰铅氧化物 和
和 )是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题:
)是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题: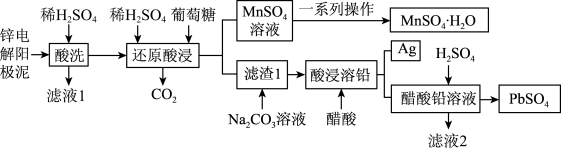
 易溶于水,不溶于乙醇
易溶于水,不溶于乙醇②在较高温度及酸性催化条件下,葡萄糖能发生如图反应:
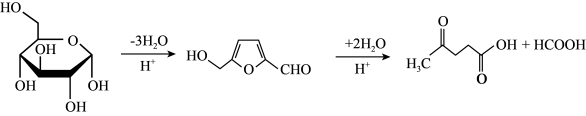
 时
时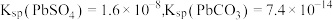
(1)已知
 中
中 为
为 价,
价, 为
为 价和
价和 价,该氧化物中
价,该氧化物中 价和
价和 价
价 的物质的量之比为
的物质的量之比为(2)“还原酸浸”过程中主要反应的离子方程式为
(3)整个流程中可循环利用的物质是
 晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是
晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是(4)书写相关反应的离子方程式,并通过计算说明
 时,可用
时,可用 溶液将“滤渣1”中的
溶液将“滤渣1”中的 完全转化为
完全转化为 的原因
的原因(5)通过氢电极增压法可制得单质锌,装置如图1所示。电解池工作时总反应的离子方程式为
 和
和 作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。
作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。①
 和
和 中
中 与
与 之间、
之间、 与
与 之间的离子键成分的百分数大小比较及解释
之间的离子键成分的百分数大小比较及解释②
 晶胞结构如图2所示,其中
晶胞结构如图2所示,其中 代表
代表 。当
。当 位于晶胞的体心时,
位于晶胞的体心时, 于晶胞的
于晶胞的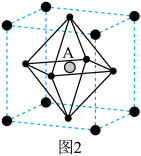
您最近一年使用:0次
7日内更新
|
94次组卷
|
2卷引用:新疆乌鲁木齐地区2024年高三下学期第三次质量监测化学试题
2 . 用氧化锌烟尘(主要成分为ZnO,还含有少量PbO、CuO、Fe2O3、FeO等)生产ZnSO4∙7H2O的流程如下(已知PbO不溶于稀硫酸酸):
(1)“酸浸”时用的稀酸是_______ (写名称)。
(2)加入NaClO的目的是_______ ,加入ZnO除杂时pH控制范围是_______ ~5.0。
(3)写出ZnO除杂得到滤渣2的离子反应方程式_______ 。
(4)滤渣3是_______ (写化学式) 。
(5)由滤液得到ZnSO4∙7H2O的操作是 蒸发浓缩、_______ 、 过滤、洗涤、干燥。
(6)已知Fe3+沉淀完全的标准为1.0×10-6mol。L-1,根据题目条件求常温下Fe(OH)3的Ksp=_______ 。

| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Cu2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 | 4.7 |
| 沉淀完全的pH | 3.0 | 8.3 | 8.2 | 6.7 |
(1)“酸浸”时用的稀酸是
(2)加入NaClO的目的是
(3)写出ZnO除杂得到滤渣2的离子反应方程式
(4)滤渣3是
(5)由滤液得到ZnSO4∙7H2O的操作是 蒸发浓缩、
(6)已知Fe3+沉淀完全的标准为1.0×10-6mol。L-1,根据题目条件求常温下Fe(OH)3的Ksp=
您最近一年使用:0次
名校
解题方法
3 . 实验小组同学欲探究 的性质并测定空气中
的性质并测定空气中 的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。
的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。_______ 。
(2)装置E的作用是_______ 。(用离子方程式表示)
(3)装置D用于验证 的
的_______ 性,发生的化学方程式为_______ 。
(4)装置C中的现象是_______ ;若将C中的溴水改为酸性高锰酸钾溶液,现象为_______ ,发生的离子方程式为_______ 。
(5)如果用硫酸溶液和 固体反应制取
固体反应制取 装置如图所示。其中a导管的作用是
装置如图所示。其中a导管的作用是_______ 。 含量(假设空气中无其他还原性气体)。
含量(假设空气中无其他还原性气体)。

实验中若通过空气的体积为 (标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是
(标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是_______ 。(结果精确到0.001%)
 的性质并测定空气中
的性质并测定空气中 的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。
的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。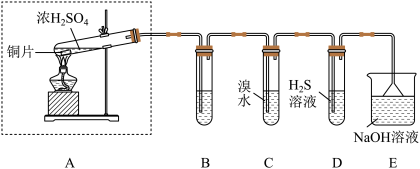
(2)装置E的作用是
(3)装置D用于验证
 的
的(4)装置C中的现象是
(5)如果用硫酸溶液和
 固体反应制取
固体反应制取 装置如图所示。其中a导管的作用是
装置如图所示。其中a导管的作用是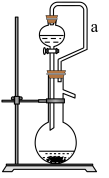
 含量(假设空气中无其他还原性气体)。
含量(假设空气中无其他还原性气体)。
实验中若通过空气的体积为
 (标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是
(标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是
您最近一年使用:0次
4 . 针对表中10种元素及由这些元素形成的单质和化合物,用元素符号或者化学式填写以下空格。
(1)最活泼的金属元素是___________ ,最活泼的非金属元素是___________ ,最不活泼的元素是___________ 。
(2)碱性最强的最高价氧化物对应水化物是___________ ,酸性最强的最高价氧化物对应水化物是___________ ,最稳定的气态氢化物是___________ 。
(3)在④与⑤中,还原性较强的是___________ ,在⑧与⑨的单质中,氧化性较强的是___________ 。
(4)④的最高价氧化物对应的水化物和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:___________ ;用电子式表示④和⑧形成的化合物的形成过程___________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
(2)碱性最强的最高价氧化物对应水化物是
(3)在④与⑤中,还原性较强的是
(4)④的最高价氧化物对应的水化物和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:
您最近一年使用:0次
名校
解题方法
5 . 根据要求回答下列问题:
(1)LiAlH4是有机合成中常用的还原剂,LiAlH4中阴离子的空间构型是___________ ,中心原子的杂化类型为___________ 。
(2)碳氧化物、氨氧化物、二氧化硫的处理和应用是世界各国研究的热点问题。SO2的VSEPR模型为___________ ;SO3的中心原子的杂化类型为___________ ;N2O与CO2互为等电子体,且N2O中O只与一个N相连,分子中的σ键和π键数目之比是___________ 。
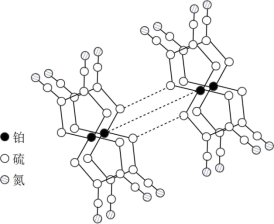
(3)某研究小组将平面形的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属”,其结构如图所示。___________ 能沿着其中的金属原子链流动。
(1)LiAlH4是有机合成中常用的还原剂,LiAlH4中阴离子的空间构型是
(2)碳氧化物、氨氧化物、二氧化硫的处理和应用是世界各国研究的热点问题。SO2的VSEPR模型为
(3)某研究小组将平面形的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属”,其结构如图所示。
您最近一年使用:0次
6 . 现有六种元素,其中A、B、C、D、E为短周期主族元素,F为第4周期元素,它们的原子序数依次增大。请根据下列相关信息回答问题。
(1)B元素基态原子具有___________ 种运动状态不同的电子,能量最高的电子,其电子云在空间有___________ 个伸 展方向。
(2)根据上述信息,画出C元素基态原子的轨道表示式___________ 。
(3)F在元素周期表中属于___________ 区元素。
(4)写出DA3的电子式:___________ (用元素符号表示)。
| 元素 | 相关信息 |
| A | 元素的原子核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 元素原子的核外p电子数比s电子数少1 |
| C | 元素的第一至第四电离能分别是I1=738 kJ/mol、I2=1451 kJ/mol、I3= 7733 kJ/mol、I4= 10540 kJ/mol |
| D | 原子核外填充电子的所有p轨道全满或半满 |
| E | 元素的主族序数与周期序数的差为3 |
| F | 在元素周期表的第6列 |
(2)根据上述信息,画出C元素基态原子的轨道表示式
(3)F在元素周期表中属于
(4)写出DA3的电子式:
您最近一年使用:0次
解题方法
7 . 以菱锰矿(主要成分为MnCO3,还含有铁、镍的碳酸盐以及SiO2杂质)为原料生产次锰酸钠(Na3MnO4)的工艺流程如图:
(1)次锰酸钠中Mn的化合价为___________ ;滤渣1的主要成分为MnO2和___________ (填化学式)。
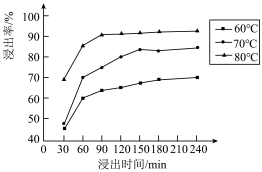
(2)锰的浸出率结果如图所示。由图可知,所采用的最佳实验条件为___________ 。___________ 。
(4)“除镍”步骤发生的反应为:MnS(s)+Ni2+(aq)=NiS(s)+Mn2+(aq)。反应的平衡常数K=___________ 。
(5)“母液1”中主要溶质的用途___________ 。
(6)煅烧产物MnO2在“共熔”过程中,反应得到Na2MnO4及一种单质气体,则该反应的化学方程式为___________ 。
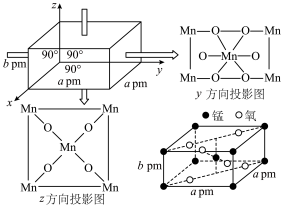
(7)某MnxO,四方晶胞结构及其投影如图所示,该晶胞由O2-和Mn3+构成。___________ ,Mn与Mn之间最近(顶点和体心)距离为___________ pm。(用含a、b的代数式表示)

| 物质 | MnS | NiS |
| Ksp | 2.0×10-13 | 1.0×10-21 |
(1)次锰酸钠中Mn的化合价为
(2)锰的浸出率结果如图所示。由图可知,所采用的最佳实验条件为
(4)“除镍”步骤发生的反应为:MnS(s)+Ni2+(aq)=NiS(s)+Mn2+(aq)。反应的平衡常数K=
(5)“母液1”中主要溶质的用途
(6)煅烧产物MnO2在“共熔”过程中,反应得到Na2MnO4及一种单质气体,则该反应的化学方程式为
(7)某MnxO,四方晶胞结构及其投影如图所示,该晶胞由O2-和Mn3+构成。
您最近一年使用:0次
解题方法
8 . 3,4-亚甲二氧基苯甲酸是一种用途广泛的有机合成中间体,微溶于水。实验室可用KMnO4氧化3,4-亚甲二氧基苯甲醛(油状液体)制备,实验装置如下图(夹持仪器已省略),其反应方程式为:
步骤1:向三颈烧瓶中加入3,4-亚甲二氧基苯甲醛11.2mL(约15.0g)和一定量水,缓慢开启搅拌器并加热。于70~80℃滴加稍过量的酸性KMnO4溶液,反应结束后,加入KOH溶液至碱性。
步骤2:趁热过滤,洗涤滤渣。合并滤液和洗涤液,向其中加入硫酸至水层不再产生沉淀。
步骤3:抽滤,洗涤,干燥,得3,4-亚甲二氧基苯甲酸固体12.2g。
回答下列问题:
(1)盛酸性KMnO4溶液的仪器的名称是___________ ;实验装置中长玻璃导管可用___________ 代替(填仪器名称)。
(2)反应结束后,加入KOH溶液前需向溶液中加入H2C2O4溶液在酸性条件下处理,发生反应的离子方程式为___________ 。
(3)步骤1中加入KOH溶液至碱性的目的是___________ 。
(4)步骤2中趁热过滤除去的物质是___________ (填化学式)。
(5)步骤3中检验产品是否洗净的操作为___________ 。
(6)写出步骤2中加入H2SO4发生的化学方程式___________ 。
(7)本实验3,4-亚甲二氧基苯甲酸的产率约为___________ %(保留两位小数)
3 +2KMnO4→2
+2KMnO4→2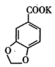 +
+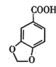 +2MnO2↓+H2O
+2MnO2↓+H2O
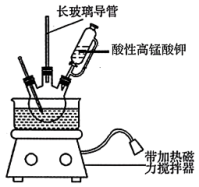
步骤1:向三颈烧瓶中加入3,4-亚甲二氧基苯甲醛11.2mL(约15.0g)和一定量水,缓慢开启搅拌器并加热。于70~80℃滴加稍过量的酸性KMnO4溶液,反应结束后,加入KOH溶液至碱性。
步骤2:趁热过滤,洗涤滤渣。合并滤液和洗涤液,向其中加入硫酸至水层不再产生沉淀。
步骤3:抽滤,洗涤,干燥,得3,4-亚甲二氧基苯甲酸固体12.2g。
回答下列问题:
(1)盛酸性KMnO4溶液的仪器的名称是
(2)反应结束后,加入KOH溶液前需向溶液中加入H2C2O4溶液在酸性条件下处理,发生反应的离子方程式为
(3)步骤1中加入KOH溶液至碱性的目的是
(4)步骤2中趁热过滤除去的物质是
(5)步骤3中检验产品是否洗净的操作为
(6)写出步骤2中加入H2SO4发生的化学方程式
(7)本实验3,4-亚甲二氧基苯甲酸的产率约为
您最近一年使用:0次
9 . 利用含钴废料(主要成分为Co、Ni、Mn、Pb以及 、
、 等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示:
等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示:
(1)基态Co原子的价电子原子轨道表达式为_______ 。铂钴合金具有较高的永磁性能,其晶胞如图所示,若A点Pt原子的坐标参数为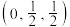 ,则B点Pt原子的坐标参数为
,则B点Pt原子的坐标参数为______ 。_______ 。“酸浸”时 发生反应的总离子方程式为
发生反应的总离子方程式为_______ 。
(3)酸浸后滤渣的主要成分为______ 。
(4)“沉锰”时, 转化为
转化为 ,则“沉锰”时发生反应的离子方程式为:
,则“沉锰”时发生反应的离子方程式为:_______ 。
(5)可以通过电解 溶液获得单质Co和较浓的盐酸,其工作原理如图所示:
溶液获得单质Co和较浓的盐酸,其工作原理如图所示:______ (填“膜a”或者“膜b”)。阴极的电极方程式为:_______ 。
 、
、 等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示:
等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示: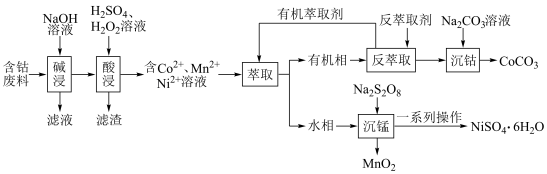
(1)基态Co原子的价电子原子轨道表达式为
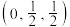 ,则B点Pt原子的坐标参数为
,则B点Pt原子的坐标参数为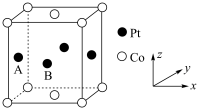
 发生反应的总离子方程式为
发生反应的总离子方程式为(3)酸浸后滤渣的主要成分为
(4)“沉锰”时,
 转化为
转化为 ,则“沉锰”时发生反应的离子方程式为:
,则“沉锰”时发生反应的离子方程式为:(5)可以通过电解
 溶液获得单质Co和较浓的盐酸,其工作原理如图所示:
溶液获得单质Co和较浓的盐酸,其工作原理如图所示: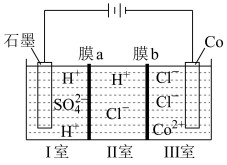
您最近一年使用:0次
10 . 金属钨是重要的战略资源,由黑钨矿(主要成分为 、
、 ,含有少量Si、As的化合物)制取金属钨的流程如图所示:
,含有少量Si、As的化合物)制取金属钨的流程如图所示:
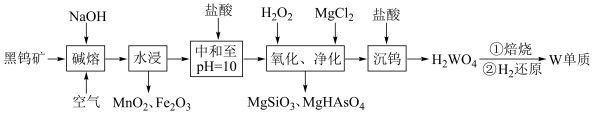
已知:常温下钨酸( )难溶于水,酸性很弱,其钠盐易溶于水。
)难溶于水,酸性很弱,其钠盐易溶于水。
回答下列问题:
(1)已知元素周期表中74号元素钨与铬同族,钨在元素周期表中的位置是第六周期第________ 族。 中铁元素的化合价为
中铁元素的化合价为________ 。
(2)“碱熔”步骤中为提高反应速率,可以将黑钨矿预先________ ,“碱熔”过程 发生反应的化学方程式为
发生反应的化学方程式为________ 。
(3)上述流程中加盐酸中和至pH=10时,溶液中的杂质阴离子有 、
、 、
、 等,则“氧化、净化”过程中,先加入
等,则“氧化、净化”过程中,先加入 发生反应的离子方程式为
发生反应的离子方程式为________ 。
(4)沉钨过程中,判断 是否沉淀完全的方法是
是否沉淀完全的方法是________ 。
(5)钨酸钙( )和氢氧化钙都是微溶电解质。某温度下
)和氢氧化钙都是微溶电解质。某温度下 和
和 的饱和溶液中,
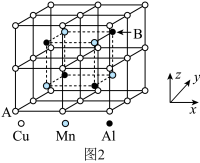
的饱和溶液中,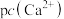 与pc(阴离子)的关系如图1所示,已知:pc(离子)=-lgc(离子)。该温度下将
与pc(阴离子)的关系如图1所示,已知:pc(离子)=-lgc(离子)。该温度下将 溶液加入石灰乳中得到大量钨酸钙,该反应的平衡常数K=
溶液加入石灰乳中得到大量钨酸钙,该反应的平衡常数K=________ 。
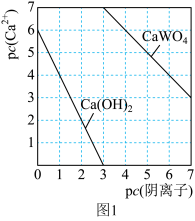
(6)合金具有比金属单质更优越的性能,Cu-Mn-Al合金为磁性形状记忆合金材料之一,其晶胞结构如图2所示。该合金的化学式为________ 。若A原子的坐标参数为(0,0,0),则B原子的坐标参数为________ 。
 、
、 ,含有少量Si、As的化合物)制取金属钨的流程如图所示:
,含有少量Si、As的化合物)制取金属钨的流程如图所示:
已知:常温下钨酸(
 )难溶于水,酸性很弱,其钠盐易溶于水。
)难溶于水,酸性很弱,其钠盐易溶于水。回答下列问题:
(1)已知元素周期表中74号元素钨与铬同族,钨在元素周期表中的位置是第六周期第
 中铁元素的化合价为
中铁元素的化合价为(2)“碱熔”步骤中为提高反应速率,可以将黑钨矿预先
 发生反应的化学方程式为
发生反应的化学方程式为(3)上述流程中加盐酸中和至pH=10时,溶液中的杂质阴离子有
 、
、 、
、 等,则“氧化、净化”过程中,先加入
等,则“氧化、净化”过程中,先加入 发生反应的离子方程式为
发生反应的离子方程式为(4)沉钨过程中,判断
 是否沉淀完全的方法是
是否沉淀完全的方法是(5)钨酸钙(
 )和氢氧化钙都是微溶电解质。某温度下
)和氢氧化钙都是微溶电解质。某温度下 和
和 的饱和溶液中,
的饱和溶液中,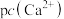 与pc(阴离子)的关系如图1所示,已知:pc(离子)=-lgc(离子)。该温度下将
与pc(阴离子)的关系如图1所示,已知:pc(离子)=-lgc(离子)。该温度下将 溶液加入石灰乳中得到大量钨酸钙,该反应的平衡常数K=
溶液加入石灰乳中得到大量钨酸钙,该反应的平衡常数K=
(6)合金具有比金属单质更优越的性能,Cu-Mn-Al合金为磁性形状记忆合金材料之一,其晶胞结构如图2所示。该合金的化学式为

您最近一年使用:0次



