10. 甲醇和乙醇都是清洁能源,也是重要的化工原料。回答下列问题:
(1)工业上利用合成气合成甲醇:


,已知:几种热化学方程式如下:

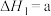
kJ⋅mol


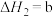
kJ⋅mol



kJ⋅mol

则上述反应中的
 ______
______kJ⋅mol

(用含有a,b,c的式子表示)。
(2)一定温度下,在恒容密闭容器中充入1 mol CO和1 mol

,在固体催化剂作用下合成甲醇:
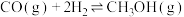
,下列叙述正确的是_____(填字母)。
A.当 体积分数不变时达到平衡状态 体积分数不变时达到平衡状态 |
| B.平衡后充入少量氩气,平衡向左移动 |
C.平衡后再充入0.1 mol CO和0.1 mol  ,CO平衡转化率增大 ,CO平衡转化率增大 |
| D.平衡后增大催化剂表面积,逆反应速率大于正反应速率 |
(3)甲醇是一种潜在储氢材料。我国学者研究甲醇在钯基催化剂表面上分解制氢:
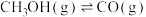
,其反应历程如图所示(吸附在催化剂表面的物种用“*”表示)。
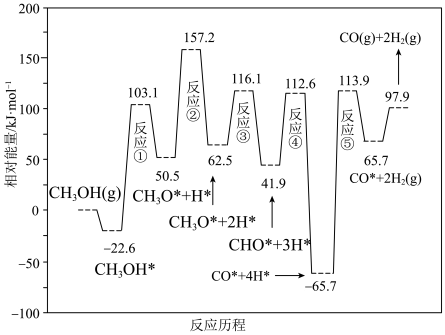
总反应的焓变为
______kJ/mol;该反应的决速步为
____(填反应后的序号):总反应经历5步反应中,最大能垒为
_____kJ⋅mol

,写出该步反应式:
________。
(4)工业上,可以采用

催化还原制备

、

。发生反应如下:
①

(主反应)
②

(主反应)
③

(副反应)
一定温度下,在甲、乙体积相同的反应容器中分别充入1 mol

和3 mol

,发生上述反应,其中一个容器使用水分子膜分离技术,另一个容器不使用水分子膜分离技术。实验测得

平衡转化率与压强关系如图所示。

其他条件相同,增大压强,

平衡转化率增大,其原因是
______;采用水分子膜分离技术的容器是
_____(填“甲”或“乙”)。
(5)一定温度下,向总压强恒定为100kPa的反应器中充入1 mol

和3 mol

,发生(4)中反应①②③,达到平衡时

转化率为50%,甲醇选择性为

,生成0.05 mol

,则反应①的平衡常数

为
______
(写出数字表达式即可)[用分压计算的平衡常数为压强平衡常数

,分压=总压×物质的量分数;甲醇选择性:

]。