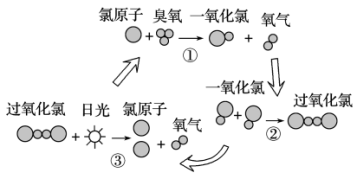
环状碳酸酯广泛用于极性非质子溶剂、电池的电解质等,离子液体研究团队近期报道了一种环氧乙烷衍生物与二氧化碳催化合成环状碳酸酯的反应历程如图所示。已知:R表示烃基。
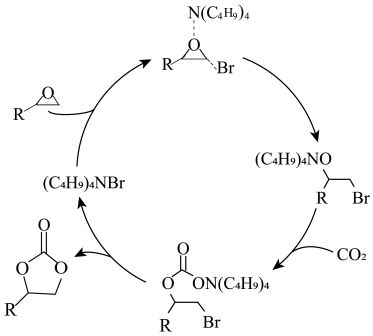
| A.(C4H9)4NBr是反应的催化剂 |
| B.反应过程存在非极性键的断裂和形成 |
| C.反应过程中有3种中间体 |
| D.总反应原子利用率可达100% |
更新时间:2022-08-19 20:37:56
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】在一定的温度和压强下,将按一定比例混合的 和
和 通过装有催化剂的反应器可得到甲烷。已知:
通过装有催化剂的反应器可得到甲烷。已知:



催化剂的选择是 甲烷化技术的核心。在两种不同催化剂作用下反应相同时间,测
甲烷化技术的核心。在两种不同催化剂作用下反应相同时间,测 转化率和生成
转化率和生成 选择性[
选择性[ 选择性=
选择性=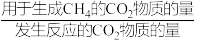 ×100%]随温度变化的影响如图所示。下列有关说法正确的是
×100%]随温度变化的影响如图所示。下列有关说法正确的是
 和
和 通过装有催化剂的反应器可得到甲烷。已知:
通过装有催化剂的反应器可得到甲烷。已知:
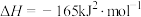


催化剂的选择是
 甲烷化技术的核心。在两种不同催化剂作用下反应相同时间,测
甲烷化技术的核心。在两种不同催化剂作用下反应相同时间,测 转化率和生成
转化率和生成 选择性[
选择性[ 选择性=
选择性=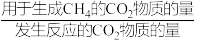 ×100%]随温度变化的影响如图所示。下列有关说法正确的是
×100%]随温度变化的影响如图所示。下列有关说法正确的是
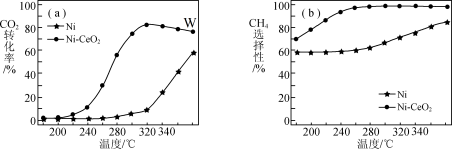
A.在260℃-320℃间,以 为催化剂,升高温度相同时间内 为催化剂,升高温度相同时间内 的产率不变 的产率不变 |
B.延长W点的反应时间,一定能提高 的转化率 的转化率 |
C. 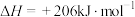 |
D.高于320℃后,以Ni为催化剂,随温度的升高 转化率上升的原因是催化剂活性增大,反应速率加快 转化率上升的原因是催化剂活性增大,反应速率加快 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】某课题组研究煤燃烧过程中氮氧化物与砷反应的微观机理,得到如下数据和图象。已知:反应速率为反应物浓度和速率常数 的函数,
的函数, 为活化能。对于所研究的三个反应,下列说法错误的是
为活化能。对于所研究的三个反应,下列说法错误的是

 的函数,
的函数, 为活化能。对于所研究的三个反应,下列说法错误的是
为活化能。对于所研究的三个反应,下列说法错误的是反应 |
|
| 78.45 |
| 2.58 |
| 155.85 |

A.相同条件下的氧化性: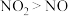 |
| B.相同条件下,As与NO的反应速率最慢 |
C.升高温度能增大As与 反应的活化能 反应的活化能 |
D.其他条件不变,改变温度不能显著改变As与 的反应速率 的反应速率 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
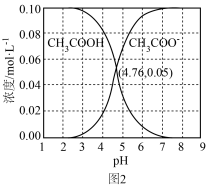
【推荐1】图1为CO2与CH4转化为CH3COOH的反应历程(中间体的能量关系如虚框中曲线所示),图2为室温下某溶液中CH3COOH和CH3COO-两种微粒浓度随pH变化的曲线。下列结论错误的是
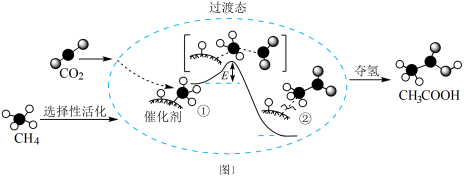
| A.CH4分子在催化剂表面会断开C—H键,断键会吸收能量 |
| B.中间体①的能量大于中间体②的能量 |
| C.室温下,CH3COOH的电离常数Ka=10-4.76 |
| D.升高温度,图2中两条曲线交点会向pH增大方向移动 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】中山大学化学科研团队首次将CsPbBr3纳米晶锚定在氨基化RGO包覆的α—Fe2O3(α—Fe2O3/Amine—RGO/CsPbBr3),构筑Z—Scheme异质结光催化剂,可有效降低电荷复合,促进电荷分离,从而提升光催化性能。光催化还原CO2和氧化H2O的反应路径如图。下列说法正确的是( )
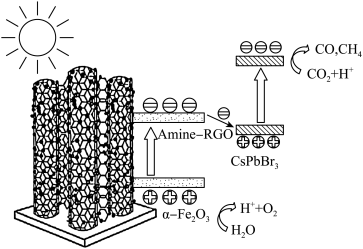

| A.该路径能量转化形式为电能→化学能 |
| B.该光催化转化反应可以阻止温室效应 |
| C.“CsPbBr3纳米晶”表面发生了还原反应 |
| D.该催化转化的总反应涉及到非极性共价键、极性共价键的断裂和形成 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】生产环氧乙烷( )的反应为: 2CH2=CH2(g) + O2(g)
)的反应为: 2CH2=CH2(g) + O2(g)  2
2  (g) △H=-106 kJ/mol
(g) △H=-106 kJ/mol
其反应机理如下:
①Ag + O2→AgO2 慢 ②CH2=CH2 + AgO2→ +AgO 快
+AgO 快
③CH2=CH2 + 6AgO→2CO2+2H2O+6Ag 快
下列有关该反应的说法正确的是( )
 )的反应为: 2CH2=CH2(g) + O2(g)
)的反应为: 2CH2=CH2(g) + O2(g)  2
2  (g) △H=-106 kJ/mol
(g) △H=-106 kJ/mol其反应机理如下:
①Ag + O2→AgO2 慢 ②CH2=CH2 + AgO2→
 +AgO 快
+AgO 快③CH2=CH2 + 6AgO→2CO2+2H2O+6Ag 快
下列有关该反应的说法正确的是( )
| A.反应的活化能等于 106 kJ/mol | B.AgO2也是该反应的催化剂 |
| C.增大乙烯的浓度能显著提高环氧乙烷的生成速率 | D.该反应的原子利用率为100% |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】我国自主研发对二甲苯的绿色合成路线取得新进展,其合成示意图如图。
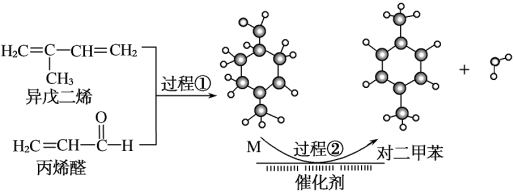
下列说法正确的是( )

下列说法正确的是( )
| A.过程①发生了取代反应 |
B.中间产物M的结构简式为 |
| C.利用相同原理以及相同原料,也能合成邻二甲苯和间二甲苯 |
| D.该合成路线原子利用率为100%,最终得到的产物易分离 |
您最近半年使用:0次


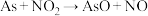

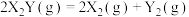 ,其速率方程为
,其速率方程为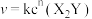 ,已知部分信息如下:
,已知部分信息如下: 为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:
为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:




 起始浓度为
起始浓度为 ,则反应物浓度减半所需时间为
,则反应物浓度减半所需时间为
 时
时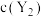 可能小于
可能小于